C R

126
La Lettre de l’Infectiologue - Tome XIV - n° 3 - mars 1999
RÉUNIONS GEMHEP
Cette journée s’est tenue le 15 janvier 1999 au Centre Chaillot-
Galliera (Paris). Le thème était les “Données récentes sur les
virus des hépatites”, mais une grande partie du congrès a été
consacrée au virus de l’hépatite C (VHC).
TRANSPLANTATION HÉPATIQUE ET VIRUS DE L’HÉPATITE C
C. Feray (Paris) a rappelé que la transplantation hépatique
concernait 600 patients par an. Dans le cas d’une transplanta-
tion hépatique liée à une infection par le VHC, la récidive spon-
tanée sur le greffon est très fréquente : récidive virologique (pré-
sence de l’ARN-VHC dans le greffon ou dans le sérum) dans
plus de 90 % des cas dès le premier mois, récidive histopatho-
logique (survenue d’une hépatite sur le greffon puis à terme
d’une cirrhose) dans 75 % des cas, 4 ans après transplantation.
Chez le transplanté, l’infection du greffon par le virus de l’hé-
patite C est plus sévère que chez le sujet immunocompétent,
avec une progression accélérée vers la cirrhose. Il semble exis-
ter une corrélation entre le génotype viral et la sévérité de la
maladie : le génotype 1b du VHC serait associé à des récidives
histologiques plus graves sur le greffon. Ces souches 1b indui-
raient une réponse immune et une apoptose plus importantes
que les autres génotypes entraînant une évolution plus rapide
vers la fibrose. En fait, le génotype viral n’est probablement
que le marqueur indirect de mutations définissant des souches
virales associées à une pathogénicité accrue.
Lors de l’infection du greffon, il existe un haut niveau de répli-
cation du VHC. La charge virale intrahépatique mesurée au
moment de l’hépatite aiguë est très significativement prédic-
tive de l’évolution vers la cirrhose. Pendant cette phase, les pro-
priétés pathogéniques directes du VHC prédominent en raison
de l’immunosuppression thérapeutique. Par la suite, l’immu-
nosuppression étant progressivement diminuée, la réponse
immune antivirale se développe, et on observe une diminution
de la réplication intrahépatique du VHC lors de l’évolution vers
l’hépatite chronique.
L’utilisation précoce post-transplantation d’une bithérapie asso-
ciant interféron et ribavirine semble donner des résultats inté-
ressants, puisque près de la moitié des patients présentent une
négativation de l’ARN-VHC plasmatique. Néanmoins, la
réponse virologique à long terme n’est que rarement obtenue.
L’interféron doit être utilisé avec prudence, car il peut être à
l’origine d’un rejet chronique du greffon.
CHARGE VIRALE VHC : TECHNIQUES ET APPLICATIONS
J.P. Zarski (Grenoble) a présenté les différentes techniques
de mesure de la charge virale du VHC ainsi que leurs applica-
tions.
Te c hniques
Les techniques de détection de l’ARN du VHC par PCR qua-
litative dans le sang sont actuellement les plus sensibles. Le test
Amplicor™ HCV Roche a une sensibilité de 100 à 1 000 copies/ml
de sérum. La nouvelle version du test Amplicor™ HCV, dont
le seuil de détection est de 100 copies/ml, est maintenant dis-
ponible. Leur grande sensibilité rend ces tests particulièrement
indiqués dans le diagnostic de l’infection à VHC et dans le suivi
d’un traitement antiviral.
La quantification de l’ARN du VHC dans le sang fait appel à deux
types de techniques : technique d’amplification de la cible par PCR
(Amplicor™ HCV Monitor 2.0) ou technique d’amplification du
signal d’hybridation par ADN branché (Quantiplex™ HCVRNA
2.0, Chiron Diagnostic). Le seuil de détection est de 1 000 copies/ml
pour le test Monitor™ 2.0 et de 200 000 Eq.génomes/ml pour le
test Quantiplex™ 2.0. Ces tests de deuxième génération quantifient
de manière équivalente les différents génotypes.
Applications de la mesure de la charge virale du VHC
Épidémiologie. Le niveau de la charge virale plasmatique du
VHC intervient dans le risque de contamination en cas de trans-
mission nosocomiale, sexuelle ou mère-enfant. Les études réa-
lisées dans le cadre de la transmission mère-enfant montrent
que seules les mères ayant une charge virale élevée sont sus-
ceptibles de transmettre l’infection, celle-ci n’étant cependant
pas constante. En l’absence de standardisation des tests, il est
impossible de définir avec précision les seuils permettant d’éva-
luer le risque de transmission.
! Évaluation de la gravité de la maladie. Il n’existe pas de
corrélation entre le niveau de la réplication virale et la sévérité
de la maladie. Néanmoins, au stade de cirrhose C sévère, la
charge VHC diminue de façon significative du fait de la raré-
faction des hépatocytes.
! Prise en charge thérapeutique. Plusieurs études ont mon-
tré que la charge VHC plasmatique préthérapeutique était un
facteur prédictif indépendant de la réponse au traitement. Les
patients ayant une charge virale basse ont un taux de réponse
prolongée significativement supérieur à ceux ayant une charge
élevée. La limite entre charge “élevée” et “basse” varie selon
les études. Elle est de l’ordre de 2 x 106Eq.génomes/ml pour
le QuantiplexTM 2.0 et de 105copies/ml pour le test MonitorTM.
À l’échelon individuel, il est impossible de prédire avec certi-
tude la réponse en fonction de la charge virale. Le développe-
ment de nouvelles stratégies thérapeutiques (modes d’admi-
nistration différents de l’interféron, association de molécules
anti-VHC) permettra l’adaptation du traitement à chaque
malade en fonction des facteurs prédictifs de réponse, notam-
ment de la charge virale préthérapeutique.
3eJournée annuelle du Groupe d’étude moléculaire
des hépatites

En cours de traitement, la mesure de la charge virale pourrait
permettre d’évaluer l’efficacité du traitement sur la réplication
virale. En effet, on observe fréquemment une dissociation entre
l’évolution des transaminases et celle de la charge virale, en
particulier en cas d’association interféron-ribavirine. Le suivi
de la charge pendant et après traitement est donc le seul moyen
permettant d’apprécier l’effet du traitement sur le virus. Par
ailleurs, la cinétique de décroissance de la charge VHC obser-
vée en début de traitement serait un facteur prédictif de réponse
prolongée. Des études prospectives contrôlées et randomisées
sont en cours.
! Suivi après transplantation hépatique. Chez les patients
transplantés pour cirrhose virale C, lors de la réinfection du
greffon, on observe un pic de virémie précédant de quelques
jours l’hépatite aiguë avec une élévation significative de la
charge virale par rapport à son niveau pré-greffe. L’observation
de ces pics permettrait de faire la preuve d’une hépatite liée à
la réinfection du greffon.
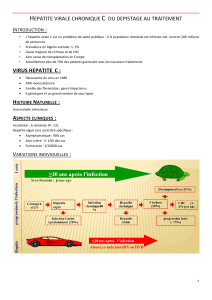
TRAITEMENT DE L’HÉPATITE CHRONIQUE C PAR L’ASSOCIA-
TION INTERFÉRON-RIBAVIRINE
P. Marcellin (Paris) a rapporté les résultats des dernières études
concernant le traitement des patients porteurs d’une hépatite C
chronique par l’association interféron-ribavirine.
Chez les patients naïfs, l’association interféron-ribavirine
entraîne une réponse complète prolongée chez 33 à 48 % des
patients versus 6 à 18 % pour ceux traités par l’interféron seul.
Deux études récentes incluant plus de 1 700 patients (Poynard
et coll. Lancet 1998 ; 352 : 1426-32 ; McHutchison et coll.
N Engl J Med 1998 ; 339 : 1485-92) montrent la supériorité de
l’association interféron-ribavirine (31 à 35 % de réponse viro-
logique prolongée après 6 mois de bithérapie, 38 à 43 % après
12 mois) par rapport à l’interféron en monothérapie (13 à 19 %
après 12 mois). Les patients infectés par un génotype 2 ou
3 et/ou présentant une charge virale 2 x 106Eq.génomes/ml
ont une réponse virologique prolongée de 47 à 64 % après
un traitement d’un an. Chez les patients infectés par un
génotype 1, 4, 5, ou 6 et/ou présentant une charge
virale>2x10
6Eq.génomes/ml, la réponse virologique prolon-
gée est de 30 à 40 % après un traitement d’un an. Ces résultats
doivent inciter à traiter les patients par l’association interféron-
ribavirine, qui peut désormais être considérée comme le traite-
ment de choix de l’hépatite C chronique.
Chez les patients ayant rechuté après un premier traitement par
l’interféron, une étude portant sur 345 patients (Davis et coll.
N Engl J Med 1998 ; 21 : 1493-9) a montré l’efficacité de la
bithérapie. Une réponse virologique prolongée a été obtenue
chez 49 % des patients traités par l’association interféron-riba-
virine contre 5 % chez ceux traités par l’interféron seul pen-
dant six mois. Une amélioration significative de l’histologie
hépatique a pu être obtenue avec la bithérapie.
Les patients non répondeurs à un premier traitement par l’in-
terféron en monothérapie ont des taux de réponse faibles en
bithérapie, allant de 0 à 19 %.
L’association interféron-ribavirine est généralement bien tolé-
rée. La ribavirine est responsable de l’apparition d’une anémie
hémolytique chez environ 30 % des patients, nécessitant par-
fois une réduction des doses. L’utilisation de ribavirine présente
un risque cardiovasculaire, en particulier chez les patients athé-
romateux.
FACTEURS VIRAUX DE RÉSISTANCE AUX TRAITEMENTS :
EXEMPLE DU VHC
J.M. Pawlotsky (Paris) a rappelé les différents paramètres viro-
logiques identifiés comme prédictifs de la réponse virale pro-
longée après traitement.
! Charge virale préthérapeutique et génotype. Un génotype
2 ou 3 ainsi qu’une faible charge virale sont indépendamment
associés à une forte probabilité de réponse virologique soute-
nue chez les sujets traités par interféron seul ou associé à la
ribavirine.
! Cinétique de réplication virale. Les études de dynamique
virale montrent que la demi-vie du VHC dans la circulation
périphérique est d’environ 3 heures, et 1012 particules virales
sont produites quotidiennement. Lors d’une administration
intermittente d’interféron (3 injections par semaine), la chute
de la charge virale dans les 24 heures qui suivent l’injection est
suivie d’un rebond à 48 heures. Ce rebond n’est pas observé
lorsque l’injection d’interféron est quotidienne. L’administra-
tion quotidienne de fortes doses d’interféron provoque dans les
deux premiers jours du traitement une diminution rapide de la
charge virale, cette diminution étant dose-dépendante. Un trai-
tement agressif de l’hépatite C permettrait ainsi un contrôle pré-
coce de la réplication virale augmentant le taux de réponse viro-
logique prolongée.
! Chez un sujet infecté, le VHC circule sous forme d’un
mélange de variants viraux génétiquement distincts définissant
une répartition en quasi-espèces. La complexité génétique
des quasi-espèces du VHC avant traitement chez un patient
donné semble être un paramètre prédictif indépendant de la
réponse virologique soutenue. Seuls les patients présentant une
faible complexité génétique de leur quasi-espèce circulante
pourraient éliminer le virus après un traitement standard par
l’interféron.
! La présence de séquences particulières dans certaines régions
du génome, notamment la région NS5A, pourrait également
être associée à la résistance des souches au traitement. La pro-
téine NS5A inhiberait l’autophosphorylation de la protéine
kinase, indispensable à son action antivirale.
L’interféron exerce une pression de sélection qui modifie pro-
fondément la composition des sous-populations virales circu-
lantes. Chez les malades résistants au traitement, des sous-popu-
lations majoritaires avant traitement vont disparaître ou devenir
minoritaires, alors que des variants minoritaires avant traite-
ment vont être sélectionnés en raison de leur meilleure adap-
tation aux nouvelles conditions environnementales.
P. Trimoulet, Bordeaux
La Lettre de l’Infectiologue - Tome XIV - n° 3 - mars 1999
127
RÉUNIONS
GEMHEP
1
/
2
100%