Alcools, aldéhydes, cétones et acides carboxyliques, liaison

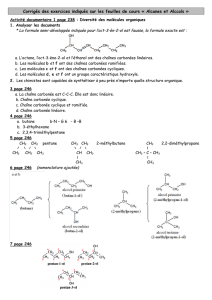
Alcools, aldéhydes, cétones et acides carboxyliques, liaison hydrogène
Le cours complet sur les composés oxygénés de Thierry Collet en vidéo
http://www.youtube.com/watch?v=oXHs226jMdY&feature=youtu.be
ou chapitre par chapitre
http://thierry.col2.free.fr/restreint/exovideo_lycee/1S_18_composes_organiques_oxygenes.htm
Nomenclature des composés oxygénés (cf fin du polycopié)
Exercice 1 : Test sur les familles de composés oxygénés
http://www.ostralo.net/4_exercices_jeux/premiereS_chimie/chimIIB2/exo_fonctions.swf
Exercice 2: Test sur les alcools
http://www.micromega-hatier.com/enligne1S/c24_qcm.html
Aide : http://www.micromega-hatier.com/enligne1S/c24_bilan.html
Exercice 3: Test sur les acides
http://www.micromega-hatier.com/enligne1S/c25_qcm.html
Aide http://www.micromega-hatier.com/enligne1s/c25_bilan.html
Exercice 4: Connaître les molécules (alcanes, composés oxygénés)
http://www.ostralo.net/3_animations/swf/alcane.swf
http://www.ostralo.net/4_exercices_jeux/premiereS_chimie/chimIIB2/exo_fonctions.swf
Qcm : http://www.sciencesslsc.fr/index.php?niveau=1&chapitre=10
Exercice 5 : Composés oxygénés
http://scphysiques2010.voila.net/1sch08c.htm#_Toc323274740

Exercice 6 : Modèles moléculaires et formules
4
5
6
7
8
1
2
3
Tableau 1
Formule semi-développée
Formule brute
Fonction organique

12
10
11
1
9
Tableau 1 (suite)
Formule semi-développée
Formule brute
Fonction organique
15
16
13
14

Corrigé
Formule semi-développée
Formule
brute
Fonction
organique
1
CH3-CH2-CH=CH-CH3
C5H10
Alcène
2
CH3-CH=CH-CH3
C4H8
Alcène
3
CH3-CH2-CH2-CH2-OH
C4H10O
Alcool I
4
CH3-CH2-CH-CH3
CH3
C5H12
Alcane
5
CH3-CH2-CH2-CH2-CH=CH3
C6H12
Alcène
6
CH3-CH2-CH2-CH=O
C4H8O
Aldéhyde
7
CH3-CH2-CH2-CH2 -CH2- OH
C5H12O
Alcool I
8
CH3-CO-CH2-CH3
C4H8O
Cétone

9
CH3-CH2-CH-CH2 -CH3
OH
C5H12O
Alcool II
10
CH3-CH=CH-CH2-CH2-CH3
C6H12
Alcène
11
CH3-CH=CH-CH3
C4H8
Alcène
12
CH3-CH2-CH2-CH2-CH3
C5H12
Alcane
13
CH3-CH-CH2-CH2 -CH3
OH
C5H12O
Alcool II
14
CH3 -CH2-CH=CH-CH2-CH3
C6H12
Alcène
15
CH3-CH2-CH=CH-CH3
C5H10
Alcène
16
CH3-O-CH2-CH2-CH3
C4H10O
Ether-
oxyde
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
1
/
12
100%