ETUDE D`UN GRAPHE n°1 La réaction entre l`hydrogène sulfureux

ETUDE D’UN GRAPHE n°1
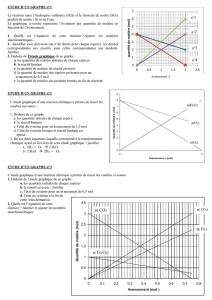
La réaction entre l’hydrogène sulfureux (H2S) et le dioxyde de soufre (SO2)
produit du soufre ( S) et de l’eau.
Le graphique ci-contre représente l’évolution des quantités de matière en
fonction de l’avancement.
1. Quelle est l’équation de cette réaction ? Ajuster les nombres
stœchiométriques
2. Identifier avec précision (un n°de droite pour chaque espèce) les droites
correspondantes aux réactifs puis celles correspondantes aux produits.
Justifier.
3. Déduire de l’étude graphique de ce graphe :
a. les quantités de matière initiales de chaque espèces
b. le réactif limitant
c. la quantité de matière du réactif en excès
d. la quantité de matière des espèces présentes pour un
avancement de 0,5 mol
e. la quantité de matière des produits formés en fin de réaction
n°2
n°3
n°4
n°1
avancement x

0
1
2
3
4
5
6
7
8
9
0 4
Avancement x (mol)
Quantité de matière n (mol)
ETUDE D’UN GRAPHE n°2
L’étude graphique d’une réaction chimique a permis de tracer les
courbes suivantes :
1. Déduire de ce graphe
a. les quantités initiales de chaque espèce
b. le réactif limitant
c. l’état du système pour un avancement de 1,5 mol
d. l’état du système lorsque le réactif limitant est
épuisé.
2. De ces deux équations laquelle correspond à la transformation
chimique ayant eu lieu lors de cette étude graphique ? justifier
a. 2H2 + O2 2 H2O
b. 2 H2O 2H2 + O2
n(H2O)
n(O2)
n(H2)

ETUDE D’UN GRAPHE n°3
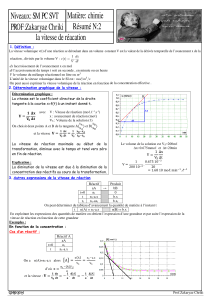
L’étude graphique d’une réaction chimique a permis de tracer les courbes ci-contre.
1. Déduire de l’étude graphique de ce graphe :
a. les quantités initiales de chaque espèces
b. le réactif en excès . Justifier
c. l’état du système pour un avancement de 0,5 mol
d. l’état du système à la fin de
cette transformation.
2. Quelle est l’équation de cette
réaction ? Justifier et ajuster les nombres
stoechiométriques
0
0,5
1
1,5
2
2,5
3
3,5
0 0,1 0,2 0,3 0,4 0,5 0,6 0,7 0,8
Avancement (mol )
Quantité de matière (mol)
n( CO)
n( Fe3O4)
n( CO2)
n( Fe)
1
/
3
100%