Stade II

•Incidence estimée en France # 40 000 cas en 2010
Augmentation lente de l’incidence
Données INVS 2010

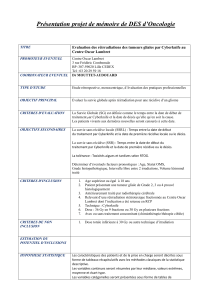
Stade au diagnostic
Période de diagnostic
76-79 80-83 84-87 88-91 92-95 96-99
Fréquence relative
0
10
20
30
40
Stade IV
Stade III
Stade II
Stade I
Répartition par stade
(Registre de Côte d’Or)

CCR stade II, maladie du patient âgé
• 45% des CCR sont diagnostiqués après 75 ans
• Stade au diagnostic
Stade I-II Stade III Stade IV
<75 ans 51,3% 23,9% 24,4%
>75 ans 48,6% 24,3% 26,8%
Faivre-Finn C et al, Gut, 2002
Réseau FRANCIM 2010

Stades TNM 7ème édition (2010)
Stade I : pT1-2 N0 M0
Stade IIA : pT3 N0 M0
Stade IIB : pT4a N0 M0
Stade IIC : pT4b N0 M0
Stade IIIA : pT1-T2 N1a-b M0 et pT1 N2a M0
Stade IIIB : pT3-T4a N1a-bM0, pT2 T3N2aM0, pT1 T2N2bM0
Stade IIIC : pT4a N2a M0; pT3,T4a N2b M0; pT4 N1-N2M0
Stade IVA : tout T, Tout N, M1a
Stade IVB : tout T, tout N, M1b
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
 26
26
 27
27
 28
28
 29
29
 30
30
 31
31
 32
32
 33
33
 34
34
 35
35
 36
36
 37
37
 38
38
 39
39
 40
40
 41
41
 42
42
 43
43
 44
44
1
/
44
100%