Double antiagrégation plaquettaire pour le traitement et la

REVUE MÉDICALE SUISSE
WWW.REVMED.CH
25 mai 2016
1022
Double antiagrégation plaquettaire
pour le traitement et la prévention
secon daire de la maladie coronarienne
Indications, modalités et durées de traitement
Le choix et la durée optimale de la double antiagrégation pla-
quettaire (DAPT) pour le traitement de la maladie coronarienne
constituent un dilemme dans la pratique clinique. La stratégie de
traitement antiplaquettaire est déterminée par le contexte cli-
nique, les comorbidités et la stratégie de prise en charge globale
du patient. Si l’aspirine constitue le pilier de la prévention secon-
daire de la maladie coronarienne, la DAPT est associée à une
réduction significative du risque d’événements ischémiques au
détriment d’une augmentation du risque d’hémorragie majeure.
Une approche individualisée, basée sur l’évaluation des risques
ischémique et hémorragique du patient, est actuellement préco-
nisée. Cet article propose une revue sur l’évidence actuelle dans
le domaine de la DAPT pour le traitement et la prévention secon-
daire de la maladie coronarienne.
Dual antiplatelet therapy for treatment and
secondary prevention of coronary artery disease :
indications, modalities and duration
The choice and optimal duration of dual antiplatelet therapy (DAPT)
for the treatment of coronary artery disease (CAD) represent a chal-
lenging clinical dilemma. Antiplatelet treatment strategies are de-
termined by the clinical setting, patient comorbidities and manage-
ment strategy. While aspirin remains the cornerstone for secondary
prevention of CAD, DAPT significantly reduces recurrent ischemic
adverse events at the expense of an increased risk of major bleeding
complications. A tailored approach based on individual ischemic
and hemorrhagic risk assessment is currently recommended. This
review aims to provide a contemporary overview on the current
body of evidence concerning DAPT for treatment and secondary
prevention of CAD with practical emphasis on current indications,
choice, combination and optimal duration of antiplatelet therapy.
INTRODUCTION
Les patients avec une maladie coronarienne (MC) demeurent
à risque élevé d’événements cardiovasculaires majeurs (MACE)
récurrents sur le long terme, incluant la mortalité cardiovas-
culaire (CV), l’infarctus du myocarde (IM) ou l’accident vas-
culaire cérébral (AVC).1 Les agents antiplaquettaires (AAP)
constituent un pilier important du traitement et de la pré-
vention secondaire de la MC. L’antiagrégation plaquettaire
est associée à une réduction significative des événements
isché miques récurrents pour les patients avec une maladie
coronarienne stable (MCS) ou un syndrome coronarien aigu
(SCA) en comparaison du placebo.2 Si l’intensification de
l’inhibition plaquettaire par une double antiagrégation plaquet-
taire (DAPT) permet une réduc tion significative du risque
d’événements thrombotiques après une intervention coro-
narienne percutanée (PCI) ou un SCA en comparaison de la
monothérapie antiplaquettaire (AP), elle est associée à une
augmentation du risque d’hémorragie majeure potentielle-
ment fatale.3-6 Les stratégies de traitement AP dépendent du
contexte clinique, des comorbidités et de la stratégie de prise
en charge globale du patient. Le choix des indications, des
modalités et de la durée de traitement AP constitue un di-
lemme dans la pratique clinique. Cet article propose une
revue sur l’évidence actuelle concernant la DAPT pour le trai-
tement et la prévention secondaire de la MC.
PRINCIPAUX AGENTS ANTIPLAQUETTAIRES
Les plaquettes sont les acteurs principaux de l’hémostase et
jouent un rôle important dans le développement et la pro-
gression de la maladie athérothrombotique. La progression
incontrôlée des processus pathophysiologiques d’activation
et d’agrégation plaquettaires conduit à la formation d’un throm-
bus intracoronaire résultant en une occlusion, complète ou
partielle, responsable d’une ischémie ou d’un infarctus myo-
cardiques. Les AAP actuellement disponibles interfèrent avec
les différentes étapes des processus d’activation et d’agréga-
tion plaquettaires. Les caractéristiques, mécanismes d’action
et indications des principaux AAP utilisés pour le traitement
et la prévention secondaire de la MC sont résumés dans le ta-
bleau 1. Compte tenu de leurs différents mécanismes d’action,
la combinaison de plusieurs agents permet d’augmenter leur
efficacité et, par conséquent, le bénéfice clinique. L’aspirine et
le clopidogrel ont été évalués dans tout le spectre clinique de la
MC alors que les nouveaux AAP inhibant le récepteur plaquet-
taire P2Y12 (prasugrel, ticagrelor) n’ont été évalués à l’heure
actuelle que dans des études incluant des patients avec un SCA.
DOUBLE ANTIAGRÉGATION PLAQUETTAIRE
Bien que plusieurs combinaisons soient possibles, le terme
de « DAPT » se réfère communément à l’association entre
Drs SOPHIE DEGRAUWE a et JUAN F. IGLESIAS a
Rev Med Suisse 2016 ; 12 : 1022-34
a Service de cardiologie, CHUV, 1011 Lausanne
sophie.degrauwe@chuv.ch | juan-fernando.iglesias@chuv.ch
14_26_39268.indd 1022 19.05.16 10:17

Cardiologie
WWWREVMEDCH
mai
1023
l’aspirine et un inhibiteur du récepteur P2Y12 (clopi dogrel, pra-
sugrel ou ticagrelor). L’intensification de l’inhibition plaquet-
taire par une DAPT réduit de manière significative la survenue
d’événements ischémiques récurrents dans certains sous-
groupes de patients avec une MC, mais elle est associée à une
augmentation du risque de saignement majeur par rapport à
la monothérapie AP. Le choix de l’inhibiteur du récepteur
P2Y12 associé à l’aspirine et de la durée optimale de la DAPT
est déterminé par le contexte clinique au sein du spectre de
présentation de la MC (MCS ou SCA), les comorbidités du
patient et la stratégie de prise en charge (traitement médical
conservateur (PCI), ou revascularisation coronarienne chi-
rurgicale (CABG)).3-6 Une approche individualisée, basée sur
l’évaluation des risques ischémique et hémorragique du pa-
tient, est actuellement préconisée afin de maximiser l’effica-
cité de la thérapie AP et de réduire le risque d’hémorragie.3-6
MALADIE CORONARIENNE STABLE
L’antiagrégation plaquettaire par aspirine constitue la pierre
angulaire du traitement et de la prévention secondaire des pa-
tients avec une MCS, indépendamment de la stratégie de trai-
tement (traitement médical conservateur, PCI ou CABG). Dans
une méta-analyse incluant six études de prévention primaire
(95 000 patients) et seize études de prévention secondaire
Aspirine Clopidogrel Prasugrel Ticagrelor
Molécule / classe chimique Acide acétylsalicylique Thiénopyridine Thiénopyridine Cyclopentyl-triazolo pyrimidine
Voie d’administration Orale Orale Orale Orale
Mécanisme d’action Inhibition de la cyclo-
oxygénase-1
Inhibition du récepteur P2Y12 Inhibition du récepteur P2Y12 Inhibition du récepteur P2Y12
Dosage 150-300 mg PO ou 80-150 mg
IV, puis 75-150 mg / jour PO
300-600 mg PO,
puis 75 mg / jour
60 mg PO, puis 10 mg / jour 180 mg PO, puis 90 mg
2 x / jour
Action antiplaquettaire Irréversible Irréversible Irréversible Réversible
Activation Promédicament, hydrolyse par
une estérase
Promédicament, métabolisme
hépatique variable
Promédicament, métabolisme
hépatique prédictible
Médicament actif avec
métabolite actif additionnel
Entrée en action après la
dose de charge
30-40 minutes 2-6 heures 30 minutes 30 minutes
Durée de l’effet 5 jours 3-10 jours 7-10 jours 3-5 jours
Arrêt avant une chirurgie Pas d’interruption si possible,
5 jours si opération à haut
risque hémorragique
5 jours 7 jours 5 jours
Demi-vie plasmatique de la
substance active
2-3 heures 30-60 minutes 30-60 minutes 6-12 heures
Inhibition de la recapture de
l’adénosine
Non Non Non Oui
Indications • Maladie coronarienne stable
• Syndrome coronarien aigu
• Maladie coronarienne stable
• Syndrome coronarien aigu
• Syndrome coronarien aigu
traité par PCI
• Syndrome coronarien aigu
• Maladie coronarienne stable
après un infarctus du
myocarde
Contre-indications • Saignement actif
• Hypersensibilité à l’aspirine
• Insuffisance hépatique
sévère
• Saignement actif
• Insuffisance hépatique
sévère
• Saignement actif
• Antécédent d’AIT ou AVC
• Insuffisance hépatique
sévère (Child-Pugh C)
• Saignement actif
• Antécédent d’hémorragie
intracrânienne
• Insuffisance hépatique
modérée à sévère
• Coadministration
d’inhibiteurs puissants du
cytochrome CYP3A4
Précautions d’emploi • Insuffisance hépatique
sévère
• Insuffisance rénale sévère
• Insuffisance cardiaque
décompensée sévère
• Interaction avec les anti-
inflammatoires non stéroïdiens
• Combinaison avec le métho-
trexate
• Purpura thrombotique
thrombocytopénique
• AVC ischémique récent
(< 7 jours)
• Métaboliseurs lents du
cytochrome CYP2C19
• Insuffisance rénale
• Intolérance au galactose
• Administration concomitante
d’oméprazole ou d’ésomépra-
zole
• Age ≥ 75 ans et / ou poids
< 60 kg : 5 mg / jour
• Purpura thrombotique
thrombocytopénique
• Intolérance au galactose
• Bradycardies
• Asthme et / ou BPCO
• Insuffisance rénale modérée
à sévère
• Administration concomitante
d’antagonistes du récepteur
de l’angiotensine
• Hyperuricémie ou arthrite
goutteuse
• Néphropathie urique
• Coadministration de
simvastatine ou lovastatine
> 40 mg / jour
• Coadministration de digoxine
Tableau 1 Principaux agents antiplaquettaires pour le traitement et la prévention
secondaire de la maladie coronarienne
AIT : accident ischémique transitoire ; AVC : accident vasculaire cérébral ; BPCO : bronchopneumopathie chronique obstructive ; PCI : intervention coronarienne percutanée.
(Adapté de réf.3-6).
14_26_39268.indd 1023 19.05.16 10:17

REVUE MÉDICALE SUISSE
WWW.REVMED.CH
25 mai 2016
1024
(17 000 patients), une antiagrégation plaquettaire par aspirine
à faible dose (75-150 mg / jour) réduit l’incidence des MACE de
33 % pour les patients avec une MCS et de 53 % après une PCI.2
Pour les patients avec un antécédent d’IM, l’aspirine réduit
l’incidence de la mortalité CV, de l’IM et de l’AVC, au détri-
ment d’une augmentation du risque de saignement majeur.2
En prévention secondaire, l’aspirine est associée à une réduc-
tion du risque absolu annuel de mortalité de 34 % et d’IM de
66 %.2 Sur la base des données disponibles, la dose optimale
d’aspirine con fé rant une protection maximale contre les évé-
nements ischémiques et minimisant le risque hémorragique
(en particulier gastro-intestinal) se situe entre 75 et 150 mg /
jour.3,6
Traitement médical conservateur
L’étude CAPRIE a évalué le bénéfice d’une monothérapie
par clopidogrel (75 mg / jour) par rapport à l’aspirine (325 mg /
jour) dans une population de 19 185 patients avec une maladie
CV (AVC ou IM récents, maladie vasculaire périphérique).7
L’étude montre que la monothérapie par clopidogrel au long
cours (suivi médian : deux ans) est associée à une réduction
significative du risque annuel de MACE par rapport à l’aspi-
rine, sans augmentation du risque d’hémorragie intracrânienne
ou gastro-intestinale. Au contraire de leur supériorité démon-
trée pour les patients avec un SCA, le bénéfice clinique des
nouveaux inhibiteurs du récepteur P2Y12 (prasugrel, ticagre-
lor) n’a pas été évalué dans le cadre d’études randomisées
incluant des patients avec une MCS et sans antécédent récent
d’IM. Aucune évidence ne permet donc de soutenir actuelle-
ment le bénéfice d’une inhibition plaquettaire avec le prasu-
grel ou le ticagrelor pour les patients avec une MCS, traités de
manière conservative. En l’absence de contre-indications,
les recommandations pré conisent une monothérapie par
aspirine à faible dose au long cours pour tous les patients avec
une MCS (classe de recommandation I),3,6 le clopidogrel (75
mg / jour) pouvant être considéré comme une alternative en cas
d’intolérance à l’aspirine (classe I).3 En cas d’hypersensibilité /
allergie à l’aspirine, l’alternative d’un traitement de désensibi-
lisation rapide à l’aspirine peut également être envisagée.
L’étude CHARISMA a évalué le bénéfice d’une DAPT par aspi-
rine et clopidogrel par rapport à une monothérapie par aspi-
rine (75-162 mg / jour) pour la prévention secondaire chez
15 603 patients avec une maladie CV ou de multiples facteurs
de risque CV.8 L’étude ne montre pas de différence significa-
tive entre les deux thérapies sur l’incidence des MACE dans la
population totale après un suivi médian de 28 mois. Cepen-
dant, une analyse secondaire du sous-groupe de 9478 patients
avec un antécédent d’IM, d’AVC ischémique ou de maladie
vasculaire périphérique suggère un bénéfice de la DAPT au
long cours, avec une réduction significative de 17 % des MACE
et de 14 % des hospitalisations pour une ischémie myocardique,
sans augmentation de l’incidence des saignements sévères
par rapport à la monothérapie par aspirine, mais au détriment
d’une augmentation significative de 60 % du risque de saigne-
ments modérés.9
Le bénéfice d’une combinaison entre l’aspirine et le vorapaxar,
un antagoniste du récepteur plaquettaire PAR-1 à la throm-
bine, a été évalué dans l’étude TRA 2P-TIMI 50, qui a rando-
misé 26 449 patients avec un antécédent d’IM, d’AVC ou de
maladie vasculaire périphérique (94 % des patients sous aspi-
rine) entre le vorapaxar (2,5 mg / jour) et un placebo. Si TRA
2P-TIMI 50 montre une réduction significative de 13 % des
MACE à trois ans en faveur des patients traités par le vora-
paxar, l’étude a dû être interrompue prématurément en rai-
son d’une augmentation significative du risque d’hémorragies
modérées / sévères et intracrâniennes par rapport au place-
bo.10 De manière similaire, l’analyse du sous-groupe de 17 779
patients avec un antécédent d’IM montre que le vorapaxar en
prévention secondaire est associé à une réduction significative
de 20 % des événements ischémiques au prix d’une augmenta-
tion des hémorragies modérées / sévères et intracrâniennes par
rapport au placebo.11
Une combinaison d’AAP ne peut actuellement pas être re-
commandée de routine pour les patients avec une MCS et sans
antécédent de SCA, de PCI ou de CABG dans les douze mois
précédents (classe III).6 Les données de l’étude CHARISMA
suggèrent toutefois le bénéfice potentiel d’une DAPT combi-
nant aspirine et clopidogrel par rapport à une monothérapie
par aspirine, dans un sous-groupe de patients avec une MCS
stable et à haut risque d’événements CV 9 (figure 1).
Revascularisation coronarienne percutanée
L’intensification de l’inhibition plaquettaire après la mise en
place d’un stent endocoronaire permet de réduire le risque
d’événements ischémiques et de la thrombose de stent (TS).
La durée de la DAPT est déterminée par le type de stent et le
risque hémorragique individuel du patient.3,4,6 Si une durée
minimale d’un mois de DAPT est actuellement recommandée
après la mise en place d’un stent non actif (BMS),3,4,6 la durée
optimale de la DAPT après un stent actif (DES) demeure
controversée. La nouvelle génération de DES, caractérisée
par une épaisseur des mailles plus fine, un composant poly-
mérique biocompatible ou biodégradable et une concentra-
tion réduite en agent antiprolifératif favorisant une endothé-
lialisation précoce, permet actuellement de réduire le risque
de TS et de limiter l’importance d’une inhibition plaquettaire
prolongée après une PCI. Plusieurs études randomisées et
méta-analyses, parues au cours des dernières années, ont remis
en question le dogme de la DAPT minimale de douze mois
après un DES.12-27 De manière générale, la tendance actuelle
s’oriente vers un raccourcissement de la durée de DAPT, mais
plusieurs études ont également suggéré le bénéfice potentiel
d’une prolongation de la durée de DAPT au-delà de douze
mois dans un sous-groupe de patients à haut risque CV.3-6
Cinq études randomisées, évaluant le bénéfice clinique d’une
courte durée (3-6 mois) de DAPT après un DES par rapport à
une durée standard de douze mois dans une population à
faible risque d’événements CV,12-16 ont montré la non-infério-
rité d’un raccourcissement de la DAPT sur l’incidence des
événements ischémiques incluant la TS, et une diminution
significative de l’incidence des complications hémorragiques
majeures.12-16 Au contraire, six autres études randomisées ont
comparé une durée prolongée (18-48 mois) de DAPT après
un DES par rapport à une durée standard (6-12 mois) afin
d’évaluer le bénéfice potentiel d’une prolongation de la DAPT
pour la prévention des événements CV associés à la progres-
sion de la maladie athérosclérotique et l’incidence de la TS
(très) tardive.17-23 Ces études montrent que la prolongation de
14_26_39268.indd 1024 19.05.16 10:17

Cardiologie
WWWREVMEDCH
mai
1025
la durée de DAPT est associée à une réduction de l’incidence
de l’IM et de la TS, au détriment d’une augmentation signifi-
cative du risque hémorragique.
L’étude DAPT a comparé l’efficacité et la sécurité d’une DAPT
prolongée (30 mois) par rapport à une durée standard (douze
mois) dans une population de patients à faible risque throm-
botique et hémorragique. Après une DAPT de douze mois par
aspirine et une thiénopyridine (clopidogrel ou prasugrel) après
un DES, 9961 patients ont été randomisés entre une poursuite
de la DAPT pendant dix-huit mois ou une monothérapie par
aspirine seule. Les résultats de l’étude montrent que la durée
de DAPT de 30 mois est associée à une réduction significative
des MACE, de la TS et de l’IM, par rapport à la durée de douze
mois, au détriment d’une augmentation significative des sai-
gnements modérés ou sévères.17 Le suivi des patients durant
les trois mois suivant l’arrêt du traitement randomisé suggère
un effet rebond après l’arrêt de la DAPT, caractérisé par une
augmentation du risque d’IM et de la TS qui semble plus élevé
lorsque la DAPT est interrompue à douze mois plutôt qu’à 30
mois. Les données de l’étude doivent toutefois être contreba-
lancées par l’augmentation significative du risque de mortalité
globale en cas de prolongation de la DAPT, malgré un risque
de mortalité CV similaire. Une analyse post-hoc des causes de
décès démontre que l’excès de mortalité non CV dans le groupe
des patients avec une DAPT prolongée n’est pas secondaire à
une augmentation des hémorragies fatales mais de la morta-
lité résultant de cancers, essentiellement préexistants au mo-
ment de la randomisation.24 Cependant, la prolongation de la
DAPT n’est pas associée à une augmentation de l’incidence de
nouveaux cancers diagnostiqués au cours de l’étude.
Les résultats contradictoires des nombreuses études rando-
misées évaluant la durée optimale de DAPT après un DES ont
récemment été combinés dans quatre méta-analyses, incluant
pour certaines onze études randomisées et plus de 33 000
patients (environ 50 % des patients avec une MCS).25-28 Les
données de ces méta-analyses montrent qu’en comparaison
d’une durée de DAPT de douze mois après un DES :
• le raccourcissement de la durée de DAPT (3-6 mois) est as-
socié à une réduction significative d’environ 40 % du risque
d’hémorragie majeure, alors qu’aucune différence signifi-
cative n’est constatée sur les événements CV ischémiques
et la TS.
• La prolongation de la durée de DAPT (> 12-48 mois) est as-
sociée à une réduction significative d’environ 50 % du risque
d’IM et 70 % du risque de TS, au détriment d’une augmen-
tation significative du risque d’hémorragie majeure et de la
mortalité globale, alors qu’aucune différence n’est consta-
tée sur la mortalité CV.
Par conséquent, la décision d’une prolongation de la durée de
DAPT (18-48 mois) nécessite une évaluation individuelle de la
balance entre le bénéfice ischémique (réduction de l’incidence
de l’IM et de la TS) et le risque hémorragique (augmentation
du risque de saignement majeur et de mortalité non CV).28
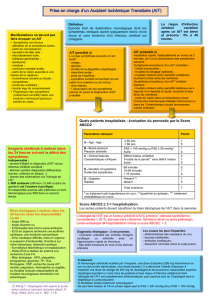
Un score clinique a récemment été développé à partir des
données de l’étude DAPT (score DAPT) pour faciliter l’iden-
fig 1 Recommandations sur le choix et la durée de la double antiagrégation plaquettaire
pour les patients avec une maladie coronarienne stable
ATCD : antécédent ; BMS : stent non actif ; CABG : revascularisation coronarienne chirurgicale ; CV : cardiovasculaire ; DAPT : double antiagrégation plaquettaire ; DES : stent actif ;
IM : infarctus du myocarde ; PCI : intervention coronarienne percutanée.
* ≥1 critère de haut risque : âge ≥ 65 ans, diabète, second infarctus du myocarde, atteinte coronarienne multitronculaire ou insuffisance rénale chronique.
Maladie coronarienne stable
0 mois
1 mois
3 mois
6 mois
12 mois
Traitement médical CABG PCI
BMS
Pas ATCD IM,
PCI ou CABG
Classe III :
pas de
bénéfice
Classe I :
min. 1 mois
(clopidogrel)
Pas de risque élevé d’hémorragie, pas
d’hémorragie significative sous DAPT
Pas de risque élevé d’hémorragie, pas
d’hémorragie significative sous DAPT
Risque élevé
d’hémorragie,
ou
hémorragie
significative
Classe I :
min. 6 mois
(clopidogrel)
Classe IIb :
poursuite
DAPT peut être
considérée
(ticagrelor)
Classe IIb :
durée 12 mois,
peut être
considérée
(clopidogrel) Classe IIb : > 1 mois, peut être considéré
Classe IIb : > 6 mois, peut être considéré
Classe IIb :
arrêt après
3-6 mois, peut
être considéré
ATCD IM
récent et haut
risque CV* DES
(Adaptée de réf.3-6).
14_26_39268.indd 1025 19.05.16 10:17

REVUE MÉDICALE SUISSE
WWW.REVMED.CH
25 mai 2016
1026
tification des patients susceptibles de bénéficier d’une pro-
longation de la durée de DAPT sur la base d’une évaluation
individuelle du risque ischémique et hémorragique.29
Les dernières recommandations pour les patients avec une
MCS, traités par PCI, préconisent une DAPT associant l’aspi-
rine (75-150 mg / jour) (classe I) et le clopidogrel (75 mg / jour)
(classe I) pour une durée minimale d’un mois après un BMS
(classe I) et de six mois après un DES (classe I).4,6 En l’absence
de données, l’administration de prasugrel ou de ticagrelor ne
peut actuellement pas être recommandée pour les patients à
bas risque lors d’une PCI élective (classe III),3 mais elle peut
être envisagée comme une alternative pour les patients avec
un antécédent de TS sous une DAPT avec le clopidogrel
(classe IIa) et dans certaines situations à haut risque de TS
(PCI du tronc commun, diabète) (classe IIb).3 Au-delà de la
période de DAPT, une monothérapie par aspirine à faible dose
(75-150 mg / jour) est actuellement recommandée à vie (classe
I).3,4 En cas d’intolérance à l’aspirine, une monothérapie par
clopidogrel peut être envisagée comme alternative (classe I).3
Une prolongation de la DAPT peut être considérée pour les
patients à haut risque ischémique et à faible risque hémorra-
gique, qui ont toléré la période initiale de DAPT sans compli-
cation hémorragique (classe IIb) 4,6 (figure 1).
Revascularisation coronarienne chirurgicale
Une antiagrégation plaquettaire par aspirine est associée à
une amélioration de la perméabilité des pontages veineux (en
particulier durant la première année après l’intervention) et
à une réduction de l’incidence des MACE après un CABG.6
Plusieurs études ont évalué le bénéfice d’une DAPT par aspi-
rine et clopidogrel par rapport à une monothérapie (aspirine
ou clopidogrel) sur la perméabilité des pontages après un
CABG, et ont démontré des résultats contradictoires.6 Dans la
plus grande méta-analyse, incluant cinq études randomisées
et six études observationnelles (25 728 patients),30 la DAPT est
associée à une réduction significative de 41 % de l’incidence des
occlusions des pontages veineux et de la mortalité à 30 jours
par rapport à la monothérapie, au détriment d’une augmenta-
tion des saignements majeurs. Les résultats suggèrent un
bénéfice plus important de la DAPT dans le sous-groupe des
patients après un CABG à cœur battant, avec une réduction
de 68 % du risque d’IM et de 55 % du risque d’occlusion des
pontages veineux par rapport aux patients après un CABG
sous circulation extracorporelle. Dans une autre méta-ana-
lyse de cinq études randomisées incluant 958 patients,31 la
DAPT par aspirine et clopidogrel est également associée à une
diminution significative de l’incidence des occlusions de pon-
tages veineux à une année, au détriment d’une augmentation
du risque de saignement majeur par rapport à la monothéra-
pie (aspirine ou clopidogrel). Cependant, aucun bénéfice cli-
nique n’est observé sur la perméabilité des pontages artériels.
Le bénéfice clinique d’une DAPT (aspirine et clopidogrel) sur
la perméabilité des pontages 32 et le pronostic clinique 33 pour
les patients avec un CABG à cœur battant a récemment été
confirmé dans des études observationnelles monocentriques 33
et une étude randomisée.32
Les recommandations préconisent une monothérapie par
aspirine à faible dose (75-150 mg / jour) à vie pour les patients
avec une MCS (classe I) 3,4 et de considérer une DAPT associant
aspi rine et clopidogrel (débutée précocement après l’inter-
vention) pendant une durée de douze mois pour les patients
avec une MCS après un CABG pour améliorer la perméabilité
des pontages veineux (classe IIb).6 Une DAPT pour les pa-
tients avec une MCS et sans antécédent de SCA, de PCI ou de
CABG dans les douze mois précédents n’est pas recomman-
dée (classe III).6 Pour les patients traités par CABG après une
PCI élective récente, les recommandations proposent de re-
prendre le traitement par inhibiteur du récepteur P2Y12 après
le CABG de manière à compléter la durée prévue de DAPT
(classe I) 6 (figure 1).
SYNDROME CORONARIEN AIGU
L’antiagrégation plaquettaire par aspirine constitue le pilier
du traitement pharmacologique des patients avec un SCA, in-
dépendamment du contexte clinique (angor instable, IM sans
(NSTEMI) ou avec (STEMI) élévation du segment ST) et de
la stratégie de prise en charge (traitement médical conserva-
teur, PCI ou CABG).5,6 Plusieurs études randomisées évaluant
l’administration de l’aspirine par rapport à un placebo ont dé-
montré une réduction > 50 % du risque absolu de mortalité CV
et d’IM dans le groupe des patients avec un SCA traités par as-
pirine.7 Dans l’étude CURRENT-OASIS 7, aucune différence
significative n’est constatée entre une haute dose (300-325 mg /
jour) et une faible dose (75-100 mg / jour) d’aspirine en termes
de MACE à 30 jours, dans une population de 25 086 patients
avec un SCA, indépendamment de la stratégie de traitement
(traitement conservateur ou PCI).34,35 Cependant, la faible dose
d’aspirine est associée à une diminution significative du risque
de saignement gastro-intestinal majeur, suggérant une balance
entre le risque ischémique et hémorragique en faveur d’une
faible dose quotidienne d’aspirine pour les patients avec un
SCA.34 Par ailleurs, des données récentes suggèrent une inter-
action significative entre la dose d’aspirine et l’efficacité du
ticagrelor, avec une réduction moins importante des MACE
pour les patients traités avec des hautes doses (≥ 300 mg / jour)
par rapport à des faibles doses (≤ 100 mg / jour) d’aspirine.36
Traitement médical conservateur
L’étude CURE a évalué le bénéfice clinique d’une DAPT par
aspirine et clopidogrel pendant 3-12 mois par rapport à une
monothérapie par aspirine, dans une population de 12 562
patients avec un NSTEMI (64 % traités de manière conser-
vative). L’étude montre que la DAPT est associée à une ré-
duction significative de 20 % de l’incidence des MACE et une
augmentation signi ficative du risque d’hémorragie majeure,
mais pas d’hémor ragie fatale ou d’AVC hémorragique, par
rapport à la monothérapie.37
L’étude randomisée TRILOGY ACS a comparé l’efficacité d’une
DAPT associant l’aspirine et le prasugrel par rapport au clopi-
dogrel, dans un collectif de 7243 patients avec un SCA traités
de manière conservative.38 L’étude ne montre pas de différence
significative entre une DAPT avec le prasugrel ou le clopido-
grel sur l’incidence des MACE et des hémorragies majeures. A
l’inverse, l’analyse du sous-groupe de 5216 patients (28 %) de
l’étude PLATO traités de manière non invasive 39 montre que la
DAPT avec le ticagrelor est associée à une réduction significa-
tive de 15 % de l’incidence des MACE et de 20 % de la mortalité
14_26_39268.indd 1026 19.05.16 10:17
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
1
/
12
100%