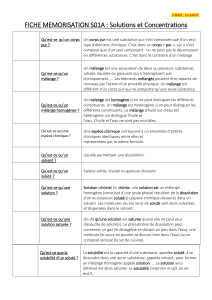
molécules chimique solvant plusieurs

2016-11-052016-11-05 1
Thermodynamique
statistique biomoléculaire
GBM2620
Automne 2016
Chapitre 16 de
Molecular Driving Forces
Michael D. Buschmann et Marc Lavertu

2016-11-052016-11-05 2
Chapitre 16 : Solvatation et transfert
de molécules entre phases
Dans ce chapitre, on s’intéresse à la solvatation et à la
partition de particules d’une espèce chimique dans un
milieu composé d’une autre espèce chimique.
Par exemple, certaines toxines se dissolvent dans un milieu tel que
l’eau et s’accumulent dans un autre, tel que le gras de poisson.
On va aussi déterminer comment des molécules modifient
l’équilibre de phase pour des molécules d’une autre espèce
chimique.
L’ajout de sel fait fondre la glace et fait augmenter le point d’ébullition
de l’eau.
Différences de potentiel chimique est la force motrice :
1) Les particules ont tendance à se déplacer vers des régions où leur
concentration est plus faible afin d’augmenter l’entropie (s).
2) Les particules ont tendance à se déplacer vers des régions pour
lesquelles elles ont une plus grande affinité chimique (enthalpie h).
Michael D. Buschmann et Marc Lavertu

2016-11-052016-11-05 3
La solvatation est le transfert de
molécules entre un gaz et un liquide
On considère un mélange liquide de deux composants A et B,
B (l’eau) est volatil, A (sel) ne l’est pas:
B peut se déplacer librement entre la phase gazeuse et le liquide.
Le degré de liberté du système est le nombre de molécules de type B
dans le gaz ou le nombre de molécules dans le liquide .
Pour un sel (A) dissout dans l’eau (B), l’eau est plus volatil.
On peut aussi avoir un gaz (B volatil) dissout dan l’eau (A moins volatil)
La condition d’équilibre à constantes est
D’après les chapitres 11 (Eq. 11.50) et 15 (Eq.15.17)
Michael D. Buschmann et Marc Lavertu
( ) ( )
BB
gl
µµ
=
et Tp
( ) ( )
( )
( )
2
0,int
ln ln 2 1
µµ
χ
=
= ++ −
BB
B B B BB AB B
gl
kT p p kT x zw kT x
( )
B
Ng
( )
B
Nl

2016-11-052016-11-05 4
Modèle du réseau pour solvatation et
diminution de la pression de vapeur
On peut exprimer dans une forme plus compacte:
où (Eq. 14.9) est la tension de vapeur de B
au-dessus d’une solution pure de B ( )
Dans le cas d’une solution idéale ( ),
est une fonction linéaire de , c’est la
loi de Raoult.
B a plus tendance à s’échapper lorsque
et moins lorsque .
Lorsque , la solution se comporte comme
si elle était idéale, peu importe la valeur de .
Michael D. Buschmann et Marc Lavertu
B
p
( )
()
( )
()
22
ln 21 21
0,int
B BB AB B BB AB B
x zw kT x zw kT x
BB
B
pe xe
p
χχ
+ +− +−
⇒= =
B
p
()
()
2
1
0AB B
x
B BB
p pxe
χ
−
=
( )
2
00
,int
BB
zw kT
BB
p pe=
0
AB
χ
>
0
AB
χ
=
B
x
(~idéal)
0
AB
χ
<
1
B
x→
AB
χ
1
B
x→
1=
B
x

2016-11-052016-11-05 5
Modèle du réseau pour solvatation et
diminution de la pression de vapeur
L’ajout d’une faible quantité de sel à de l’eau pure diminue sa
pression de vapeur. Pourquoi si l’énergie d’interaction ne joue
aucun rôle ( ) ?
L’ajout de A (sel) diminue la tendance à s’échapper de B (eau). Comme
pour l’idéalité dans un gaz parfait, l’idéalité en solution ( )
décrit des processus dont la force motrice est l’entropie de translation
et non pas l’énergie d’interaction.
Pour un liquide pur de B,
Quand des molécules A sont ajoutées,
Michael D. Buschmann et Marc Lavertu
0
1 ln 0, 1 2
B BB B
W S k W x zw
µµ
=⇒= = =⇒= =
0 ou 1
AB B
x
χ
= →
1W=
1W>
( )
( )
2
0
00
1 0, ln 1
ln si 0 ou 1
B B B AB B
BB BBB AB B
W S kT x kT x
kT x x
µµ χ
µµ µχµ
>⇒ > = + +
= →⇒ <
−
= +
** car les B ont principalement B
comme voisin proche, comme dans une phase pure de B.
ne dépend pas de lorsque 1
B AB B
x
µχ
→
0 ou 1
AB B
x
χ
= →
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
 26
26
 27
27
 28
28
 29
29
 30
30
 31
31
 32
32
 33
33
 34
34
1
/
34
100%