Réa1 Com Ana

La création de nouvelles espèces chimiques résulte souvent d’un changement de groupe caractéristique
pour passer d’une famille chimique à une autre. L’importance des alcools en chimie organique vient de leur très
grande réactivité qui en fait des intermédiaires réactionnels dans la synthèse d’autres produits finaux.
La plupart des réactions en chimie organique peut être classée en 3 catégories (et leurs combinaisons) :
Une réaction de substitution est une réaction organique au cours de laquelle un atome ou groupe d'atomes (en
général le ou l’un des groupes fonctionnels) d'un composé chimique est remplacé par un autre.
E1. Dans trois tubes à essais secs et propres, verser environ 1 mL de réactif de Lucas (solution d’acide chlorhydrique
(H3O+
(aq) + Cl-
(aq)) accompagnée d’un catalyseur).
Dans chaque tube, ajouter 5 gouttes d’un des alcools suivants : butan-1-ol, butan-2-ol et 2-méthylpropan-2-ol.
Boucher les tubes, agiter vigoureusement pendant trois minutes puis placer au bain marie à 40°C si rien ne se
passe.
Q2. Laisser reposer puis noter vos observations.
……………………………………………………………………………………………………………………………………………………………………………………..
……………………………………………………………………………………………………………………………………………………………………………………..
……………………………………………………………………………………………………………………………………………………………………………………..
……………………………………………………………………………………………………………………………………………………………………………………
Q3. Donner la formule topologique des trois alcools employés. Quelle est la classe de chacun d’eux ? Justifier.
Q4. Sachant que cette réaction consiste au remplacement du groupe fonctionnel hydroxyle par un groupe
fonctionnel chloro, écrire les équations des réactions de substitution ayant lieu dans chaque tube.
……………………………………………………………………………………………………………………………………………………………………………………..
……………………………………………………………………………………………………………………………………………………………………………………..
……………………………………………………………………………………………………………………………………………………………………………………..
Q5. Compléter la phrase suivante :
« Le test au réactif de Lucas permet de préciser la ………………….. d'un ………………….. donné. En effet, pour un alcool
………………….. on n’observe aucune réaction ; pour un alcool ………………….., un ………………….. apparaît après plusieurs
minutes (il peut être nécessaire de tiédir le milieu réactionnel) ; enfin pour un alcool ………………….., le trouble
apparaît …………………… »
Réa1
Com
Ana

Applications :
L'éthanenitrile est aussi appelé acétonitrile dans l'industrie. On peut le préparer par
réaction de substitution des ions chlorure du monochlorométhane par les ions cyanure CN-. L'éthanenitrile
est utilisé comme solvant industriel sélectif dans l'extraction des cires et des graisses.
Q6. Ecrire l’équation de la transformation aboutissant à la formation d’éthanenitrile.
La méthionine est le précurseur de la S-adénosylméthionine ou SAM, un
métabolite essentiel des réactions de transfert de méthyle dans la cellule. La SAM est formé par substitution
des triphosphates de l’ATP par la méthionine :
ATP méthionine SAM ion triphosphate
Une réaction d'addition est une réaction organique au cours de laquelle au moins deux molécules se combinent pour
en former une autre, plus grande. Les réactions d'addition sont conditionnées par la possession par les composés
chimiques concernés de liaisons multiples, les éventuelles liaisons triples devenant des liaisons doubles ou simples, les
liaisons doubles devenant des liaisons simples.
La réaction d’un alcène avec le dibrome a pour équation : CnH2n + Br2 CnH2nBr2
Chacun des atomes de brome se liant à l’un des deux atomes de carbone de la double liaison.
E7. Dans deux tubes à essais contenant environ 1 mL de solution aqueuse de dibrome, introduire deux gouttes de
cyclohexène et de cyclohexane. Agiter.
Q8. Noter vos observations.
……………………………………………………………………………………………………………………………………………………………………………………..
……………………………………………………………………………………………………………………………………………………………………………………..
Q9. En utilisant les formules topologiques, écrire l’équation de la réaction se produisant.
Q10. Expliquez quel test caractéristique utilise comme réactif l’eau de dibrome.
……………………………………………………………………………………………………………………………………………………………………………………..
……………………………………………………………………………………………………………………………………………………………………………………..
CH3C N
+
+
Ana
Val
Com
Ana
Réa 1

Applications :
L’huile de vaseline est un mélange d’alcanes à chaînes carbonées assez longues (entre 8 et 19 atomes de
carbone).
E11. Dans un tube à essais ajouter environ 1mL d’huile de vaseline. Introduire de la paille de fer dans la vaseline.
Adapter un tube à dégagement et plonger son extrémité dans un tube à essais (T1) contenant environ 1mL d’eau
de dibrome (diluée 5 fois). Préparer également un témoin (T2).
Chauffer vivement la vaseline pendant quelques minutes.
Q12. Noter vos observations.
……………………………………………………………………………………………………………………………………………………………………………………..
……………………………………………………………………………………………………………………………………………………………………………………..
Q13. Que peut-on déduire de l’observation précédente ?
……………………………………………………………………………………………………………………………………………………………………………………..
……………………………………………………………………………………………………………………………………………………………………………………..
L’une des réactions se produisant a pour équation : C18H38 C16H34 + C2H4
Q14. S’agit-il d’une réaction de craquage catalytique, de reformage catalytique ou de reformage ?
……………………………………………………………………………………………………………………………………………………………………………………..
……………………………………………………………………………………………………………………………………………………………………………………..
Q15. Ecrire l’équation de la réaction à l’origine du changement de couleur observé.
……………………………………………………………………………………………………………………………………………………………………………………..
……………………………………………………………………………………………………………………………………………………………………………………..
Les triglycérides (également appelés triacylglycérols ou triacylglycérides ou TAG) sont des triesters du
glycérol et d’acides carboxyliques à longue chaîne carbonée (appelés acides gras). Ils constituent le
composant principal des huiles végétales et des graisses animales.
Les triglycérides peuvent être saturés, monoinsaturés ou polyinsaturés
selon la présence ou l’absence d’une ou plusieurs double liaisons dans
la chaine d’acide gras.
L'indice d'iode d'un lipide est la masse de diiode (I2) (exprimée en
gramme) capable de se fixer par réaction d’addition sur les
insaturations (doubles liaisons le plus souvent) des chaines d’acides gras pour 100 g de matière grasse.
Le réactif de Wijs : I-Cl permet de déterminer par expérimentation le nombre de doubles liaisons que
possède la chaîne carbonée d’un acide gras. Il se compose d’iodure de chlore I-Cl qui s’additionne sur une
double liaison
Q16. Ecrire l’équation de cette réaction d’addition en plaçant 4 groupes alkyl (R1, R2, R3 et R4) sur un alcène.
……………………………………………………………………………………………………………………………………………………………………………………..
……………………………………………………………………………………………………………………………………………………………………………………..
……………………………………………………………………………………………………………………………………………………………………………………..
Com
Réa 1
Val
Val
Ana
Ana

Une réaction d’élimination est une réaction organique qui transforme un alcane substitué (halogénoalcanes,
alcools...) en dérivé éthylénique (espèce chimique contenant une ou plusieurs insaturations).
Q17. Proposer un protocole expérimental permettant de montrer qu’une réaction d’élimination a lieu lorsque de
l’éthanol est chauffé en présence d’un catalyseur solide : l’alumine.
……………………………………………………………………………………………………………………………………………………………………………………..
……………………………………………………………………………………………………………………………………………………………………………………..
……………………………………………………………………………………………………………………………………………………………………………………..
Q18. La manipulation est réalisée par le professeur. Faire un schéma de la manipulation :
Q19. Que peut-on déduire de la manipulation réalisée ?
……………………………………………………………………………………………………………………………………………………………………………………..
……………………………………………………………………………………………………………………………………………………………………………………..
……………………………………………………………………………………………………………………………………………………………………………………..
……………………………………………………………………………………………………………………………………………………………………………………..
Q20. En utilisant les formules semi-développées, écrire l’équation de la réaction se produisant.
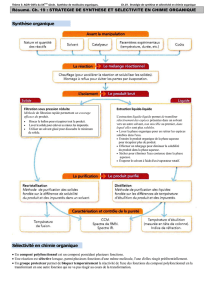
En chimie organique, de nombreux composés peuvent être obtenus à partir de réactions d’élimination ou de
substitution des alcools.
Q21. Compléter le schéma suivant précisant certaines de ces réactions :
Q22. Ces réactions d’addition, substitution et d’élimination sont-elles des
réactions de changement de chaine ou de changement de groupe
caractéristique ?
……………………………………………………………………………………………………………………
………………………………………………………………..………………………………………………….
……………………………………………………………………………………………………………………
ALCOOLS
Groupe fonctionnel :
_ _ _ _ _ _ _ _ _ _ _
DERIVES HALOGENES
Groupe fonctionnel :
_ _ _ _ _ _ _ _ _ _ _ _
_ _ _ _ _ _ _ _ _ _ _ _
_
Présence d’une
liaison double :
Décoloration
Composé formé :
_ _ _ _ _ _ _ _ _ _ _ _
R-X (X = Cl,
Br, I)
Al2O3
_ _ _
Réaction
_ _ _ _ _ _ _
Réaction
_ _ _ _ _ _ _
Réaction
_ _ _ _ _ _ _
Ana
Com
Val
Ana
Val
App

Substances
chimiques
Phrases danger et prudence et
pictogramme
Recyclage
Acide chlorhydrique
(H3O+
(aq) ; Cl-
(aq))
H314 : provoque de graves brûlures de la peau
et des lésions oculaires
H335 : Peut irriter les voies respiratoires
/
Butan-1-ol
H226 : liquide et vapeurs inflammables
H302 : : nocif par ingestion et inhalation
H315 : provoque une irritation cutanée
H318 : Provoque des lésions oculaires graves
H335 : Peut irriter les voies respiratoires
H336 : peut provoquer somnolence ou vertiges
Solvant organique
Butan-2-ol
H226 : liquide et vapeurs inflammables
H319 : provoque une sévère irritation des yeux
H335 : Peut irriter les voies respiratoires
H336 : peut provoquer somnolence ou vertiges
Solvant organique
2-méthylpropan-2-ol
H225 : liquide et vapeurs inflammables
H332 : nocif par inhalation
Solvant organique
solution aqueuse de
dibrome
H314 : provoque de graves brûlures de la peau et
des lésions oculaires
H330 : Mortel par inhalation
H400 : Très toxique pour les organismes aquatiques
Flacon prévu à cet effet afin
de neutraliser le dibrome
avant de le disperser
Cyclohexane
C6H6
H225 : liquide et vapeurs inflammables
H304 : peut être mortel en cas d'ingestion et de
pénétration dans les voies respiratoires
H315 : provoque une irritation cutanée
H336 : peut provoquer somnolence ou vertiges
H410 : très toxique pour les organismes aquatiques,
entraîne des effets à long terme
Solvant organique
cyclohexène
/
Solvant organique
1
/
5
100%