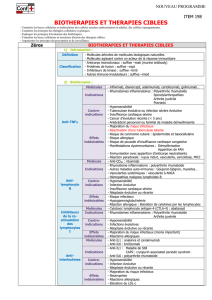
Risque de cancer chez les patients avec une AR

Néoplasies et immunosuppresseurs
en rhumatologie
Louis Bessette MD, MSc, FRCPC
Centre Hospitalier de l’Université Laval
(CHUL)

Conflits d’intérêts
Conférencier
Amgen, BMS, Janssen, Roche, UCB, AbbVie, Pfizer, Merck
Consultant
Amgen, BMS, Janssen, Roche, UCB, AbbVie, Pfizer, Celgene
Recherche
Amgen, BMS, Janssen, Roche, UCB, AbbVie, Pfizer, Merck,
Celgene, Sanofi

Objectifs
•Tenir compte du risque de développer une néoplasie
lors de la prescription et suite à l'utilisation des
différents immunosuppresseurs;
•Élaborer un plan de dépistage adapté de néoplasie
chez les patients immunosupprimés;
•Mesurer le risque d'utiliser un immunosuppresseur
chez un patient avec antécédent de cancer ou
discuter des précautions à prendre dans l’utilisation
des immunosuppresseurs chez les patients avec
antécédents de cancer.

PRÉSENTATION EN SIX QUESTIONS
•Les patients avec une arthrite rhumatoïde (AR) ont-il un
risque plus élevé de cancer?
•Est-ce que les biologiques augmentent l’incidence des
lymphomes?
•Est-ce que les biologiques augmentent le risque de
cancer solide?
•Est-ce que les biologiques augmentent le risque de
récurrence de cancer chez les patients avec une histoire
de cancer?
•Est-ce que les biologiques augmentent la mortalité chez
les patients avec une AR qui développent un cancer?
•Dans quel cas devrait-on être prudent ou faire un
dépistage?

Sujets qui ne seront pas discutés
•Risque de néoplasie avec les ARMMs non
biologiques (méthotrexate) et les
immunosuppresseurs (cyclophosphamide,
azathioprine, etc.)
•Prise en charge du patient avec arthropathie
inflammatoire et cancer
ARMM: Les anti-rhumatismaux modificateurs de la maladie
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
 26
26
 27
27
 28
28
 29
29
 30
30
 31
31
 32
32
 33
33
 34
34
 35
35
 36
36
 37
37
 38
38
 39
39
 40
40
1
/
40
100%