Additions nucléophiles suivies d`élimination

Chimie organique
Chapitre 3 : Additions nucléophiles
suivies d'élimination
I ) Acides carboxyliques et dérivés
d'acide
1 ) Les acides carboxyliques
Structure
Nucléophilie / électrophilie
Acide / base
Réduction

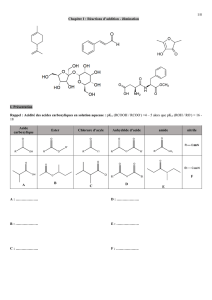
2 ) Les dérivés d'acide
Groupement inductif attracteur et mésomère
donneur.
0,285
0,194
0,84
0,286
1,53
E
BV
(eV)
Me O Me
Me Me
OMe
NH
2
O
O
O
O O
Me Cl
O
chlorure d'acide
ester
amide
anhydride
cétone
réactivité croissante

3 ) Propriétés spectroscopiques
Cf tableau

II ) Synthèse des esters
1 ) Activation de l'acide carboxylique
Les acides carboxyliques sont trop peu
électrophiles pour réagir directement avec les
alcools.
→ activation de l'acide carboxylique ces réactifs
afin d’augmenter le caractère électrophile du
carbone.

Activation ex situ&:
Transformation en chlorures d’acyle ou en
anhydrides d'acide.
R OH
O
chauffage
2
R O
O
R
O
+ H
2
O
R OH
O
SOCl2
R Cl
O
SO2 + HCl
+
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
1
/
18
100%