T100-4-3029-3p - Société de Pathologie Exotique

Bull Soc Pathol Exot, 2007, 100, 4, 261-263 261
Description d’une forme particulière de maladie
de Hodgkin associée à une infection par le virus
Epstein-Barr.
A. Elira Dokekias (1), I. Koko (1), F.O. Atipo Galiba (1) & A. Martin (2)
(1) Service d’hématologie, CHU de Brazzaville, BP 13027, Brazzaville, République du Congo. E-mail : dokekias@yahoo.fr
(2) Service d’anatomie et de cytologie pathologique, CHU Avicenne, 125 avenue de Stalingrad, 93009 Bobigny, France.
Manuscrit n° 3029. “Clinique”. Reçu le 19 octobre 2006. Accepté le 12 juin 2007.
CLINIQUE
Summary: Description of a peculiar form of Hodgkin’s disease associated with Epstein-Barr virus
infection.
The authors report a peculiar form of Hodgkin’s disease that is associated with Epstein-Barr virus
infection. A 16-year-old patient was admitted for an autoimmune haemolytic anaemia associated
with IgG auto-immune antibodies, linked to general clinical complications, cervical adenopathies
and splenomegalia. The patient underwent hemicavectomy that was not histologically investigated.
The ganglionar exeresis helped to establish the histological diagnosis of Hodgkin’s disease, classic
form with nodular sclerosis. Tumour cells were CD30 CD15 positive and neighbouring lymphoid
cells were CD3 and CD20 positive. In situ hybridation allowed the detection of Epstein-Barr virus in
tumour cells. Under ABVD chemotherapy, supplemented with acyclovir and initial corticotherapy,
mid-treatment evolution appears to be favourable. This observation is consistent with the hypothesis
that tumour cells are of B cell origin during Hodgkin’s disease, together with the involvement of
Epstein-Barr virus in lymphomagenesis.
Résumé :
Les auteurs rapportent une forme particulière de maladie de Hodgkin associée à la présence du virus
Epstein-Barr. Il s’agit d’un adolescent de 16 ans, admis pour anémie hémolytique auto-immune avec
présence d’auto-anticorps de type IgG, associée à des signes généraux d’évolutivité clinique, des
adénopathies cervicales et une splénomégalie.
Il a subi quelques mois auparavant une hémi-cavectomie, non analysée au plan histologique.
L’exérèse ganglionnaire a conduit au diagnostic histologique de maladie de Hodgkin, forme classi-
que, sclérose nodulaire. Les cellules tumorales sont CD30, CD15 positives et les cellules lymphoïdes
environnantes sont CD3 et CD20 positives.
L’hybridation in situ (hôpital Avicenne) a permis d’isoler l’EBV au sein des cellules tumorales. Sous
chimiothérapie (ABVD) associée à l’acyclovir ainsi qu’à une corticothérapie initiale, l’évolution à mi-
parcours semble bonne.
Cette observation renforce l’hypothèse de l’origine B des cellules tumorales au cours de la MDH ainsi
que l’implication du virus EBV dans le processus de lymphomagenèse.
Hodgkin
disease
infection
therapeutics
Epstein-Barr
hospital
Brazzaville
Congo
Sub Saharan Africa
Hodgkin
maladie
infection
thérapeutique
Epstein-Barr
hôpital
Brazzaville
Congo
Afrique intertropicale
Introduction
Depuis la description en 1932 par Thomas HODGKIN de
cette hémopathie maligne, de nombreux progrès ont été
réalisés dans la compréhension des aspects étiopathogéniques,
cliniques et histopathologiques.
La démonstration de la nature lymphoïde B de la cellule de
Hodgkin ainsi que l’existence d’une association au virus Eps-
tein-Barr (EBV) sont récentes. La présente enquête rapporte,
chez un sujet jeune, des aspects cliniques particuliers d’une
forme de maladie de Hodgkin, où les analyses spécialisées
témoignent de la présence de l’EBV.
Cas clinique
Monsieur M. D., 16 ans, est admis dans le service d’hématologie du
Centre hospitalier et universitaire de Brazzaville le 31 juin 2006, pour
fatigue, fièvre et émission d’urines d’aspect Coca-Cola.
Dans l’histoire de la maladie, on retient qu’il a subi une hémi-cavectomie
en mai 2004 : les analyses histologiques n’ont pu être obtenues.
L’histoire actuelle remonterait au mois de mai 2006, par des épisodes
de fièvre traités sans succès comme un paludisme, une salmonellose
et une infection des voies aériennes supérieures. Ce tableau clinique
s’aggrave en juin 2006 et est assimilé à une hématurie, motivant l’ad-
mission dans le service.
Examen clinique à l’arrivée
L’examen relève :
– une pâleur importante des conjonctives et des téguments ;
– un ictère ;
– un amaigrissement (poids antérieur 52 kg ; poids actuel 41 kg), soit
> 10 % ;
– des sudations très importantes, en particulier nocturnes ;
– une présence d’adénopathies cervicales bilatérales, indolores et fer-
mes, dont le diamètre pour la plus volumineuse atteint 3-4 cm ;
– une splénomégalie dépassant de 10 cm le rebord costal, mais pas
d’hépatomégalie ;
– un souffle systolique d’intensité mineure à l’auscultation cardiaque

Clinique 262
Elira Dokekias, I. Koko, F. O. Atipo Galiba & A. Martin
et une auscultation pulmonaire normale ;
– la présence de lésions micronodulaires autour du cavum à l’examen
ORL.
Bilan complémentaire à l’admission
– radiographie thoracique normale ;
– échographie abdominale et scanner abdomino-pelvien confirmant
la présence d’une splénomégalie hétérogène et l’absence d’adénopa-
thies profondes ;
– hémogramme : Hb : 5,5 g/dl ; Ht : 16,6 ; VGM 98/fl ; leucocytes
6,2 giga/l ; plaquettes 186 giga/l ;
– autres examens biologiques : VS : 100 mm (1re heure) ; ALAT : 48,8
UI/l ; ASAT : 45,9 UI/l ; LDH : 1 200 UI/l ; bilirubine libre : 68 mg/l ;
– test de Coombs direct érythrocytaire positif ;
– biopsie ganglionnaire et histologie standard après inclusion en
paraffine et coloration : caractère remanié et tumoral du ganglion
avec une architecture nettement scléronodulaire.
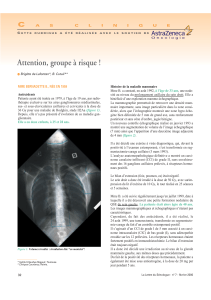
Les nodules renferment de nombreuses cellules tumorales de grande
taille de Reed Sternberg ou de Hodgkin avec des éléments lacunaires
(photo 1 à 4). Elles sont par endroits nombreuses, formant des pla-
ges pseudo-syncitiales. Le fond est constitué de petits lymphocytes,
de plasmocytes, d’histiocytes et d’assez nombreux polynucléaires
éosinophiles.
– immuno-histochimie :
• CD30 : vive positivité membranaire et cytoplasmique des cel-
lules tumorales ;
• CD15 : positivité cytoplasmique des cellules tumorales (faible
positivité des témoins internes, c’est-à-dire des polynucléaires
neutrophiles) ;
• CD3 : positivité de la majorité des petits lymphocytes dans
l’environnement des cellules tumorales ;
• CD20 : positivité des petits lymphocytes dispersés ou regroupés
en petits amas. Positivité focale de quelques cellules de grande
taille.
– hybridation in situ : sonde EBER : vive positivité nucléaire des
cellules tumorales, témoignant de la présence de l’EBV ;
– biopsie ostéo-médullaire : absence d’image d’infiltration tumo-
rale ; hyperplasie de la lignée rouge ; présence de cellules lymphoïdes
d’allure infiltrées ;
– traitement institué ;
• dans un 1er temps ; prédnisone 2 mg/kg/j + acide folique 20 mg/j
+ transfusion de 3 unités de concentrés de globules rouges ;
• dans un 2e temps, après obtention des analyses histologi-
ques, le patient reçoit une poly-chimiothérapie de type ABVD
(doxorubicine 30 mg dose totale J1, et J15 ; bléomycine 15 mg
dose totale J1 et J15 ; vinblastine 7,5 mg dose totale J1 et J15 ; à
défaut de dacarbazine, cyclophosphamide 500 mg J1 et J15, le
tout en IV).
Ce traitement est associé à la prise d’acyclovir 10 mg/kg/j toutes
les 8 heures pendant 15 jours, puis relais per os 5 mg/kg/j toutes les
12 heures pendant 15 jours.
Évolution
Elle est marquée par la correction de l’anémie, la disparition des signes
généraux et du syndrome splénoganglionnaire.
Le patient est revu au début du mois de septembre 2006 et poursuit
normalement son traitement.
Discussion
La maladie de Hodgkin (MDH) est une hémopathie mali-
gne rare, dont le pronostic est d’autant meilleur, du fait
de sa sensibilité au traitement, que les indications thérapeu-
tiques sont adaptées au stade évolutif (3). Dans une étude
antérieure en Afrique, il est rapporté des résultats thérapeu-
tiques encourageants, malgré un contexte socio-économique
peu favorable (2). La présente observation médicale conduit
aux commentaires suivants :
Au plan du diagnostic positif
Même s’il existe des formes frontières (3) dont l’aspect his-
tologique seul ne peut permettre des conclusions sans apport
Photo 1.
Architecture ganglionnaire au faible grossissement (coloration standard).
Ganglionar architecture at low magnification (standard coloration).
Photo 2.
Architecture à fort grossissement d’une cellule de Reed Sternberg.
Architecture at high magnification of Redd Sternberg cell.
Photo 4.
Hybridation
in situ
(EBER) pour l’EBV (x 200 marquage nucléaire en noir).
In situ Hybridation (EBER) for EBV (x 200 nuclear labelling in black).
Photo 3.
Immuno-marquage à l’anti-CD30 :
marquage membranaire et cytoplasmique des cellules tumorales x 200.
Immuno labelling with anti CD30:
membranous and cystoplasmic labelling of the tumour cells x 200.

Description dʼune forme particulière de maladie de Hodgkin.
Bull Soc Pathol Exot, 2007, 100, 4, 261-263 263
des examens immuno-histochimiques, cette forme correspond
au type classique (sclérose nodulaire).
Cependant, la présentation clinique initiale sous forme d’ané-
mie hémolytique auto-immune est une complication rare de
la MDH (3, 9, 11).
Le patient présente à l’admission des signes généraux d’évo-
lutivité clinique se traduisant par une importante perte pon-
dérale et des sudations abondantes.
On peut relever que le stade tardif du diagnostic de cette
hémopathie maligne aurait dû être évité à l’époque où ce jeune
patient avait subi une hémi-cavectomie sans étude histolo-
gique.
Au plan histologique, l’évidence du diagnostic positif du
lymphome a permis la description de cette forme classique
(sclérose nodulaire), la plus fréquente et de meilleur pronostic
(4).
Grâce à la collaboration Nord-Sud, le ganglion, à travers ses
coupes, a pu bénéficier d’analyses immuno-histochimiques,
confirmant le marquage positif par les anticorps monoclonaux
CD30 et CD15 (3).
On peut tout de même relever la positivité des lymphocytes
CD20 groupés en amas de petite et grande taille, traduisant
la nature B de la prolifération lymphoïde qui est évoquée à
l’origine des cellules de Hodgkin et/ou des cellules de Reed
Sternberg (3, 6, 12).
Étiopathogénie
Les techniques d’hybridation in situ rapportées par d’autres
études (1, 6, 8) ont permis de faire la démonstration de la pré-
sence du virus d’EBV au sein des cellules tumorales étudiées.
Cependant, l’association la plus fréquente est rapportée dans
la MDH, forme classique à cellularité mixte, 50-75 % des cas,
plutôt que dans les formes à scléroses nodulaires (3, 11, 7).
De plus, la présence du virus semble augmenter chez les
enfants de bas niveau socio-économique, (tel est le cas de
notre patient) (5, 10).
Il existe plusieurs arguments en faveur de l’implication de
l’EBV dans la pathogénie de la MDH EBV positive :
– présence du virus dans les cellules ;
– intégration clonale dans le génome cellulaire ;
– présence de l’expression des protéines virales par les cellules
de Reed Sternberg (LMP-1 plus particulièrement) (1, 8, 12),
ce qui n’a pu être étudié dans notre cas.
Traitement et évolution
Le patient a bénéficié d’une polychimiothérapie de type
ABVD qui se poursuit actuellement. On peut remarquer après
deux cures une réponse clinique satisfaisante.
La polychimiothérapie classique réalisée dans ce cas et dans
d’autres études ne montre pas de différence significative en
termes de résultats, avec les formes non-EBV positives de la
MDH. Cependant, l’association de la polychimiothérapie
au traitement par acyclovir, tel que cela est proposé dans les
formes de mononucléose infectieuse suraiguës, est discutée
(7, 9, 11). L’avantage de cette approche découle de la forme
particulière, inaugurée ici par un tableau d’anémie hémolyti-
que à Coombs direct positif, corrigée par la corticothérapie
prescrite avant chimiothérapie et poursuivie de J2 à J14.
Conclusion
La description de ce cas clinique assez complexe permet
de renforcer l’hypothèse selon laquelle certains virus, en
particulier l’EBV, sont impliqués dans le processus de lym-
phomagenèse. Si cela est établi depuis plusieurs années dans
la forme endémique du lymphome de Burkitt, l’association de
plus en plus décrite du virus EBV avec la MDH se place dans
la lignée discutée de l’origine B des cellules tumorales.
Aussi, la prise en charge thérapeutique de ces formes cliniques
se doit d’être particulière.
Références bibliographiques
1. ANDERSSON J – Epstein-Barr virus and Hodgkin’s lymphoma.
Herpes, 2006, 13, 12-16.
2. ELIRA DOKEKIAS A, CHASEN M, MARTIN A & RAPHAËL M –
Résultats thérapeutiques au cours de la maladie de Hodg-
kin. Revue internationale des sciences médicales, 2003, 5,
102-108.
3. GAULARD PH & BROUSSE N – Lymphomes Hodgkiniens et
formes frontières. Hématologie, 2002, 8, 61-73.
4. JAFFE ES, HARRIS NL, STEIN H & VARDIMAN JW (eds) – World
Health Organization classification of tumours. Pathology
and genetic of tumours of haematopoietic and lymphoid
tissues. Lyon IARC Press, 2001.
5. JARRETT RF – Risk factors for Hodgkin’s lymphoma by
EBV status and significance of detection of EBV genomes
in serum of patients with EBV-associated. Hodgkin’s lym-
phoma. Leuk lymphoma, 2003, 44, 527-532.
6. KEEGAN TH, GLASER SL, CLARKE CA, GULLEY ML, CRAIG FE
et al. – Epstein-Barr virus as a marker of survival after Hodg-
kin’s lymphoma: a population-based study. J Clin Oncol,
2005, 23, 30, 7604-7613.
7. KERESZTES K, MILTENYI Z, BESSENYEI B, BECK Z, SZOLLOSI Z
et al. – Association between the Epstein-Barr virus and
Hodgkin’s lymphoma in the North Eastern part of Hungary:
Effects on therapy and survival. Acta Haematol, 2006, 116,
101-107.
8. KORBI S, TRIMECHE M, SRIHA B, YACOUBI MT, HMISSA S et
al. – Epstein-Barr virus in Hodgkin’s disease: the example of
central Tunisia. Ann pathol, 2002, 22, 96-101.
9. KRUGMANN J, TZANKOV A, GSCHWENDTNER A, FISCHHO-
FER M, GREIL R et al. – Longer failure-free survival interval of
Epstein-Barr virus associated classical Hodgkin’s lymphoma: A
single institution study. Mod Pathol, 2003, 16, 566-573.
10. OTHIENO-ABINYA NA, ABWAO HO, OPIYO A, NJUGUNA E,
MAINA JM & NYABOLA LO – Hodgkin’s lymphoma in the
1990’s: a Kenyatta national hospital experience. East Afr
Med J, 2005, 82, 60-66.
11. PROVENCIO M, ESPANA P, MILLAN I, YEBRA M, SANCHEZ
AC et al. – Prognostic factor in Hodgkin’s disease. Leuk Lym-
phoma, 2004, 45, 1133-1139.
12. THEIL J, LAUMEN H, MARAFIOTI T, HUMMEL M, LENZ G et
al. – Defective octamer-dependent transcription is respon-
sible for silenced immunoglobulin transcription in Reed-
Sternberg cells. Blood, 2001, 97, 3191-3196.
1
/
3
100%