Une nouvelle stratégie thérapeutique parvient à vaincre la résistance

46 02
_ 2013 _ info@onkologie
RAPPORT SPÉCIAL
Inhibition de la voie de signalisation mTOR
Une nouvelle stratégie thérapeutique
parvient à vaincre la résistance
Importance de la voie de signalisation
mTOR dans les cellules tumorales
résistantes
mTOR (Mammalian Target of Rapamycin) est
une protéine qui se lie à la rapamycine, une
molécule immunosuppressive. Elle intervient
dans la prolifération, la différenciation et la
multiplication cellulaire et assure la survie des
cellules. mTOR est activée par le récepteur
à l’EGF (facteur de croissance épidermique)
et contrôle la traduction des protéines et des
facteurs de transcription. La prolifération, la
croissance des cellules et l’angiogenèse sont
stimulées par cette voie de signalisation qui ré-
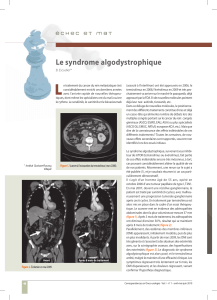
prime en outre l’apoptose (3, 4) (fi g. 1). Dans
les tumeurs malignes, mTOR est souvent sur-
activée. Il en résulte une augmentation de la
synthèse protéique. Une croissance incontrô-
lée, un métabolisme anormal et une augmen-
tation de l’angiogenèse tumorale sont alors
rendus possibles et la survie des cellules ma-
lignes est assurée (5). Les mutations en me-
sure d’activer mTOR font partie des anomalies
génétiques les plus fréquentes en cas de can-
cer (6–8). L’activation de mTOR joue ainsi un
rôle important dans l’apparition du cancer et la
progression tumorale.
La voie de signalisation mTOR, avec son rôle unique et crucial dans les cellules tumorales
ayant développé une résistance ou un mécanisme « escape » envers certains traitements,
est très importante. En effet, elle constitue la base d’une nouvelle approche thérapeu-
tique chez les patient(e)s dont la maladie est en progression. Cette stratégie vise à répri-
mer l’angiogenèse et la prolifération dans différents types de cancer, pour permettre une
nouvelle réponse de la tumeur au traitement.
mTOR étant suractivée dans toute une
série de types cancéreux, l’utilisation d’inhi-
biteurs de mTOR dans des objectifs thérapeu-
tiques variés semble indiqué. Le traitement
par l’inhibition de mTOR de différents types
de cancer, en particulier du cancer rénal,
des tumeurs neuroendocrines d’origine pan-
créatique (pNET) et du cancer du sein, s’est
effectivement avéré une stratégie thérapeu-
tique effi cace. L’inhibition de mTOR représente
en outre une approche importante concernant
le contournement de la résistance et des mé-
canismes « escape » ainsi que pour la répres-
sion de l’angiogenèse et de la prolifération des
cellules tumorales. Pour ces raisons, cette
stratégie semble tout à fait fondée pour le trai-
tement antitumoral. L’évérolimus est un inhibi-
teur de mTOR qui exerce aussi bien un effet
direct sur les cellules tumorales qu’une ac-
tion indirecte par inhibition de l’angiogenèse.
Cette molécule exerce un effet à différents ni-
veaux dans la voie de signalisation. D’un côté,
le blocage de mTOR diminue la production de
la protéine HIF-1 (facteur inductible par l’hy-
poxie), qui est un activateur de l’angiogenèse
et d’un autre côté, des effets en aval sont éga-
lement inhibés, comme la production du VEGF
(Facteur de croissance endothéliale vascu-
laire). Un deuxième mécanisme essentiel ré-
side dans le blocage de la prolifération des
cellules à l’origine de l’angiogenèse. L’évéroli-
mus est administré une fois par jour par voie
orale et les études rapportent une bonne tolé-
rance globale.
L’inhibition de mTOR pour traiter
le cancer rénal
Les premières études menées sur l’évérolimus
ont été effectuées auprès de patients atteints
de cancer rénal avancé (mRCC). Dans ce type
de cancer, l’angiogenèse est augmentée par la
perte du gène de suppression tumorale (gène
VHL), ce qui conduit à une augmentation de la
production du facteur de transcription HIF-1. Le
HIF-1 induit la production de facteurs de crois-
ance angiogéniques comme le VEGF et stimule
le métabolisme des cellules tumorales. Le HIF-1
joue un rôle très important dans le mRCC. Ces
éléments ont constitué la base rationnelle pour
la réalisation des études sur les effets de l’évé-
rolimus sur ce cancer. Le cancer rénal est une
maladie fréquemment associée à un pronostic
défavorable. La chimiothérapie et les cytokines
sont ineffi caces. Le taux de survie au bout de
5 ans est inférieur à 10 %. L’évérolimus, un in-
hibiteur de mTOR, permet de contourner la ré-
sistance aux inhibiteurs de tyrosine kinase (TKI)
et de resensibiliser le patient à ces derniers.
La toxicité cumulée est également plus faible.
Les résultats cliniques sur l’effi cacité (survie
sans progression) de l’évérolimus sont convain-
cants et le profi l de sécurité est favorable.
L’étude RECORD-1 montre que l’évérolimus ré-
duit de 67 % le risque de progression de la ma-
ladie (9). Les participants à RECORD-1 étaient
des patients atteints de cancer rénal méta-
statique ayant progressé sous traitement par
TKI-VEGFR. Les patients ont été traités après
randomisation soit par de l’évérolimus, 10 mg/j
Figures : Novartis Pharma Schweiz AG
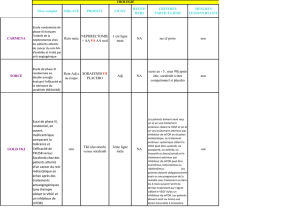
Fig. 1: Voie de signalisation mTOR dans une cellule normale
Fig. 2: Voie de signalisation dans une cellule tumorale

info@onkologie
_ 02 _ 2013 47
RAPPORT SPÉCIAL
(n=277) soit par un placebo (n=139) en asso-
ciation avec les mesures symptomatiques. Le
critère d’évaluation primaire était la survie sans
progression (PFS) après examen centralisé in-
dépendant. Parmi les patients ayant été traités
auparavant par un seul TKI-VEGFR, la PFS mé-
diane a été de 5,4 mois sous évérolimus contre
1,9 mois sous placebo, ce qui représente une ré-
duction du risque de 68 % (HR: 0,32, intervalle
de confi ance à 95 % [IC]: 0,24- 0,43, p<0,001).
Parmi les patients ayant été traités auparavant
par deux TKI-VEGFR, la PFS médiane a été de
4,0 mois sous évérolimus contre 1,8 mois sous
placebo (HR: 0,32, intervalle de confi ance à
95 %: 0,19-0,54, p <0,001). Le profi l de sécurité
a été identique dans les deux groupes. Au cours
de l’analyse intermédiaire d’une étude d’obser-
vation non interventionnelle et prospective au-
près de 400 patients, l’évérolimus a permis une
durée jusqu’à la progression de 7 mois après
échec de la première thérapie anti-VEGF (10).
Après le traitement par évérolimus, un TKI peut
à nouveau être utilisé avec succès (11).
Ces résultats plaident en faveur de l’utili-
sation de l’évérolimus en tant que médicament
standard lorsque le premier traitement par TKI-
VEGFR échoue. En raison des résultats positifs
de l’étude de phase III RECORD-1, les direc-
tives cliniques américaines et européennes re-
commandent l’utilisation de l’évérolimus chez
les patients souffrant de mRCC réfractaire aux
TKI-VEGFR.
L’inhibition de mTOR contre les tumeurs
neuroendocrines pancréatiques
L’évérolimus a également sa place dans le trai-
tement des tumeurs neuroendocrines pan-
créatiques (TNEp). En Suisse, il est autorisé
pour le traitement des patients porteurs de tu-
meurs neuroendocrines d’origine pancréatique
avancées, en progression, fortement ou mo-
dérément différenciées. L’effi cacité de l’évéro-
limus a été examinée au cours de l’étude de
phase III randomisée et contrôlée contre place-
bo RADIANT-2 auprès de patients souffrant de
tumeurs neuroendocrines avancées de grade
faible ou intermédiaire en comparant l’évéroli-
mus à 10 mg/j avec un placebo, les deux en
association avec 30 mg d’octréotide LAR (13).
La durée médiane de survie sans progression
a été de 5,1 mois plus longue dans le groupe
sous évérolimus que dans le groupe sous pla-
cebo (16,4 contre 11,3 mois) mais la limite de
signifi cativité a été manquée de peu.
Au cours de RADIANT-3, une étude de
phase III randomisée en double aveugle,
410 patients atteints de TNEp avancée (non ré-
sécable ou métastatique) de grade 1 ou 2 ont
été traités par l’évérolimus (10 mg/j) ou placebo
après randomisation (14). La survie sans pro-
gression sous évérolimus a été plus du double
de celle sous placebo (11,0 contre 4,6 mois,
HR: 0,35, p<0,0001), ce qui signifi e que le
risque de progression ou de décès a été ré-
duit de 65 % par l’inhibition de mTOR. Après
18 mois, une absence de progression était
constatée chez 34,2 % des patients sous évé-
rolimus contre 9 % sous placebo. Ce bénéfi ce
a été indépendant de l’âge, du sexe, de la ré-
gion géographique, du grade de la tumeur,
des performances et du traitement antérieur
par des analogues de la somatostatine ou de
la chimiothérapie. Les effets indésirables mé-
dicamenteux ont été généralement de grade
1 ou 2. Parmi les effets indésirables de grade
3/4, seules l’anémie (6 % contre 0 %) et l’hy-
perglycémie (5 % contre 2 %) ont été obser-
vées plus fréquemment sous évérolimus que
sous placebo. Selon les auteurs du consen-
sus ENETS (15), l’évérolimus représente chez
les patients atteints de TNEp une option thé-
rapeutique après échec de la chimiothérapie,
mais peut également être envisagé en première
intention. Dans l’étude RADIANT-3, 40 % des
patients n’avaient pas été traités auparavant et
leurs résultats ont été similaires à ceux des pa-
tients pré-traités (14).
Au cours de RADIANT-4, étude de phase III
randomisée, multicentrique et en double
aveugle, l’évérolimus sera comparé en terme
d’effi cacité avec un placebo, les deux en as-
sociation avec le meilleur traitement disponible
(BSC) dans les tumeurs neuroendocrines avan-
cée d’origine gastrointestinale ou pulmonaire.
Le critère d’évaluation primaire sera la survie
sans progression. Les critères secondaires se-
ront la survie globale et la sécurité par rapport
au placebo.
L’inhibition de mTOR contre le cancer
du sein positif pour les récepteurs
aux hormones
En dépit des progrès continus dans le traitement
du cancer du sein au cours des deux dernières
décennies, la situation des patientes atteints de
cancer du sein avancé ne s’est que sensiblement
améliorée. L’effi cacité clinique des options théra-
peutiques disponibles est limitée. Après l’appa-
rition de métastases éloignées, la survie globale
médiane des patientes se situe entre 18 et 36
mois seulement après la pose du diagnostic (16).
Une espérance de vie de 2 à 3 ans ne constitue
pas une perspective thérapeutique satisfaisante.
Le traitement endocrinien constitue la base de la
thérapie du cancer du sein positif pour les récep-
teurs hormonaux (17). Néanmoins, chez environ
50 % des patientes, la réponse est absente ou in-
suffi sante à ce traitement endocrinien initial et les
patientes qui réagissent au traitement au début
développent en général une résistance tôt ou tard
(18, 19). Le développement de résistances à l’en-
docrinothérapie représente le problème clinique
majeur inhérent au traitement du cancer du sein
positif pour les récepteurs hormonaux. La voie de
signalisation endocrine et la voie de signalisation
mTOR étant impliquées dans la résistance endo-
crine, un traitement associé semble indiqué.
IMPRESSUM
Rapport : Prof. Dr. Dr. h.c. Walter F. Riesen
Rédaction : Christian Heid
Avec le soutien de Novartis Pharma Schweiz AG, Berne
© Aerzteverlag medinfo AG, Erlenbach
Références :
1. Early Breast Cancer Trialists‘ Collaborative Group.
Tamoxifen for early breast cancer: an over-
view of the randomised trials. Lancet. 1998 May
16;351(9114):1451-67
2. Gradishar WJ. Tamoxifen – what next? Oncologist.
2004;9:378-84
3. Jacinto E., Hall MN. Tor signalling in bugs, brain
and brawn. Nat Rev Mol Cell Biol. 2003; 4:117-26.
4. Schmelzle T, Hall MN. TOR, a central controller of
cell growth. Cell. 2000;103:253-62
5. Shaw RJ, Cantley LC. Ras, PI(3)K and mTOR si-
gnalling controls tumour cell growth. Nature.
2006;441:424-430
6. Benjamin D et al. Rapamycin passes the torch: a
new generation of mTOR inhibitors. Nat Rev Drug
Discov. 2011;10:868-80.
7. Wullschleger S, et al. TOR signaling in growth and
metabolism. Cell. 2006;124:471-484
8.
Humar R, et al. Hypoxia enhances vascular cell proli-
feration and angiogenesis in vitro via rapamycin
(mTOR)-dependent signaling. FASEB J. 2002;16:
771-780. Erratum in: FASEB J. 2006; 20:1573
9. Motzer RJ, Escudier B, Oudard S, et al. Phase 3 tri-
al of everolimus for metastatic renal cell carcinoma:
fi nal results and analysis of prognostic factors. Can-
cer 2010;116:4256–65
10. Staehler M et al J Clin Oncol 2012;30: suppl 5;abs-
tract 361
11. Grunwald V et al Br J Cancer 2011;doi10.1038/
bic.2011. Published online October 27;2011
12.
Calvo et al. What is the optimal therapy for patients with
metastatic renal cell carcinoma who progress on an initi-
al VEGFr-TKI? Cancer Treatment Reviews 2012 in press
13. Pawel M et al. Everolimus plus octreotide long ac-
ting repeatable fort he treatment of advanced neu-
roendocrine tumours associated with carcinoid syn-
drome (RADIANT-2: a randomised, placebo-cont-
rolled, phase 3 study. Lancet 2011;378:2005-2012
14.
Yao JC et al. Everolimus for advanced pancreatic neu-
roendocrine tumors. N Engl J Med 2011;364:514-523
15. Pawel M et al. ENETS consensus guidelines for the
management of patients with liver and other distant
metastases from neuroendocrine neoplasms of fore-
gut, midgut, hindgut, and unknown primary. Neuro-
endocrinology 2012;95:157-176)
16. Enju A et al. Weekly administration of docetaxel and
paclitaxel in metastatic or advanced breast cancer.
Oncologist 2005;10:665-685
17. Schiff R et al. Breast cancer endocrine resistance:
how growth factor signalling and estrogen receptor
coregulators modulate response. Clin Cancer Res
2003;9 (1 Pt 2):447S-454S
18. Harichand-Herdt S, et al. Endocrine treatment of
postmenopausal women with breast cancer. Expert
Rev Anticancer Ther 2009;2:187-198
19. Normanno N, et al. Mechanisms of endocrine re-
sistance and novel therapeutic strategies in breast
cancer. Endocr Relat Cancer 2005;4:721-747
1
/
2
100%