cours RX - CPGE Brizeux

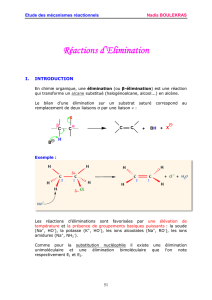
Les liaisons simples carbone-halogène
I) Présentation des halogénoalcanes :
1. Définition et classe
:
Def :
Restriction :
Les éléments de la famille des halogènes sont : F, Cl, Br, I et At. Toutefois, l’astate étant radioactif et le fluor
donnant des fluoroalcanes peu réactifs, on ne s’intéressera qu’au cas où X est Cl, Br ou I
Classe :
Comme pour un carbocation ou un alcool, la classe de l’halogénoalcane dépend du nombre de chaînes carbonées
liées au carbone portant l’halogène.
primaire secondaire tertiaire
2. Origine et utilisation
:
Les halogénoalcanes sont plutôt rares dans la nature. On
peut citer le pourpre, pigment naturel extrait d’un
mollusque marin, qui servait déjà dans l’antiquité pour
orner les toges romaines comme insigne de leur rang
social.
Dans l’industrie, ils jouent de très nombreux rôles :
• Dans les insecticides : bromoéthane (insecticide aujourd’hui interdit)
DDT
• Dans les solvants : dichlorométhane CH
2
Cl
2,
chloroforme CHCl
3
, tétrachlorure de
carbone CCl
4
(solvant exceptionnel mais aujourd’hui quasiment interdit car
cancérigène)
• Dans les polymères : le PVC plastique d’usage courant (sacs plastiques, bouteilles …),
ou le PTFE (Téflon)
• Dans les liquides caloporteurs : CFC (petites molécules ne
comportant que des atomes de carbone, fluor et chlore) aujourd’hui
remplacés par les HFC (petites molécules ne comportant que des atomes d’hydrogène, fluor et
carbone)
3. Propriétés de la liaison C-X :
Longueur de liaison :
Halogène X Cl Br I
Longueur de la liaison C-X en pm 177 194 214
Energie de liaison en kJ.mol
-1
327 285 213
Quand on descend dans la colonne des halogènes :
N
O
Br
N
O
Br
Pourpre
H
H
Cl Cl
Cl
C
l
Cl
DDT
Cl
PVC
n
F
F
F F
PTFE
n

Polarité :
Halogène X Cl Br I
Electronégativité (échelle de Pauling) 3,1 2,9 2,6
Moment dipolaire de la liaison C-X en D 1,57 1,48 1,29
Rappel : χ(c) = 2,5 χ(H) = 2,2 1D = 3,33.10
-30
C.m
(il y a ici 2 effets qui joue en sens contraire car µ = δ d, d’une part la longueur augmente, mais la charge partielle
δ diminue du fait de la baisse de différence d’électronégativité, et c’est ce 2
ème
effet qui l’emporte)
Polarisabilité :
4. Réactivité :
Toute la réactivité des halogénoalcanes a pour origine la polarité de la liaison C-X.
1
er
cas :
Condition nécessaire pour être un nucléophile :
Attention,
2
ème
cas :

Récapitulatif :
II) Réactions de substitution nucléophile S
N
:
1. Mécanisme limite S
N
2 :
a. Observations expérimentales :
Cinétique :
Ex : −−
+→+ ClOHCHHOClCH
33
Stéréochimie :
Cl
++
Cl
I
H
3
CH
2
C
H
3
C
H
propanone
25 °C
I
C
H
2
C
H
3
CH
3
H
(S) (R)
Cl
++
Cl
I
H
3
CH
2
C
H
H
3
C
propanone
25 °C
I
CH
2
CH
3
HCH
3
(R) (S)
⇒.
b. Mécanisme :
Ex :
c. Diagramme Ep = f(CR)

d. Aspect stéréochimique :
Retournement :
Si le C
α
est asymétrique, et que le nucléophile va occuper la même place dans l’ordre des substituants suivant les
règles CIP que le nucléofuge, alors il y a inversion de configuration absolue.
Ex :
Cl
E
t
Me
H
I
(S)
+
Mais
Cl
H
3
C
S
H
H
3
C
H O
(R)
+
2. Mécanisme limite S
N
1 :
a. Observations expérimentales :
Cinétique :
Ex :
La vitesse est indépendante de la concentration en nucléophile (OH
-
) : quelle conséquence pouvons-nous en tirer
sur le mécanisme ?
Stéréochimie :
Cl
++
Cl
Ph
Me
H
25 °C
HO
P
h
Me
H
(S)
(R) 50%
(S) 50%
DMSO
H O
racémique
b. Mécanisme :
Le mécanisme est en 2 étapes.
1
ère
étape : .
Br +OH
-
OH +Br
-

2
ème
étape :
c. Diagramme Ep = f(CR)
d. Origine de l’absence de stéréosélectivité :
Ex :
3. Compétition S
N
2/ S
N
1 :
Rappelons que la nucléophilie est une considération cinétique :
a. Facteur principal : la classe du substrat
Mécanisme S
N
2 :
Vitesses relatives de la substitution d’un bromoalcane par des ions chlorure dans de l’acétone selon un
mécanisme S
N
2
Cl
-
RCl+ RBr + Br
-
Bromoalcane
H C Br
H
H
H3C C Br
H
H
H3C C
CH3
Br
H
H
3
C C
CH
3
Br
CH
3
Constante de vitesse relative 2,2.10
5
1,4.10
3
1 Trop faible pour
être mesurée
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
1
/
11
100%