Traitement du diabète et cancer - International Diabetes Federation

DiabetesVoice Mars 2014 • Volume 59 • Numéro 1
36
Pratique clinique
Traitement du diabète
et cancer : cinq ans
après l'annonce de
« nouvelles brûlantes
Andrew Renehan
En juin 2009, la publication collective
de quatre études épidémiologiques à
la pointe de l'actualité examinant les
liens entre le traitement du diabète
et le cancer dans le même numéro de
la revue Diabetelogia a suscité un vif
émoi au sein de la communauté du dia-
bète. Ces articles ont mis en lumière
le lien entre l'utilisation thérapeutique
d'insuline exogène et, en particulier,
de glargine (Lantus®), un analogue
d'insuline, et le développement ulté-
rieur d'un cancer. Les quatre études
présentant des limites en termes de
conception, il s'est avéré impossible de
tirer des conclusions définitives. Si les
études ont dans un premier temps créé
la confusion au sein de la communauté
du diabète, des conséquences positives
n'ont cependant pas tardé à émerger.
En 2010, je suis revenu sur les deux
premières années de cette aventure
dans Diabetes Voice.
1
Le présent article
me permettra de faire le point sur les
trois dernières années.
Une des premières conséquences construc-
tives des événements de 2009 a été la ren-
contre de spécialistes en diabétologie et en
cancérologie. Un des exemples visibles a été
la création du Diabetes and Cancer Research
Consortium, un groupe international de
chercheurs qui examine principalement
des questions pharmaco-épidémiologiques,
mais a également pour objectif majeur de
développer et d'optimiser des approches mé-
thodologiques en vue de s'attaquer aux liens
complexes entre le diabète, son traitement
et la cancer. Le groupe a publié deux docu-
ments-cadres : un sur l'incidence du cancer
2
et l'autre sur la mortalité due au cancer.
3
Deux caractéristiques analytiques impor-
tantes ont été mises en exergue : (1) la prise
en compte du « biais de temps de détection »
et (2) la configuration des données pour la
prise en compte des « expositions variables
dans le temps ». La première se traduit par
des associations de risque exagérées en rai-
son de la cooccurrence temporelle du diag-
nostic du diabète, ou du début du traitement,
et du diagnostic du cancer. La deuxième
fait référence aux variations réelles dans les
médicaments prescrits au fil du temps et, à
défaut d'être prise en charge correctement, se
traduit par de fausses associations de risque
dans le sens positif ou négatif.
Insuline glargine
Après 2009, plusieurs études observation-
nelles se sont penchées sur le lien présumé
entre l'insuline glargine et le risque de cancer,
mais, dans l'ensemble (même avec des mé-
thodologies robustes), aucune donnée con-
cluante n'a émergé. La publication de l'essai
ORIGIN en 2012 a toutefois permis de cla-
rifier la situation. Les chercheurs d'ORIGIN
ont réparti aléatoirement 12 537 patients
Le Diabetes and Cancer
Research Consortium
développe et optimise
des approches
méthodologiques
en vue de s'attaquer
aux liens complexes
entre le diabète, son
traitement et le cancer.

DiabetesVoice
Mars 2014 • Volume 59 • Numéro 1 37
Pratique clinique
présentant une intolérance au glucose ou
un diabète de type 2 dans des groupes sous
insuline glargine ou sous traitement stan-
dard4 – le plus grand essai de ce type jamais
réalisé. Même si les critères d'évaluation du
protocole étaient les événements non fatals
et les décès d'origine cardiovasculaire, les
chercheurs ont également détaillé le risque
par type de cancer et par traitement reçu à
la suite des craintes soulevées par les articles
de 2009. Aucun différence n'est apparue
entre les groupes de traitement en ce qui
concerne l'incidence et les décès tous cancers
confondus, pas plus que pour les types de
cancer rapportés suivants : sein, prostate,
côlon, poumon et mélanome. Ces données
semblaient concluantes, ce qui a conduit
certains commentateurs à laisser entendre
que le sujet était clos. Des réserves ont tou-
tefois été émises concernant l'interprétation
de l'essai ORIGIN et du risque de cancer.
Premièrement, bien que le suivi médian ait
été de 6,2 ans, la diminution a été tellement
rapide par la suite que seuls 14 % des patients
ont été suivis la septième année (Figure 1).
Pour de nombreux épidémiologistes du
cancer, cette période de latence trop courte
pour évaluer les liens entre l'exposition et
l'incidence du cancer.
Deuxièmement, la contamination entre les
groupes a été importante – 16,7 % des pa-
tients sous glargine ont arrêté celle-ci, tan-
dis que 11,5 % des patients sous traitement
standard ont commencé
à prendre de l'insuline
sous une forme quelcon-
que durant la période de
suivi. En résumé, la mise
en balance des données
probantes penche en fa-
veur de l'absence de lien
entre l'insuline glargine
et le risque de cancer. Cependant, les ré-
serves émises concernant l'interprétation
de l'essai ORIGIN devraient encourager
les chercheurs d'ORIGIN à analyser leurs
données sur une période de suivi plus lon-
gue et à procéder à une « analyse basée sur
le protocole » (comparaison des groupes
en incluant uniquement les participants
qui ont réussi à maintenir le traitement
qui leur avait été initialement attribué), en
plus de l'« analyse en intention de traiter »
déjà présentée.
Metformine
Aujourd'hui, nous comprenons mieux l'effet
protecteur présumé de la metformine et le
risque de cancer. Il est notamment apparu
de manière claire ces dernières années que
bon nombre des études épidémiologiques
antérieures présentaient des biais liés au
temps importants qui ont donné l'impres-
sion que les résultats étaient « protecteurs
». Mais surtout, elles présentaient des biais
appelés « biais de temps immortel ». Cet
aspect statistique est compliqué d'un point
de vue conceptuel et n'a
peut-être pas été apprécié
correctement par les com-
munautés de chercheurs
en diabétologie et en
cancérologie. Un tel biais
survient lorsque l'analyse
ne prend pas en compte le
laps de temps sans traite-
ment entre le début de l'étude de cohorte et
le début du traitement. Les individus doivent
survivre au début de l'exposition – d'où le
nom d'« immortel ». Le résultat est un avan-
tage pour les utilisateurs du médicament à
Suivi médian
01234567
7000
6000
5000
4000
3000
2000
1000
0
Nb de patients
Années
Figure1. Diminution du suivi selon le traitement attribué dans
le cadre de l'essai ORIGIN
Exposés à la glargine
Non exposés à la glargine
(traitement standard)
Le nombre renseigné pour chaque groupe correspond au nombre de patients suivis après la randomisation moins
ceux qui ont interrompu la glargine dans le groupe de l'intervention et ceux qui ont débuté la glargine dans le
groupe sous traitement standard.
Adapté de la référence n°4.
La mise en balance des données
probantes penche en faveur de
l'absence de lien entre l'insuline
glargine et le risque de cancer.

DiabetesVoice Mars 2014 • Volume 59 • Numéro 1
38
l'étude lorsque l'analyse est classée simple-
ment en fonction des catégories d'utilisation
« toujours » ou « jamais ». Ce phénomène
a été parfaitement illustré par Suissa et ses
collègues5, qui ont établi que de nombreuses
études épidémiologiques faisant état d'une
réduction du risque de cancer associé à la
metformine présentaient un biais de temps
immortel. En revanche, les études faisant
appel à des méthodes analytiques pour éviter
de tels biais n'ont mis en évidence aucun effet
de la metformine sur l'incidence du cancer.
Il est probable que les biais liés au temps
identifiés dans le cadre des études portant
sur l'utilisation de metformine et l'incidence
du cancer sont également fréquents dans les
études de la survie des patients atteints de
cancer sous metformine. Ces incertitudes
font aujourd'hui l'objet de plusieurs essais
randomisés de phase III chez des patients
atteints d'un cancer sans diabète. L'essai NCIC
MA.32 de grande envergure portant sur les
traitements adjuvants dans le cancer du sein
au stade précoce, avec pour principal critère
de référence la survie à cinq ans sans
cancer invasif, en est un exemple
notable. 3 582 femmes ont terminé la
procédure d'enrôlement début 2013
et nous attendons à présent les ré-
sultats de cet essai avec impatience.
Le troisième facteur d'appréciation
clé du lien entre la metformine et le
cancer réside dans la biologie. De
nombreux laboratoires à travers le
monde étudient désormais le rôle
de la metformine dans le dévelo-
ppement de cancers, et plusieurs
nouveaux mécanismes anticancé-
reux ont été décrits et validés. Il est toutefois
apparu que de nombreuses études préclini-
ques in vivo utilisent des concentrations de
metformine supérieures à celles utilisées en
toute sécurité en milieu clinique. En outre, la
plupart des études in vitro indiquent utiliser
des doses de metformine comprises entre 1
et 40 mM, ce qui est bien au-delà des con-
centrations plasmatiques thérapeutiques
pouvant être atteintes (0,465-2,5 mg/l ou
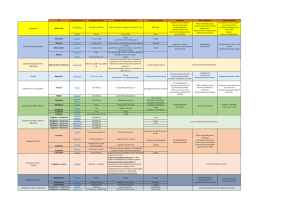
2,8-15 mM) chez l'être humain (Figure 2).
6
Il
est donc possible que la metformine induise
un stress énergétique dans ces études très
supérieur aux effets qui seraient enregistrés
sur le plan clinique. En résumé, la mise en
balance des données probantes penche éga-
lement en faveur de l'absence de lien entre la
metformine et le risque de cancer. La dose
de metformine actuellement utilisée dans les
essais oncologiques est celle qui a démontré
être efficace pour le contrôle de la glycémie.
Il convient à présent de déterminer la dose
appropriée de metformine en vue d'obtenir
l'effet anticancéreux escompté.
Pioglitazone
Lors de l'examen de leurs bases de données,
les chercheurs ont découvert que l'exposi-
tion au pioglitazone pourrait être associée
à un risque accru de cancer de la vessie. Les
premières études reposaient sur des analyses
assez rudimentaires des bases de données
des systèmes d'assurance santé contenant un
faible nombre de cas de cancer de la vessie.
Ce « signal d'alarme » a toutefois suffit pour
que les autorités françaises et allemandes de
réglementation des médicaments retirent
cet agent en juin 2011. Depuis lors, trois
analyses de grande ampleur s'appuyant sur
la General Practice Research Database au
Royaume-Uni,
7
le Système National d'Infor
-
mation Inter-régimes de l'Assurance Maladie
en France
8
et le registre du diabète Kaiser
Permanente Northern California (KPNC)
aux États-Unis9 ont été réalisées – avec un
nombre élevé de cas de cancer de la vessie, et
toutes ont laissé entendre l'existence d'un ris-
que accru de cancer. Mais ici aussi, des biais
pourraient avoir entravé l'interprétation. De
Il convient à présent
de déterminer la
dose appropriée
de metformine en
vue d'obtenir l'effet
anticancéreux
escompté.
Utilisation clinique
standard
Études précliniques
in vivo
Études en laboratoire
in vitro
Dose 250 à 2250mg/
jour
750mg/kg par jour 2 à 50mM
Dose
relative*
0,15 à 1,0 2 à 45 25 à 1 000
Concentrations de metformine
Figure2. Concentrations de metformine utilisées
dans les études en laboratoire
. Les études cliniques et épidémiologiques utilisent des doses de metformine allant jusqu'à 2250mg/jour. En
revanche, les études in vitro et précliniques in vivo utilisent souvent des concentrations non physiologiques
extrêmement élevées de metformine qui dépassent les niveaux thérapeutiques atteints en toute sécurité chez
les patients humains. Adapté de la référence6.
*Par rapport à l'utilisation clinique standard.
Pratique clinique

DiabetesVoice
Mars 2014 • Volume 59 • Numéro 1 39
Andrew Renehan
Andrew Renehan est professeur d'études
et de chirurgie du cancer su sein de
l'Institute of Cancer Sciences de l'Université
de Manchester, au Royaume-Uni.
Références
1. Renehan AG. Diabetes, diabetes treatment and
cancer risk. Diabetes Voice 2010; 55: 38-40.
2. Johnson JA, Carstensen B, Witte D, et al.
Diabetes and cancer (1): evaluating the temporal
relationship between type 2 diabetes and cancer
incidence. Diabetologia 2012; 55: 1607-18.
3. Renehan AG, Yeh HC, Johnson JA, et al.
Diabetes and cancer (2): evaluating the impact
of diabetes on mortality in patients with
cancer. Diabetologia 2012; 55: 1619-32.
4. Gerstein HC, Bosch J, Dagenais GR, et al. Basal
insulin and cardiovascular and other outcomes
in dysglycemia. N Engl J Med 2012; 367: 319-28.
5. Suissa S, Azoulay L. Metformin and the risk
of cancer: time-related biases in observational
studies. Diabetes Care 2012; 35: 2665-73.
6. Dowling RJ, Niraula S, Stambolic V, et al.
Metformin in cancer: translational challenges.
J Mol Endocrinol 2012; 48: R31-43.
7. Azoulay L, Yin H, Filion KB, et al. The use of
pioglitazone and the risk of bladder cancer
in people with type 2 diabetes: nested case-
control study. BMJ 2012; 344: e3645.
8. Neumann A, Weill A, Ricordeau P, et al.
Pioglitazone and risk of bladder cancer among
diabetic patients in France: a population-based
cohort study. Diabetologia 2012; 55: 1953-62.
9. Lewis JD, Ferrara A, Peng T, et al. Risk of bladder
cancer among diabetic patients treated with
pioglitazone: interim report of a longitudinal
cohort study. Diabetes Care 2011; 34: 916-22.
10. Butler PC, Elashoff M, Elashoff R, et al. A
critical analysis of the clinical use of incretin-
based therapies: are the GLP-1 therapies
safe? Diabetes Care 2013; 36: 2118-25.
récentes analyses actualisées de l'étude de
cohorte du KPNC sur le pioglitazone et le
cancer de la vessie montrent que le risque
disparaît pour l'essentiel lorsqu'un ajuste-
ment pour l'albuminurie est réalisé. D'après
ces nouvelles analyses, le lien établi avec le
cancer de la vessie serait donc dû à un biais
de détection. Des études complémentaires
sont par conséquent clairement requises
pour trancher cette question.
Hypoglycémiants à base d'incrétine
Les hypoglycémiants à base d'incrétine ont
été introduits sur le marché américain en
2005 et ont démontré leur efficacité, que ce
soit en tant qu'agonistes des récepteurs du
GLP-1 (glucagon-like peptide 1) ou qu'in-
hibiteurs de la DPP-4 (dipeptidyl peptidase
4). Des craintes quant aux conséquences
à long terme de l'utilisation de ces traite-
ments en termes de cancer ont toutefois
surgi ces dernières années. Les problèmes
invoqués concernent la capacité de ces
deux classes de médicaments à favoriser
une pancréatite aiguë, puis à induire des
modifications histologiques évoquant une
pancréatite chronique subclinique avec lé-
sions précancéreuses associées (prolifération
canalaire, par exemple), voire, à long terme,
un cancer du pancréas.10 Il pourrait par ai-
lleurs y avoir un risque accru de cancer de la
thyroïde. Ces données sont particulièrement
difficiles à interpréter, et ce pour plusieurs
raisons. D'une part, l'utilisation à long ter-
me d'hypoglycémiants à base d'incrétine
est limitée et, d'autre part, on ignore avec
certitude si les données des modèles animaux
précliniques se traduisent directement par le
développement d'un cancer chez l'homme et
s'il y a eu un ajustement et une modélisation
adéquats afin de prendre en compte les biais
et la confusion expliqués dans les premiers
paragraphes de cet article.
Conclusion
Que signifient donc ces diverses observations
pour la pratique clinique au quotidien ? En ce
qui concerne l'utilisation d'analogues d'insu-
line à action longue, les données sont rassu-
rantes : s'il y a des raisons théoriques (sur la
base d'études en laboratoire) de penser que
ces analogues peuvent accroître le risque de
cancer, cette hausse est toutefois négligeable,
voire nulle, chez les patients. Pour ce qui est
de la metformine, il convient d'encourager
la poursuite de l'étude en laboratoire de ce
médicament en tant qu'agent anticancéreux.
Dans la pratique clinique, la prescription ad
hoc de metformine chez des patients sou-
ffrant d'un cancer mais pas de diabète ne
peut être justifiée ; son utilisation doit être
limitée à des essais prospectifs enregistrés.
En cas de prescription de pioglitazone, le
clinicien doit être attentif aux patients ayant
des antécédents de cancer de la vessie ou
une prédisposition à celui-ci. Pour ce qui est
des hypoglycémiants à base d'incrétine, les
données probantes sont actuellement trop
immatures pour avoir un impact significatif
sur la pratique clinique.
Pratique clinique
1
/
4
100%