Mailing Vimovo Fr.indd

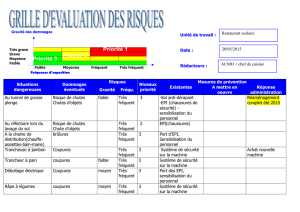
naproxène 500mg
libération retardée
ésomeprazole 20mg
libération immédiate
enrobage gastro-résistant
évite une libération directe de naproxène
dans l'estomac
Nouveau médicament mis sur le marché, remboursé dès le 1ier septembre 2011
VimovoTM est remboursé en catégorie Bf, avec contrôle à priori (M.B. 19.08.2011, ed. 2).
VimovoTM est disponible dans un fl acon de 60 comprimés et se prend par voie orale à raison de
2x1 comprimé par jour, au moins 30 minutes avant le repas.
Si vous désirez recevoir plus d’informations concernant ce produit, n’hésitez pas à contacter Laura
Van Gysegem, Customer Relations Manager, par téléphone 02/370 49 33 ou par mail
Laura.V[email protected], ou bien le département ‘Medical Information’ au numéro
02/370 49 73 ou par mail : [email protected].
Nous espérons avoir pu vous renseigner et restons à votre disposition pour toute autre question.
Veuillez agréer, Madame, Monsieur le pharmacien, l’expression de nos salutations distinguées,
Madame, Monsieur le pharmacien,
AstraZeneca a le plaisir de vous annoncer qu’un nouveau médicament est disponible dès
le 1ier septembre: VimovoTM.
VimovoTM 500 mg/20 mg comprimés à libération modifi ée est une combinaison fi xe d’un
AINS et d’un IPP dans un comprimé.
Ainsi, les patients ont l’assurance de la prise d’IPP à chaque prise de leur anti-infl ammatoire,
l’effi cacité du naproxène leur procurant un puissant effet analgésique et anti-infl ammatoire. VimovoTM
est destiné aux patients souffrant d’arthrose, de polyarthrite rhumatoïde et de spondylarthrite
ankylosante présentant un risque gastro-intestinal.
Prix public :
28,76 €
Ticket modérateur
(actif) :
7,81 €
Ticket modérateur
(VIPO) :
4.65 €
Prix pharmacien :
22,00€
Anne-Laure Dreno
Marketing Manager Vimovo
Marc Tomas
Medical Director

1518-08-2011
[VIMOVO 500/20]
1
INFORMATIONS ESSENTIELLES DENOMINATION DU MEDICAMENT VIMOVO™ 500 mg/20 mg comprimés à libération modifiée COMPOSITION QUALITATIVE ET QUANTITATIVE Chaque comprimé
à libération modifiée contient 500 mg de naproxène et 20 mg d’ésoméprazole (sous forme de sel de magnésium trihydraté). VIMOVO contient des taux très faible
s, non-conservateurs de parahydroxybenzoate
de méthyle (0,02 mg) et de parahydroxybenzoate de propyle (0,01 mg) (voir rubriques ‘Mises en garde spéciales et précautions d’emploi’ et ‘Liste des excipients’)
Pour la liste complète des excipients, voir rubrique
‘Liste des excipients’. FORME PHARMACEUTIQUE Comprimé à libération modifiée contenant du naproxène à enrobage entérique (gastro-résistant) et de l’ésoméprazole pelliculé. C
omprimé ovale, biconvexe,
jaune, marqué « 500/20 » à l’encre noire. DONNEES CLINIQUES Indications thérapeutiques Traitement symptomatique de l’arthrose, de la polyarthrite
rhumatoïde et de la spondylarthrite ankylosante chez les
patients qui risquent de développer des ulcères gastriques et/ou duodénaux associés à la prise d’anti-inflammatoires non stéroï
diens (AINS) et lorsqu’un traitement avec des doses plus faibles de naproxène ou
d’autres AINS n’est pas jugé suffisant. Posologie et mode d'administration Posologie chez l’adulte La posologie est d’1 comprimé (500 mg/20 mg) deux fois par jour.
Les effets indésirables du naproxène
peuvent être limités en utilisant la dose efficace la plus faible pendant la plus courte durée possible (voir rubrique ‘Mises en garde spéciales et précautions d’emploi
’). Chez les patients qui n’étaient pas
préalablement traités par AINS, une dose journalière plus faible de naproxène ou d’autres AINS doit être envisagée. Lorsqu’une
dose journalière totale de 1 000 mg de naproxène n’est pas jugée appropriée, des
alternatives thérapeutiques doivent être utilisées. Le traitement doit être poursuivi afin d’atteindre les objectifs individuels de traitement, réévalué régulièrement et arrê
té en l’absence d’amélioration. En raison de la
libération retardée du naproxène provenant de la formulation à enrobage entérique, VIMOVO n’est pas destiné au traitement de do
uleurs aiguës (telles que douleurs dentaires ou douleurs dues à la goutte).
Cependant, l’inflammation due à l’arthrose, la polyarthrite rhumatoïde et la spondylarthrite ankylosante peut être traitée par VIMOVO. Mode d’administration
VIMOVO doit être avalé en entier avec un verre d’eau.
Les comprimés ne doivent être ni mâchés, ni divisés ou écrasés. Il est recommandé de prendre VIMOVO au moins 30 minutes avant la prise de nourriture (voir rubrique ‘Propriétés pharmacocinétiques’).
Populations spéciales Patients insuffisants rénaux Chez les patients souffrant d’insuffisance rénale légère à modérée, VIMOVO doit être utilisé avec précaution et la fonction rén
ale doit être étroitement surveillée.
Une réduction de la dose journalière totale de naproxène doit être envisagée (voir rubriques ‘Mises en garde spéciales et précautions d’emploi’ et ‘Interactions avec
d’autres médicaments et autres formes
d’interactions’). Quand la dose journalière totale de 1 000 mg de naproxène n’est pas jugée appropriée, des alternatives thérapeutiques doivent être utilisées. VIMOVO est
contre-indiqué chez les patients souffrant
d’insuffisance rénale sévère (clairance de la créatinine < 30 ml/min) car une accumulation des métabolites du naproxène a été o
bservée chez les patients souffrant d’insuffisance rénale sévère et chez les patients
dialysés (voir rubriques ‘Contre-indications’ et ‘Mises en garde spéciales et précautions d’emploi’). Patients insuffisants hépatiques Chez les patients souffrant d’insuffi
sance hépatique légère à modérée, VIMOVO
doit être utilisé avec précaution et la fonction hépatique doit être étroitement surveillée. Une réduction de la dose journaliè
re totale de naproxène doit être envisagée (voir rubriques ‘Mises en garde spéciales et
précautions d’emploi’ et ‘Propriétés pharmacocinétiques’). Quand la dose journalière totale de 1 000 mg de naproxène n’est pas considérée appropriée, des alternat
ives thérapeutiques doivent être
utilisées.VIMOVO est contre indiqué chez les patients souffrant d’insuffisance hépatique sévère car ces patients ne doivent pas recevoir une dose d’ésoméprazole supéri
eure à 20 mg par jour (voir rubriques
‘Contre-indications’ et ‘Propriétés pharmacocinétiques’). Personnes âgées (> 65 ans) Les patients âgés présentent un risque plus élevé de dével
opper des conséquences graves d’effets indésirables (voir
rubriques ‘Mises en garde spéciales et précautions d’emploi’ et ‘Propriétés pharmacocinétiques’). Quand la dose journalière tot
ale de 1 000 mg de naproxène n’est pas jugée appropriée (ex : chez les patients
âgés ayant une insuffisance rénale ou un faible poids corporel), des alternatives thérapeutiques doivent être utilisées. Enfants ( 18 ans)
VIMOVO n’est pas recommandé chez les enfants, en raison du manque
de données de sécurité d’emploi et d’efficacité. Contre-indications -Hypersensibilité connue au naproxène, à l’ésoméprazole, aux dérivés benzimidazolés ou à l’un des excipients. -Antécédents d’asthme,
d’urticaire ou de réactions de type allergique, induits par l’administration d’aspirine ou d’autres AINS (voir rubrique ‘Mises en garde spéciales et précautions d’emploi’) -
Troisième trimestre de la grossesse. (voir
rubrique ‘Fécondité, grossesse et allaitement’) -Insuffisance hépatique sévère (ex. Child-Pugh C)-Insuffisance cardiaque sévère-Insuffisance rénale sévère-
Ulcération peptique active (voir rubrique ‘Mises en
garde spéciales et précautions d’emploi’, hémorragie gastro-intestinale, ulcération et perforation, naproxène)-Hémorragie gastro-intestinale, hémorragie cérébr
o-vasculaire ou autres troubles du saignement (voir
rubrique ‘Mises en garde spéciales et précautions d’emploi’ Effets hématologiques)-VIMOVO ne doit pas être utilisé en concomitance avec l’atazanavir
et le nelfinavir (voir rubriques ‘Mises en garde spéciales et
précautions d’emploi’ et ‘Interactions avec d’autres médicaments et autres formes d’interactions’) Effets indésirables Résumé du profil de sécurité d’emploi L’ésoméprazole à libérati
on immédiate a été inclus
dans une formulation en comprimé pour diminuer l’incidence des événements indésirables gastro-intestinaux du naproxène. VIMOVO a révélé une diminution significative
de la survenue des ulcères gastriques et
des effets indésirables au niveau gastro-intestinal supérieur associés à la prise d’AINS, par comparaison avec la prise de napr
oxène seul (voir rubrique ‘Propriétés pharmacodynamiques’). En comparaison avec
les profils de sécurité d’emploi bien connus des substances actives seules (naproxène et ésoméprazole), aucune donnée supplémentaire de sécurité d’emploi n’a été obse
rvée durant le traitement par VIMOVO
dans la population totale étudiée (n=1157). Résumé tabulé des effets indésirables Les effets indésirables sont classés par fréquence et cla
sse de système d’organe. Les différentes catégories de fréquence sont
définies de la manière suivante : très fréquent (1/10), fréquent (1/100 à < 1/10), peu fréquent ( 1/1 000 à <1/100), rare (
1/10 000 à <1/1000), très rare (< 1/10 000), fréquence indéterminée (ne peut être
estimée sur la base des données disponibles).
VIMOVO Les évènements indésirables indiqués ci-dessous ont été identifiés chez les patients sous traitement VIMOVO lors des études cliniques : -Infections et infestations Peu fréquent infection Rare
diverticulite - Affections hématologiques et du système lymphatique Rare éosinophilie, leucopénie - Affections du système immunitaire Rare réactions d’hypersensibilité
- Affections du métabolisme et
de la nutrition Peu fréquent trouble de l’appétit Rare rétention de fluides, hyperkaliémie, hyperuricémie - Affections psychiatriques Peu fréquent anxiété, dépression, insomnie Rare confusion, rêves
anormaux - Affections du système nerveux Fréquent sensation de vertige, maux de tête, troubles du goût Peu fréquent paresthésie, syncope Rare somnolence, tremblement
- Affections de l’oreille et du
labyrinthe Peu fréquent acouphènes, vertige -Affections cardiaques Peu fréquent arythmie, palpitations Rare infarctus du myocarde, tachycardie - Affections vasculaires Fréquent hypertension -
Affections respiratoires, thoraciques et médiastinales Peu fréquent asthme, bronchospasme, dyspnée - Affections gastro-intestinales Très fréquent dyspepsie Fréquent douleur abdominale,
constipation, diarrhée, oesophagite, flatulence, ulcères gastriques/duodénaux*, gastrite, nausées, vomissement Peu fréquent sécheresse buccale, éructation, saignements gastro-intestinaux, stomatite Rare
glossite, hématémèse, saignement rectal - Affections de la peau et du tissu sous-cutané Fréquent éruptions cutanées Peu fréquent dermatite,hyperhydrose, prurit, urticaire Rare alopécie, ecchymoses -
Affections musculo-squelettiques et systémiques Fréquent arthralgie Peu fréquent myalgie -Affections du rein et des voies urinaires Rare protéinurie, insuffisance rénale
- Affections des organes de
reproduction et du sein Rare troubles menstruels -Troubles généraux et anomalies au site d’administration Fréquent œdème Peu fréquent asthénie, fatigue, pyrexie
-Investigations Peu fréquent
anomalies des tests biologiques hépatiques, augmentation du taux de créatinine *détecté par endoscopie de routine programmée.
Naproxène Les évènements indésirables suivants ont été rapportés chez des patients prenant du naproxène lors des études cliniques et lors de l’utilisation postmarketing.
-Infections et infestations Fréquent
diverticulite Peu fréquent/rare méningite aseptique, infection, sepsis -Affections hémotologiques et du système lymphatique Peu fréquent/rare
agranulocytose, anémie aplastique, éosinophilie,
granulocytopénie, anémie hémolytique, leucopénie, lymphadénopathie, pancytopénie, thrombocytopénie -Affections du système immunitaire Peu fréquent/rare
réactions anaphylactiques, réactions
anaphylactoïdes, réactions d’hypersensibilité -Troubles du métabolisme et de la nutrition Peu fréquent/rare troubles de l’appétit, rétention de fluides, hy
perglycémie, hyperkaliémie, hyperuricémie,
hypoglycémie, modification de poids -Affections psychiatriques Fréquent dépression, insomnie Peu fréquent/rare agitation, anxiété, confusion, rêves anormaux, hallucinations, nervosité -Affections du
système nerveux Fréquent sensation de vertige, envie de dormir, maux de tête, sensation de tête vide, vertige Peu fréquent/rare
dysfonction cognitive, coma, convulsions, incapacité à se concentrer, névrite
optique, paresthésie, syncope, tremblement -Affections oculaires Fréquent troubles visuels Peu fréquent/rare vision trouble, conjonctivite, opacité de la cornée, papilloedème, papillite
-Affections de l’oreille et
du labyrinthe Fréquent acouphènes, troubles de l’audition Peu fréquent/rare diminution de l’audition -Affections cardiaques Fréquent palpitations Peu fréquent/rare
arythmie, insuffisance cardiaque
congestive, infarctus du myocarde, tachycardie -Affections vasculaires Peu fréquent/rare hypertension, hypotension, vascularite -Affections respiratoires, thoraciques et médiastinales Fréquent dyspnée
Peu fréquent/rare asthme, bronchospasme, pneumopathie à éosinophiles, pneumonie, œdème pulmonaire, dépression respiratoire -Affections gastro-intestinales Fréquent dyspepsie, douleurs
abdominales, nausées, vomissements, diarrhée, constipation, pyrosis, ulcères peptiques, stomatite Peu fréquent/rare sécheresse buccale, œsophagite, ulcères gastriques
, gastrite, glossite, éructation, flatulence,
ulcères gastriques/duodénaux, hémorragie et/ou perforation gastro-intestinale, méléna, hématémèse, pancréatite, colite, exacerbation de maladies intestinales inflammatoir
es (colite ulcérative, maladie de Crohn),
ulcération gastro-intestinale non peptique, hémorragie rectale, stomatite ulcérative -Affections hépatobiliaires Peu fréquent/rare cholestase, hépatite, ictère, insuffisance hépatique
-Affections de la peau et
du tissu sous-cutané Fréquent prurit, ecchymoses, purpura, éruptions cutanées Peu fréquent/rare alopécie, exanthème, urticaire, réactions bulleuses
y compris syndrome de Stevens-Johnson et nécrolyse
épidermique toxique, érythème multiforme, érythème noueux, érythème pigmenté fixe, lichen plan, lupus systémique érythémateux,
dermatite photosensible, réactions de photosensibilité, incluant de rare cas
ressemblant à une porphyrie cutanée tardive (pseudo porphyrie) dermatite exfoliante, œdème angioneurotique, réaction pustullaire
-Affections musculo-squelettiques et systémiques Peu fréquent/rare
faiblesse musculaire, myalgie -Affections du rein et des voies urinaires Peu fréquent/rare glomérulonéphrite, hématurie, néphrite interstitielle, syndrome néphrotique, oligurie/polyurie,
protéinurie, insuffisance
rénale, nécrose des papilles rénales, nécrose tubulaire -Affections des organes de reproduction et du sein Peu fréquent/rare infertilité, troubles menstruels
-Affections généraux et du site d’administration
Fréquent fatigue, œdème, transpiration, sensation de soif Peu fréquent/rare asthénie, malaise, pyrexie –Investigations Peu fréquent/rare
anomalies des tests biologiques hépatiques, augmentation du temps
de saignement, augmentation du taux sérique de créatinine.
Esoméprazole Les effets indésirables suivants ont été identifies ou suspectés lors des études cliniques du programme de développement de l’é
soméprazole comprimé gastro-résistant et/ou lors de l’utilisation
postmarketing. Aucun n’est dépendant de la dose. -Affections hématologiques et du système lymphatique Rare leucopénie,thrombocytopénie Très rare agranulocytose,pancytopénie -Affections du
système immunitaire Rare réactions d’hypersensibilité ; par exemple fièvre, angioedème et réaction/choc anaphylactique -Troubles du métabolisme et de la nutrition Peu fréquent œdème périphérique
Rare hyponatrémie Très rare hypomagnésémie -Affections psychiatriques Peu fréquent insomnie Rare agitation,confusion, dépression Très rare agression,hallucinations
-Affections du système nerveux
Fréquent maux de tête Peu fréquent sensation de vertige,paresthésie,somnolence Rare troubles du goût -Affections oculaires Rare vision trouble
-Affections de l’oreille et du labyrinthe Peu fréquent
vertig -Affections respiratoires, thoraciques et médiastinales Rare bronchospasme -Affections gastro-intestinales Fréquent douleur abdominale,diarrhée,flatulenc
e,nausées/vomissement,constipation
Peu fréquent sécheresse buccale Rare stomatite, candidose gastrointestinal -Affections hépatobiliaires Peu fréquent augmentation des enzymes hépatiques Rare hépatite avec ou sans ictère Très rare
insuffisance hépatique,encéphalopathie hépatique chez les patients avec une maladie du foie préexistante. -Affections de la peau et du tissu sous-cutané Peu fréquent
dermatite, prurit,urticaire, éruption
cutanée Rare alopécie, photosensibilité Très rare érythème multiforme,syndrome de Stevens-Johnson,nécrolyse toxique épidermique, nécrolyse toxique épidermique
-Affections musculo-squelettiques et
systémiques Rare arthralgie, myalgie Très rare faiblesse musculaire -Affections du rein et des voies urinaires Très rare néphrite interstitielle
-Affections des fonctions reproductives et du sein Très rare
gynécomastie -Troubles généraux et anomalies au site d’administration Rare malaise, augmentation de la sudation
Description de certains effets indésirables Naproxène Les données d’études cliniques et épidémiologiques suggèrent que l’utilisation de coxibs et de certainsAINS (en particulier à d
es doses élevées et lors de
traitement à long terme) peut être associée à une légère augmentation du risque d’événements thrombo-artériels (par exemple inf
arctus du myocarde ou AVC). Bien que les données suggèrent que l’utilisation du
naproxène (1 000 mg par jour) peut être associée à un risque plus faible, le risque ne peut pas être exclu (voir rubrique ‘Mises en garde spéciales et précautions d’emploi’).
Œdème, hypertension et insuffisance
cardiaque ont été rapportés lors de traitement avec des AINS. Les effets indésirables les plus communément observés sont de nature gastro-intestinale. Des ulcères peptiques, une perforation ou des
saignements gastro-intestinaux parfois fatals, tout particulièrement chez les personnes âgées peuvent se produire (voir rubriqu
e ‘Mises en garde spéciales et précautions d’emploi’). Nausée, vomissement,
diarrhée, flatulence, constipation, dyspepsie, douleur abdominale, méléna, hématémèse, stomatite ulcérative, exacerbation de colites et maladie de Crohn (voir rubrique
‘Mises en garde spéciales et précautions
d’emploi’ Mises en garde spéciales et précautions d’emploi) ont été rapportés suite à une administration de naproxène. Des gastrites ont été moins fréquemment observées.
VIMOVO a été développé avec
l’ésoméprazole pour diminuer l’incidence des effets indésirables gastro-intestinaux du naproxène et a montré une diminution significative de l’apparition d’ulcères gastriques
et/ou duodénaux et d’effets indésirables
au niveau gastro-intestinal supérieur associés aux AINS par comparaison avec du naproxène seul.
TITULAIRE DE L’AUTORISATION DE MISE SUR LE MARCHE NV AstraZeneca SARue Egide Van Ophem 110 B-1180 Bruxelles Tel: +32(0)2/370 48 11
NUMERO(S) D’AUTORISATION DE MISE SUR
LE MARCHE Flacon : BE382496 Plaquettes thermoformées : BE382505 STATUT LEGAL DE DELIVRANCE Médicament soumis à prescription médicale. DATE DE MISE A JOUR DU
TEXTE/APPROBATION DU TEXTE 12/2010 – 12/2010
1
/
2
100%