1 Quand la physiopathologie est confirmée par les grandes études

1
Quand la physiopathologie est confirmée par les grandes études statistiques et
toutes les deux sont corroborées par l’impression et l’intuition cliniques, il s’agit d’un
grand moment pour la pensée médicale et c’est ce qui se passe en ce qui concerne
le traitement de l’insuffisance cardiaque. Ce que dit la physiopathologie, c’est que la
défaillance du muscle cardiaque active des mécanismes compensateurs
neurohormonaux, bénéfiques dans un premier temps car elles permettent
d’augmenter le débit cardiaque ; mais ils sont vite dépassés et devient délétères ; le
système rénine-angiotensine secrète l’angiotensine responsable d’une
vasoconstriction et de la sécrétion de l’aldostérone, laquelle, à son tour, entraîne une
rétention hydro-sodée et une fibrose myocardique. Quant à l’activation du système
adrénergique, bénéfique à ses débuts car augmentant le débit cardiaque, elle
devient vite délétère par épuisement des récepteurs bêta adrénergiques et seul
persiste alors leur effet vasoconstricteur.
De plus, cette activation adrénergique est responsable d’un effet arythmogène.
Ces mécanismes apparaissent très vite comme un « ami qui vous veut du bien » plus
néfaste que bénéfique, et le but du traitement est de les neutraliser en bloquant le
système rénine-angiotensine par les IEC et les sartans, le système adrénergique par
les bêtabloquants et l’aldostérone par les anti-aldostérones. Ces trois familles (IEC-
AAII, bêtabloquants et anti-aldostérones) ont été longtemps, les seules qui ont pu
montrer un bénéfice dans de grandes études de morbi-mortalité, et sont la base du
traitement de l’insuffisance cardiaque. L’Ivabradine vient de rejoindre ce club très
fermé après l’étude SHIFT. Les diurétiques de l’anse soulagent d’une façon
spectaculaire les symptômes mais n’ont pas d’effet démontré sur la mortalité. La
digoxine réduit les hospitalisations mais n’a pas d’effet non plus sur la mortalité. Le
traitement de l’insuffisance cardiaque à fonction systolique altérée est actuellement
bien codifié et pourtant, il a fallu quelques décennies pour montrer ce qui parait
évident aujourd’hui. Dans les années 70, la culture du cathétérisme a mis au premier
plan l’altération de la contractilité ventriculaire et la réduction de la FEVG, et il
semblait évident à l’époque que la recherche devait s’orienter vers le développement
de molécules inotropes positives capables d’améliorer la contractilité ventriculaire ;
mais très vite on s’est rendu compte que la stimulation d’un myocarde défaillant
pouvait être néfaste et on a évolué vers un nouveau paradigme consistant à
neutraliser ces mécanismes neurohormonaux.
Avant de développer ces six familles qui sont la base du traitement de l’insuffisance
cardiaque, nous débuterons par une mise au point sur la place des autres
thérapeutiques cardio-vasculaires dans le traitement de l’insuffisance cardiaque :
Les nitrés : n’ont pas montré de bénéfice en terme de morbi-mortalité et n’ont
de place qu’en désespoir de cause en cas de persistance de symptômes
malgré un traitement maximal. Ils ont une action sur la réduction de la pré
charge et la réduction de l’insuffisance mitrale. Il est conseillé de faire une
fenêtre thérapeutique de 8 heures pour éviter les échappements
thérapeutiques sous nitrés et de leur préférer la molsidomine pour cette
raison.
TRAITEMENT DE L’INSUFFISANCE CARDIAQUE SYSTOLIQUE

2
Les inhibiteurs calciques n’ont pas de place dans le traitement de
l’insuffisance cardiaque. S’il faut les prescrire pour une autre cause (HTA ou
ischémie) il faut choisir un dihydropyridinique. Le diltiazem peut être associé
sous surveillance et le vérapamil est contre-indiqué en cas d’insuffisance
cardiaque.
Les antiarythmiques : seule l’amiodarone est autorisée. La dronédarone et
les antiarythmiques de la classe I sont tous contre-indiqués. L’amiodarone
trouve sa place en cas de troubles de rythme supraventricualires (FA, Flutter)
ou en cas de TV non soutenue ou déclenchable lors d’une exploration
électrophysiologique. En cas d’une TV soutenue, il faut discuter l’implantation
d’un défibrillateur et en cas d’extrasystolie ventriculaire isolée, opter pour
l’abstention thérapeutique car les ESV sont souvent présentes dans
l’insuffisance cardiaque.
Les antithrombotiques : malgré les différents facteurs responsables d’une
activation de la coagulation en cas d’une insuffisance cardiaque, le taux des
accidents thromboemboliques reste faible, de l’ordre de 2 à 3 %. A cet égard
les antivitamines K ne sont indiquées dans l’insuffisance cardiaque qu’en cas
de fibrillation auriculaire. L’aspirine n’est indiquée qu’en cas de cardiopathie
ischémique associée, et les HBPM ne trouvent leur place qu’au cours de la
poussée aiguë et de l’alitement prolongé, surtout lorsqu’il existe un mauvais
état veineux.
La vaccination : l’insuffisant cardiaque est très sensible aux infections
bronchiques et aux épisodes grippaux qui peuvent être une source de
décompensation et parfois d’issue fatale. Il est fortement recommandé de
pratiquer la vaccination grippale et il est conseillé de faire la vaccination
antipneumococcique et anti-Haemophilus. Une couverture antibiotique par
amoxicilline ou érythromycine en cas d’atteinte bronchique ou de
pneumopathie est indiquée.
Attention aux médicaments suivants :
Vasoconstricteurs nasaux
Bêtabloquants oculaires (timoptol).
Les bêtabloquants prescrits à dose pleine hors protocole de titration
Anti-inflammatoires non stéroïdiens et coxibs : surtout si IEC.
Corticoïdes pouvant occasionner une rétention hydrosodée
Glitazones : rétention hydrosodée.
Verapamil contre-indiqué et prudence avec le diltiazem.
Tous les antiarythmiques sont contre-indiqués sauf l’amiodarone.
Les antidépresseurs tricycliques et le lithium majorent le risque
rythmique.
Le sildénafil ne doit pas être prescrit si la TA est basse < 100 mmhg
ou en cas d’association à des nitrés.

3
Le traitement médicamenteux de l’insuffisance cardiaque
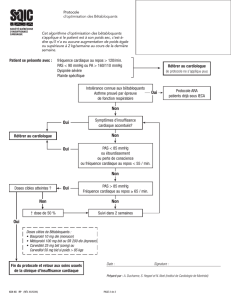
La première étape consiste à évaluer la fraction d’éjection pour distinguer :
o L’insuffisance cardiaque à fonction systolique altérée avec une FEVG < à 45 %
et dont le traitement est actuellement bien codifié avec un haut niveau de preuve,
o De l’insuffisance cardiaque à F.E préservée (FEVG > 45 %) et dont le traitement
est moins bien connu.
Le traitement de l’insuffisance cardiaque à fonction systolique altérée (FEVG < 45
%) fait appel :
o A trois familles (IEC-AAII, bêtabloquants et anti-aldostérone) qui ont montré,
toutes les trois, leur bénéfice en terme de morbi-mortalité
o Et à deux familles (les diurétiques de l’anse et la digoxine) qui ont montré un
bénéfice sur la dyspnée et le nombre d’hospitalisations.
o Et à un nouveau, l’Ivabradine, qui figurera sûrement dans les prochaines
recommandations.
Les inhibiteurs de l’enzyme de conversion :
Les IEC sont sûrement les médicaments qui ont été le plus étudiés et en ce qui
concerne l’insuffisance cardiaque, il existe un nombre important d’études qui
convergent toutes pour montrer une réduction de la mortalité de 20 à 30% au stade II
et III (NYHA) et 40 % au stade IV (NYHA). Neuf IEC possèdent une AMM dans
l’insuffisance cardiaque :
Enalapril : trois études aux différents stades de l’insuffisance cardiaque SOLVD
Prévention (classe NYHA I), SOLVD traitement (classe NYHA II et III),
CONSENSUS (classe IV). Quant à l’étude V-HEFT II, elle a montré la supériorité
de l’enalapril en terme de mortalité par rapport à l’association hydralazine-
trinitrine. Cette dernière association ayant déjà montré une baisse de la mortalité
comparée au placebo dans l’étude V-HEFT I chez des patients en classe II ou III
de la NYHA.
Trois études dans le post IDM avec insuffisance cardiaque : captopril (SAVE),
ramipril (étude AIRE), trandolapril (étude TRACE).
Les autres IEC qui ont une AMM dans l’insuffisance cardiaque sont le fosinopril,
le quinapril, le perindopril et le cilazapril.
Les IEC sont donc efficaces dans le traitement de l’insuffisance cardiaque mais à
quelle dose ? La réponse nous a été donné par l’étude ATLAS (lisinopril 35 mg/5mg)
qui a montré l’intérêt de fortes doses de lisinopril en comparant des doses faibles à 5
mg à des fortes doses à 35 mg.
Les règles de prescription des IEC : les IEC sont indiqués à tous les stades de la
NYHA et sont les seuls à prescrire dès la classe I c-à-d en cas de découverte d’une
dysfonction V.G avec une FEVG < 45 % asymptomatique. Ils doivent être prescrits à
la dose maximale requise dans l’HTA. Chez les personnes âgées où en cas d’une TA
basse, il faut débuter par la dose minimale et à distance d’une déplétion hydro-sodée
et cibler la dose maximale requise par paliers successifs, avec une surveillance de
l’ionogramme et de la créatinine avant et 15 jours après chaque modification
thérapeutique.

4
Les contre indication sont :
Sténose bilatérale des artères rénales.
Hypotension < 90 mmHg.
Hyperkaliémie > 5.5 mmol/l.
Insuffisance terminale (clairance de la créatinine <15 ml/mn).
Les effets indésirables sont :
Une toux sèche : remplacer l’IEC par un ARA II mais après avoir éliminé une
décompensation cardiaque.
Un prurit, un œdème de Quincke : il est parfois difficile de faire le lien avec
l’IEC mais si le tableau clinique est important et dans le doute, les IEC seront
arrêtés.
Une altération du goût : remplacer l’IEC par un IEC d’une autre famille ou par
un ARA II.
Des céphalées qui sont rares.
Les antagonistes des récepteurs de l’angiotensine II (ARA II).
Deux sartans ont une efficacité prouvée dans l’insuffisance cardiaque :
Le valsartan avec l’étude Val-HeFT
et le candesartan avec l’étude CHARM-Alternative qui a fait aussi bien que
l’énalapril dans SOLVD en montrant une réduction de 23 % des décès et des
hospitalisations mais en utilisant de fortes doses, ciblant 32 mg.
Seul le candesartan possède l’AMM dans l’insuffisance cardiaque ; il faut débuter
avec des doses de 4 à 8 mg en respectant les mêmes précautions décrites dans le
cas des IEC, et cibler une dose de 32 mg par paliers de 4 à 8 mg tous les 15 jours.
Deux questions peuvent légitimement être posées :
Faut-il prescrire les ARA II à la place des IEC ?
Si théoriquement les ARA II ont été présentés comme mieux placés que les IEC pour
bloquer le système rénine-angiotensine, les études n’ont pas confirmé leur
supériorité. En plus, les IEC se targuent dans ces indications d’un nombre imposant
d’études comme on vient de le voir. Mieux encore dans l’étude ELITE II il y a eu
moins de mortalité dans le groupe captopril 150 mg que dans le groupe losartan à 50
mg. Des résultats identiques ont été obtenus dans OPTIMAAL (losartan versus
captopril) et dans VALLIANT (valsartan versus captopril dans l’insuffisance cardiaque
post IDM). En pratique, les ARA II ne sont indiqués qu’en cas d’effet secondaire sous
IEC (toux).
Faut-il ajouter un ARA II à un IEC ? Val-HeFT a montré une baisse de 27 % des
hospitalisations sans amélioration de la survie. En revanche dans CHARM-Added le
candesartan diminue de 15 % le risque combiné de décès et d’hospitalisation. En
pratique, le candesartan peut être associé chez un patient qui reste symptomatique
sous IEC, bêtabloquants et diurétiques de l’anse. A ce stade le choix se fait
théoriquement entre ARA II et spironolactone. Cette dernière étant préférée en cas
d’OMI. Mais dans la pratique, il est rare de voir une association IEC-ARA II dans

5
l’insuffisance cardiaque et la place est laissée aux anti-aldostérones. Dans tous les
cas il faut impérativement éviter l’association bêtabloquant-IEC-ARAII-anti-
aldostérone.
Les bêtabloquants :
Selon le même principe du blocage des systèmes neurohormonaux, les
bêtabloquants trouvent une place privilégiée dans le traitement de l’insuffisance
cardiaque à fonction systolique diminuée. C’est le programme US Carvedilol, publié
en 1996 et comportant quatre études, qui a créé la surprise en montrant une
réduction de la mortalité totale de 65 % et des hospitalisations de 27 %, sous
carvédilol, chez des patients NYHA II ou III ayant une FEVG< 40 %. Devant
l’ampleur d’un tel résultat, des doutes ont été émis par certains sceptiques sur la
méthodologie de ce travail mais la preuve a définitivement été établit grâce à deux
études publiées en 1999 et s’adressant au même profil de patients : l’étude CIBIS II
qui a réduit la mortalité totale de 34 % sous bisoprolol et l’étude MERIT-HF qui a
réduit la mortalité totale de 34 % et la mort subite de 45 % sous succinate de
métoprolol. La place des bêtabloquants a été bien établie dans l’insuffisance
cardiaque avec une FEVG < 40 % et en stade II ou III de la NYHA mais il restait à
savoir si cette indication peut s’adresser à des patients plus graves en stade IV de la
NYHA avec une FEVG < 25 %. Ce que va prouver l’essai COPERNICUS qui sera
interrompue prématurément au bout de 10.4 mois suite à la constatation d’une
réduction de 35 % de la mortalité dans le groupe carvédilol.
Une question s’est rapidement posée : s’agit-il d’un effet de classe, ou bien cet effet
est-il spécifique à certains bêtabloquants ? La réponse a été donnée par l’étude
COMET qui a comparé le carvédilol au metoprolol tartrate [Lopressor®, Seloken®)
(qu’il ne faut pas confondre avec le metoprolol succinate)], ce dernier s’est révélé
inférieur. Il faut se limiter, donc, aux bêtabloquants qui ont fait l’objet de ces études.
Quatre bêtabloquants possèdent l’AMM dans cette indication. Ce sont :
Le carvédilol (Kredex®) avec l’étude COPERNICUS et le US programme et
dans le post infarctus avec l’étude CAPRICORN.
Le bisoprolol (Detensiel®) avec les études CIBIS I et II.
Le metoprolol succinate (Selozoc®) avec l’étude MERIT-HF.
Le nébivolol (Temerit®, Nébilox®) avec l’étude SENIORS qui est la seule
étude qui s’est adressée à des patients de plus de 70 ans. Cette étude a
montré une baisse de la mortalité globale et des hospitalisations d’origine
cardiovasculaire de 14 % sous nébivolol. Ce résultat est moins brillant qu’avec
les autres bêtabloquants étudiés dans cette indication mais il faut reconnaître
que les patients dans SENIORS sont moins sévères que dans les essais
précédents (la FEVG a été > 35 % dans un tiers des cas). Le nébivolol est le
seul bêtabloquant qui a une AMM chez le sujet âgé.
Comme les IEC, les bêtabloquants ont montré une baisse de la mortalité aussi
importante de l’ordre de 30 à 35 %, une amélioration de la fonction systolique et du
débit cardiaque, une limitation du remodelage ventriculaire et ils s’accompagnent
d’une amélioration fonctionnelle. Cette amélioration fonctionnelle n’intervient que 2 à
3 mois après leur instauration. Pendant ce laps de temps, il peut même il y avoir une
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
1
/
14
100%