htap - VD version corrigée

Hypertension Artérielle
Pulmonaire
Lucie Marry
Marie Christine Gronnier
Anne-Marie Nardy

Épidémiologie HTAP (1)
⦿Primitive : prévalence 15 cas / million
d’habitants
Médiane de survie : 2 à 3 ans / diagnostic
PAPm entre 50 et 60 mmHg
⦿Secondaire :
▪10% des patients atteints de sclérodermies
▪1 personne sur 10000 / prise anorexigènes
▪0,5% des VIH
▪50 % des BPCO > 50 ans (40 mmHg)
▪Cardiopathie – SAS, etc.
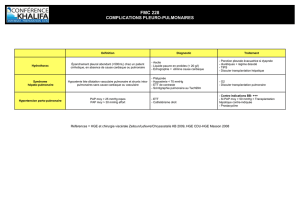
!"#$%&'(%)*(+,-,.$)*/0(+12+3*4%&,(+"0.56$(+(.+75,"0#5*%(

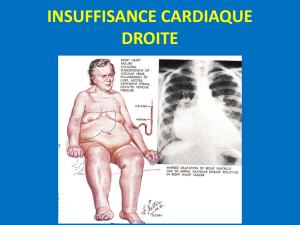
Épidémiologie HTAP (2)
⦿L’IVD a la même incidence que l’IVG : "
1 personne sur 20
⦿La mortalité péri opératoire : 7%
➔ d’où l’importance du diagnostic
préopératoire.
8-,3&6".*&6+7(6.%*"0#5*%(+950":(+;+<=>+'?@ABC+D&0%+EFG+,-,.&#*/0(+,$7H%(+(.+I=>+D&0%+EFG+'*5,.&#*/0(+,$7H%(

Définition hémodynamique
HTP : PAPm ≥ 25 mmHg au repos
(cathétérisme droit)
›PAP occluse ≤ 15 mmHg : HTP pré capillaire
›PAP occluse > 15 mmHg : HTP post capillaire
PAPm normale de l’ordre de 14,3 ± 3,3 mmHg

 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
 26
26
 27
27
 28
28
 29
29
 30
30
 31
31
 32
32
 33
33
 34
34
 35
35
 36
36
1
/
36
100%