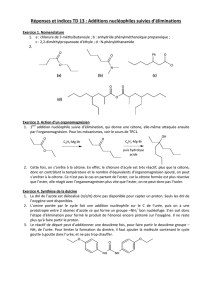
réduction énantiosélective de cétones en alcools

LiebersensDonovan
1ère Master Chimie
Synthèse asymétrique : réduction
énantiosélective de cétones en alcools : réaction
de Corey-Itsuno.
1. Définition
La synthèse asymétrique consiste à préparer un produit sous forme
d’énantiomère à partir d’un composé achiral comportant un centre pro-chiral
(souvent cétone ou alcène asymétriques). Une méthode classique pour réaliser
une synthèse asymétrique est de lier temporairement le composé achiral à un
catalyseur qui lui est chiral.
Dans le cas de la réaction de Corey-Itsuno, la cétone pro-chirale se lie à un
catalyseur chiral le temps d’être réduite en alcool.
2. Présentation
Cette réaction est aussi connue sous le nom de réduction de Corey-Bakshi-
Shibata (CBS).
Le catalyseur utilisé est une oxazaborolidine appelé également catalyseur CBS.
Celle-ci est un (bi)hétérocycle à face concave est convexe, présenté ci-dessous.
Figure 1 : les oxazaborolidnes ou catalyseur CBS utilisé pour réduire énantio-
sélectivement une cétone pro-chirale en alcools

Cette réaction se fait entre une cétone achirale et un agent réducteur achiral
(BH3) en présence d’un catalyseur chiral énantiomériquement pur (en faible
quantité car il est très cher).
3. Principe
Cette réaction est énantiosélective car BH3 ne réagit que très faiblement avec
une cétone ayant une face prochirale (susceptible de devenir chirale) de type
Rgros-C(=O)- Rpetit en l’absence du catalyseur.
Tandis que si celui-ci est présent, il forme un complexe acide de Lewis/base de
Lewis ce qui augmente le caractère électrophile du carbone de la fonction
carbonyle de la cétone. Cela facilitera la réduction, elle sera plus rapide.
Le site acide de Lewis est représenté en vert et le site base de Lewis est en
rouge.
Figure 2 : réaction CBS ; complexe substrat-catalyseur et substrat-catalyseur-
hydrure de bore
Un Rgros peut être soit un aryle tel que le phényle, ou encore le TMS ; dans le cas
ou la cétone est non cyclique.
Si celle-ci est cyclique insaturée, elle peut comporter une chaine alkyle sur la
double liaison ou alors un halogène.
Le catalyseur, qui est une oxazaborolidine, peut se comporter comme une base
de Lewis lorsqu’il est lié à la cétone. En effet, le catalyseur se lie à la cétone par
le bore. Le doublet de l’azote n’est donc plus accaparé par le celui-ci qui a atteint
l’octet. Cette paire d’électrons peut alors servir à former une liaison avec un

acide de Lewis tel que BH3.
Ces liaisons peuvent aussi se faire dans l’autre ordre : d’abord la liaison acide de
Lewis/ N puis la liaison Cétone/B (voir remarques)
Les deux réactifs se trouvent ainsi au voisinage l’un de l’autre, fixés pas le
catalyseur. Cela permet une transformation quasi intramoléculaire de la cétone
avec le réducteur. Elle se déroule stéréosélectivement. L’hétérocycle qui est
bicyclique à face concave et convexe fera les liaisons sur sa fasse convexe qui
est plus facilement accessible.
Le substituant phényle sur la face convexe permet d’orienter l’axe de la liaison
carbonyle de la cétone coordinée de manière à ce qu’elle s’éloigne de lui.
Tandis que le groupe méthyle sur l’atome de bore permet d’orienter les chaines
alkyles de la cétone.
En effet, de part l’orientation de son axe, il parvient à ce que la grande chaîne
alkylée l’évite.
Notons que le catalyseur peut être régénéré selon deux voix : selon le chemin 1
ou 2 (Figure 2).
Figure 3 : mécanisme de la réaction CBS et intermédiaires de réaction

Remarques :
•Cette réaction doit se faire en milieu anhydre car il a était prouvé que l’eau
avait une influence sur l’énantiomère préférentiellement formé. On travail
donc en milieu THF.
•La raison pour laquelle il faut une grande chaine alkylée et une petite est :
L’orientation de la cétone par le groupement méthyle dans le cas de la
figure 1 se fera par encombrement stérique. Au plus la chaine sera grande,
au plus l’effet stérique sera important et donc moins grande sera la
probabilité de former le produit avec le méthyle en face de la grande
chaine alkylée.
•Notons également qu’en général les ressources bibliographiques proposent
d’abord la liaison du réducteur sur le catalyseur et ensuite seulement la
cétone.
•Cette réaction propose un avantage majeur qui est celui du faible coût du
BH3. Mais elle ne marche cependant pas pour n’importe quelles cétones
(Rgrand et Rpetit).
4. Autres exemples de réaction
Figure 4 : un exemple de réaction

5. Influence des chaines alkyles de la cétone
Dans ce tableau nous pouvons remarquer clairement l’importance d’avoir un
grand groupe d’un des deux cotés de la cétone dans l’excès énantiomérique (ee).
On remarque que le pourcentage d’un des énantiomères formé en majorité
augmentent avec la grandeur de ce grand groupe. Le tert-butyle est plus
encombrant que le phényle et on voit donc que l’ee est plus grande.
Entre le deuxième et le troisième exemple l’ee diminue cela est du à
l’encombrement engendré par le clore.
 6
6
1
/
6
100%