8 journee oncodig paca depistage cancer et endoscopie.pptx

8ièmes journées de cancérologie digestive
PACA-CORSE
Dr. P. GRANDVAL Hôpital de la Timone

Particularités de l’endoscopie dans le dépistage
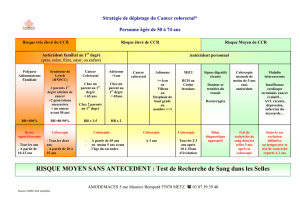
Niveau de risque des patients
Conditions de réalisations des examens
○ Matériels
○ Techniques
○ Modalités: âge, rythme?
couts efficacité? complications?
Cancers digestifs accessibles à un dépistage et
une surveillance
– Cancer colo rectal
– Cancer de l’œsophage:
• Adénocarcinome (EBO) et Carcinome épidermoïde (alcool/
tabac)

CCR: situations à risque moyen
Population générale:
Symptômes digestifs isolés
○ Après 50 ans
○ Avant 50 ans en l’absence de réponse au
traitement
Rectorragies
○ Chroniques quelque soit l'âge
○ Isolées rouge vif après 50 ans
Endocardite (streptococcus bovis)
HAS. Recommandations Avril 2004

CCR: situations à risque élevé
ATCD personnel d’adénome ou de CCR
CCR < 60 ans au 1er degré ou plusieurs
apparentés avec CCR ou adénome avancé
MICI
Acromégalie

CCR: situations à risque très élevé
Polypose adenomateuse familiale
Syndrome de Lynch
Polyposes hamartomateuses:
Syndrome de Peutz-Jeghers
Polypose juvénile
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
 26
26
1
/
26
100%