Physiologie de la jonction neuromusculaire: présentation

PHYSIOLOGIE DE LA JONCTION
PHYSIOLOGIE DE LA JONCTION
NEUROMUSCULAIRE
NEUROMUSCULAIRE
G. ROUX
G. ROUX
Anesth
Anesthé
ésie Neurochirurgie
sie Neurochirurgie
CHU Bordeaux
CHU Bordeaux

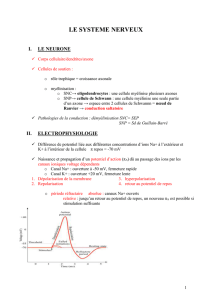
INTRODUCTION
INTRODUCTION
La jonction neuromusculaire:
La jonction neuromusculaire: permet la transformation
permet la transformation
d
d’
’une stimulation nerveuse (influx
une stimulation nerveuse (influx é
électrique) en une
lectrique) en une
activit
activité
ém
mé
écanique (contraction musculaire)
canique (contraction musculaire)
Terminaison nerveuse
Terminaison nerveuse
Espace synaptique
Espace synaptique
Plaque motrice
Plaque motrice
Transmission neuromusculaire
Transmission neuromusculaire : lib
: libé
ération
ration
d
d’
’ac
acé
étylcholine (Ach) => propagation du potentiel d
tylcholine (Ach) => propagation du potentiel d’
’action
action
=> contraction musculaire
=> contraction musculaire

RAPPELS ANATOMIQUES
RAPPELS ANATOMIQUES
Le nerf
Le nerf
Motoneurone issu du SNC (corne ant
Motoneurone issu du SNC (corne anté
érieure de la moelle
rieure de la moelle é
épini
piniè
ère ou
re ou
cerveau) :
cerveau) :
corps cellulaire
corps cellulaire : noyau, centre d
: noyau, centre d’
’activit
activité
ém
mé
étabolique et chimique
tabolique et chimique
dendrites
dendrites : permettent de recevoir l
: permettent de recevoir l’
’information
information
axone
axone : assure la liaison avec les fibres musculaires (gaine de
: assure la liaison avec les fibres musculaires (gaine de
my
myé
éline issue des cellules de Schwann et n
line issue des cellules de Schwann et nœ
œuds de Ranvier
uds de Ranvier
permettent une transmission plus rapide de l
permettent une transmission plus rapide de l’
’influx)
influx)
Synapse
Synapse: situ
: situé
ée au niveau terminal de l
e au niveau terminal de l’
’axone
axone
unit
unité
émotrice
motrice = axone + fibres musculaires
= axone + fibres musculaires


RAPPELS ANATOMIQUES
RAPPELS ANATOMIQUES
La jonction neuromusculaire
La jonction neuromusculaire
Absence de gaine de my
Absence de gaine de myé
éline
line
Plaque motrice
Plaque motrice:
:portion de la fibre musculaire associ
portion de la fibre musculaire associé
ée
e à
àune
une
synapse
synapse
Fente synaptique
Fente synaptique: espace situ
: espace situé
éentre nerf et cellule musculaire
entre nerf et cellule musculaire
Pr
Pré
ésence de
sence de v
vé
ésicules synaptiques
sicules synaptiques:
: ac
acé
étylcholine
tylcholine (
(glycine,
glycine,
GABA, s
GABA, sé
érotonine
rotonine)
)
Transmission neuromusculaire sous la d
Transmission neuromusculaire sous la dé
épendance des
pendance des
r
ré
écepteurs cholinergiques
cepteurs cholinergiques
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
 26
26
 27
27
 28
28
 29
29
 30
30
 31
31
 32
32
 33
33
 34
34
 35
35
 36
36
 37
37
 38
38
 39
39
 40
40
 41
41
 42
42
 43
43
 44
44
 45
45
 46
46
1
/
46
100%