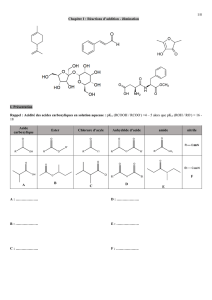
Dérivés d'acides carboxyliques : Transformations et synthèse
Telechargé par
Lotfi Hammami

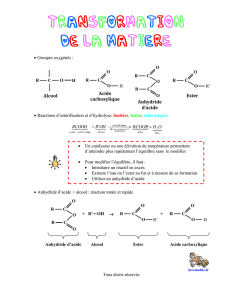
Passage entre les dérivés
des acides carboxyliques

Obtention d’esters, d’amides et
d’anhydrides à partir des chlorures
d’acyle
Objectifs
Obtention d’esters, d’amides à partir
d’anhydrides

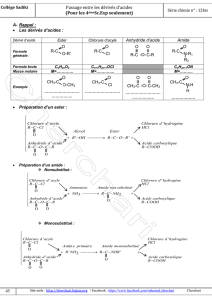
I- Passage à partir de chlorure
d’acyle
1°) Obtention d’amide
a- Formule générale d’un chlorure d’acyle
Le chlorure d’acyle a pour formule générale
O
Cl
CR-
RCOCl

b- Nomenclature
Le nom du chlorure d’acyle s’obtient par
suppression du mot « acide » du nom de
l’acide carboxylique correspondant que l’on
remplace par le mot « chlorure de » et par
remplacement de terminaison « oïque » par
« oyle »
O
Cl
C
CH3-CH3-CH-
CH3
O
Cl
C
Chlorure
d’éthanoyle
Chloure de 2-
méthylpropanoyle
Exemple

c- Obtention d’amide
Equations chimiques à considérer
Equation bilan de la réaction
RCOCl + 2 R’NH2RCONHR’+ R’NH3Cl(sd)
O
Cl
C
R-+ HN –R’
l
H
O
NH-R’
C
R-+ HCl
+ HCl + R’NH2+ R’NH3Cl
Un chlorure d'acyle R-CO-Cl réagit avec une
amine primaire ou secondaire, et donne un
amide selon une réaction rapide et totale.
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
1
/
20
100%