CDF 602

Journal Médical Libanais 2012 •
Volume 60 (2)
65
AARRTTIICCLLEEOORRIIGGIINNAALL//OORRIIGGIINNAALLAARRTTIICCLLEE
TRAITEMENT PERCUTANÉ DE L’ATRÉSIE PULMONAIRE À SEPTUM
INTERVENTRICULAIRE INTACT
http://www.lebanesemedicaljournal.org/articles/60-2/Original1pdf
Ghassan CHEHAB1, Elie CHALOUHI1, Sabine NAJARIAN1, Antoine SARKIS2, Georges BADAOUI2
Linda DAOU1, Issam EL-RASSI1,2, Tony ABDEL MASSIH2, Zakhia SALIBA1
INTRODUCTION
L’atrésie pulmonaire à septum interventriculaire intact
(APSI) est une cardiopathie complexe, très grave et rare :
1 à 3% des cardiopathies congénitales, avec une incidence
de 4,5 cas pour 100 000 naissances [1-2]. Elle est marquée
par une morphologie très variable du ventricule droit
(VD), des valves pulmonaires et tricuspides et des artères
coronaires. La stratégie thérapeutique dépend du dévelop-
pement initial du VD (uni-, bi- ou tripartite) et de l’état
de la circulation coronaire (présence de sinusoïdes avec
une circulation coronaire VD dépendante). Si la répara-
tion chirurgicale est restée pendant longtemps le premier
choix, avec pourtant un taux de morbidité et de mortalité
non négligeable [3], la solution percutanée regagne de la
Chehab G, Chalouhi E, Najarian S, Sarkis A, Badaoui G, Daou L,
El-Rassi I, Abdel Massih T, Saliba Z. Traitement percutané de
l’atrésie pulmonaire à septum interventriculaire intact. J Med
Liban 2012 ; 60 (2) : 65-69.
From CHU Hôtel-Dieu de France, Beirut, Lebanon; Depart-
ments of 1Pediatrics, 2Cardiology and Cardiothoracic Surgery.
Correspondence to: Ghassan Chehab, MD. CHU Hôtel-Dieu
de France Hospital. Pediatric Department. Naccache Blvd.
PO Box 166830. Beirut. Lebanon.
e-mail: [email protected]
RÉSUMÉ • OBJECTIF : Décrire la réparation percuta-
née de l’atrésie pulmonaire à septum interventriculaire
intact (APSI) par une technique mécanique avec ou
sans mise de stent dans le canal artériel ainsi que les
résultats à moyen terme.
MATÉRIEL ET MÉTHODE : Toute APSI favorable à la
réparation biventriculaire a bénéficié à partir de 2007
d’une tentative de perforation-dilatation percutanée et
a été incluse dans cette étude rétrospective.
TECHNIQUE : Un cathéter est placé par voie veineuse
en face du plancher valvulaire pulmonaire. Une sonde
à lasso est introduite par voie artérielle. Le bout rigide
d’un guide 0,014 est enfoncé à travers le plancher val-
vulaire. Après accrochage, le circuit permet d’effectuer
une valvuloplastie au ballon. Un test de sevrage de pro-
staglandine E1 est effectué et si l’enfant reste ductodé-
pendant (SaO2< 80%), un stent est placé dans le canal
artériel.
RÉSULTATS : Cinq patients ont été inclus. Quatre ont
pu être perforés et dilatés dont deux stentés par la suite.
Chez un patient la procédure a du être interrompue.
SUIVI : Le premier patient stenté nécessite une chi-
rurgie à l’âge d’un an. Il décède en période postopéra-
toire, avec un stent toujours perméable. Le deuxième
est actuellement âgé de 18 mois (SaO2= 96%), le
troisième (stenté) a 16 mois (SaO2= 98%) et le dernier
va bien avec une SaO2> 85%.
CONCLUSION : Le traitement percutané de l’APSI
permet d’éviter la chirurgie à cœur ouvert. La mise de
stent dans le canal artériel remplace le shunt chirurgi-
cal de Blalock. Cependant, le pronostic reste lié à la
gravité de la maladie.
Chehab G, Chalouhi E, Najarian S, Sarkis A, Badaoui G, Daou L,
El-Rassi I, Abdel Massih T, Saliba Z. The percutaneous treatment
of pulmonary atresia with intact ventricular septum. J Med Liban
2012 ; 60 (2) : 65-69.
ABSTRACT • OBJECTIVE : Describe a mechanical
method of perforation-dilatation of the pulmonary
valve in pulmonary atresia with intact interventricular
septum (PA-IVS), with or without stenting the patent
ductus arteriosus (PDA) and medium-term results.
METHOD : Since 2007, all patients with PA-IVS and a
right ventricle adequate for biventricular repair, bene-
fited from a transcatheter attempt to perforate-dilate
the valve with or without stenting the PDA, and were
included in this retrospective study. TECHNIQUE : A
catheter was percutaneously introduced through the
femoral vein and positionned in front of the atretic pul-
monary valve. A lasso catheter was introduced through
the femoral artery to the other side of the pulmonary
valve. The tip of a rigid guidewire was then pushed
through the atretic valve and taken with the lasso, cre-
ating a loop that allowed for balloon valvuloplasty. If
the child remained ductal dependant following PGE1
withdrawal, a stent is placed in the ductus arteriosus.
RESULTS : Five patients were included in this series.
Four patients were successfully dilated, and two pa-
tients necessitated stents. The procedure had to be inter-
rupted in one patient. FOLLOW-UP : One patient with a
patent stent was operated at the age of one year and died
in the postoperative period. The other patient with a
stent is now 16 months old with a patent stent and an
oxygen saturation of 98%. The two remaining patients
without stent are now 3- and 18-month-old with oxygen
saturation of 85% and 96% respectively.
CONCLUSION : The percutaneous treatment of PA-
IVS is feasible and avoids early high risk surgery.
Stenting the ductus arteriosus may replace a Blalock
shunt. However, the prognosis is still related to the
severity of the anomaly.

66 Journal Médical Libanais 2012 •
Volume 60 (2)
G. CHEHAB et al. – Traitement percutané de l’atrésie pulmonaire
popularité ces dernières années et semble offrir une alter-
native acceptable dans un groupe sélectif de patients [1, 4].
Dans cette étude, nous décrivons la procédure, ainsi que
nos résultats à court et à moyen terme, du traitement non
chirurgical de l’APSI. Cette technique consiste à perforer-
dilater la valve pulmonaire atrétique, puis à la mise ulté-
rieure, si besoin, d’un stent dans le canal artériel. Notre série,
à notre connaissance unique au Liban, met en relief les
particularités d’une méthode mécanique de perforation du
plancher valvulaire pulmonaire, élaborée par notre équipe.
MATÉRIEL ET MÉTHODE
Depuis 2007, toute APSI jugée favorable à la répara-
tion biventriculaire (Z-score de la valve tricuspide adé-
quat avec un VD tripartite et circulation coronaire aorte-
dépendante), a bénéficié d’une tentative de traitement
percutané. L’évaluation préopératoire est faite par écho-
graphie Doppler cardiaque suivie de cathétérisme diag-
nostique et éventuellement thérapeutique.
Technique
Après consentement éclairé des parents, le patient est
transféré sous perfusion continue de prostaglandine E1
(PGE1) en salle de cathétérisme. Une veine et une artère
fémorale controlatérale sont prises. Après avoir vérifié
que la circulation coronaire est totalement aorto-dépen-
dante, on procède à la perforation mécanique du plancher
valvulaire pulmonaire atrétique. Dans cette optique, une
sonde JR 4 French est placée par voie veineuse en face du
plancher valvulaire pulmonaire. Dans cette sonde, et après
lui avoir connecté une valve hémostatique, on introduit le
bout rigide d’un guide coronaire rigide 0,014 inch. A la
rencontre de ce guide, on introduit une sonde à lasso par
123
45
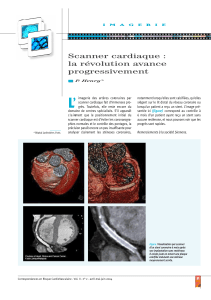
FIGURES 1 À5
1JR4 en face du plancher valvulaire.
.
2Passage du guide à travers le plancher
valvulaire.
3Bout rigide du guide capturé par le lasso.
4Valvuloplastie pulmonaire au ballon.
5Stent dans le canal artériel.

G. CHEHAB et al. – Traitement percutané de l’atrésie pulmonaire Journal Médical Libanais 2012 •
Volume 60 (2)
67
voie artérielle, qu’on place à travers le canal artériel en
face du plancher valvulaire pulmonaire du côté pul-
monaire (Fig. 1). Le lasso est prêt à recevoir le bout rigide
du guide métallique après perforation (Fig. 2).Une fois ce
dernier capturé au lasso (Fig. 3), le circuit artério-veineux
permet d’avancer le cathéter veineux à travers le plancher
valvulaire perforé, et de replacer cette fois le guide rigide
dans le bon sens (le bout souple en premier). A ce stade,
une valvuloplastie pulmonaire au ballon est effectuée
(Fig. 4) avec toutefois une assistance au lasso artériel pour
maintenir un support rigide et pour forcer le matériel à
avancer. En fin de procédure, une aortographie en pro-
jection latérale, effectuée en face du canal artériel, per-
met la délinéation anatomique de ce dernier en vue d’une
mise ultérieure éventuelle d’un stent. Le patient est en-
suite transféré en unité de soins pour surveillance. Durant
quelques jours, on va documenter le besoin d’un shunt
aorto-pulmonaire palliatif en testant la tolérance (SaO2) au
sevrage des PGE1. Ces tests répétitifs d’arrêt de PGE1
permettent d’une part, de préciser la dose minimale de
PGE1 nécessaire pour maintenir le canal artériel patent et
d’autre part, d’identifier l’intervalle de temps nécessaire
pour la fermeture (ou la restriction) du canal artériel après
sevrage de PGE1. Si malgré les mesures thérapeutiques
diverses (remplissages, bétabloquants), en vue d’amélio-
rer la fonction diastolique ventriculaire droite et de dimi-
nuer le shunt droite-gauche interauriculaire, la SaO2reste
basse (< 80%), une mise de stent dans le canal artériel sera
alors programmée. Dans cette optique, la perfusion de
PGE1 est arrêtée quelques heures avant la procédure pour
obtenir une restriction au bout pulmonaire du canal arté-
riel ce qui aidera à la mise de stent, pourvu que l’anatomie
soit favorable (canal non tortueux).
Le stent choisi est celui destiné à l’angioplastie coro-
naire. Sa longueur doit couvrir tout le canal artériel sans
déborder dans l’aorte. Son diamètre varie entre 3 et 4 mm
selon le poids du patient. Le stent est délivré par voie
veineuse et une injection artérielle à la fin de la procédure
permet d’évaluer le bon fonctionnement ainsi que le posi-
tionnement du stent (Fig. 5). Par la suite, le patient tou-
jours sevré de PGE1, est mis sous aspirine à dose anti-
agrégeante. Le suivi après sortie à domicile est clinico-
échographique et mensuel dans les six premiers mois.
RÉSULTATS
Cinq patients âgés de 2 à 11 jours avec un poids de 2,3
à 3,8 kg ont été estimés, à l’échocardiographie transtho-
racique, réparables en biventriculaire, et ainsi, ils ont été
inclus dans cette étude. Les patients sont listés par ordre
chronologique (Tableau I).
– Le 1er patient dans cette série a eu une perforation
dilatation (P-D) puis mise de stent dans le canal artériel.
Par la suite, il a développé une sténose médio-ventricu-
laire droite qui a nécessité une chirurgie à l’âge d’un an.
Le cathétérisme cardiaque, réalisé en préopératoire, a mis
en évidence un canal toujours perméable sans sténose val-
vulaire pulmonaire et une SaO2à 98%. Il décède en post-
op immédiate dans un tableau de fièvre majeure et de
défaillance multiviscérale.
– Le 2epatient a eu une P-D de la valve pulmonaire
sans la nécessité de mise de stent dans le canal artériel. Il
a actuellement 18 mois et est asymptomatique. La SaO2
est à 96% et l’échocardiographie montre une fonction car-
diaque normale.
– Le 3epatient a eu une P-D suivie d’une mise de stent
dans le canal artériel. Il a actuellement 16 mois avec une
SaO2normale et un stent perméable malgré l’arrêt de
l’aspirine depuis six mois. Il n’y a pas de sténose pulmo-
naire. Une fermeture percutanée du canal stenté sera pro-
grammée.
– Chez le 4epatient, la procédure a été abandonnée
après 70 minutes d’essai non fructueux dans de mauvaises
conditions hémodynamiques liées à des troubles de rythme
graves. Le chirurgien lui a ouvert la voie pulmonaire et lui
a connecté un shunt de Blalock-Taussig modifié. Il sort à
domicile un mois après et décède à l’âge de 3 mois d’une
infection pulmonaire virale.
TABLEAU I
LISTE DES PATIENTS AYANT BÉNÉFICIÉ D’UNE TENTATIVE DE DILATATION MÉCANIQUE PAR CATHÉTÉRISME
AVEC OU SANS MISE DE STENT DANS LE CANAL ARTÉRIEL
Nº/Sexe Age
/
Poids (kg) Tricuspide Temps Résultat Mise de stent
/
Temps Suivi
(mm)
/
Z score de procédure de procédure
1
/
MJ4
/
3 kg 13 mm
/
+0,5 80 min Succès +
/
40 min SaO2= 98% à 1 an et stent
perméable.
Décède à 1 an post chirurgie pour
sténose médio-ventriculaire droite
2
/
FJ11
/
3,1 kg 13 mm
/
0135 min Succès 18 mois, SaO2= 96%
3
/
MJ2
/
2,3 kg 10 mm
/
–1,5 45 min Succès +
/
80 min 16 mois, SaO2normale et stent
perméable
4
/
M J9
/
3,8 kg 17 mm
/
+2 120 min Echec du cathétérisme Décédé à l’âge de 3 mois suite à
(Cure chirurgicale) une infection pulmonaire virale
5
/
FJ3
/
3 kg 13 mm
/
0 110 min Succès 1 mois, SaO2 = 85%

68 Journal Médical Libanais 2012 •
Volume 60 (2)
G. CHEHAB et al. – Traitement percutané de l’atrésie pulmonaire
– Le 5eet dernier patient a eu une P-D de la valve pul-
monaire sans la nécessité de mise de stent dans le canal
artériel. Il a actuellement 1 mois [de vie] et [il] est asymp-
tomatique. La SaO2est à 85% et l’échocardiographie
montre une fonction cardiaque normale.
DISCUSSION
La réparation biventriculaire chirurgicale des APSI,
ayant une forme anatomique favorable, est standardisée.
Elle consiste à pratiquer une valvulotomie chirurgicale
avec ou sans élargissement de l’anneau pulmonaire et
à réaliser dans le même temps chirurgical un shunt de
Blalock-Taussig modifié. Cependant, cette chirurgie exige
une circulation extracorporelle à cœur ouvert chez des
nouveau-nés en état critique, ce qui augmente le risque
opératoire et le taux de mortalité [5]. La recherche d’une
alternative moins invasive via le développement du cathé-
térisme cardiaque lui a redonné de la popularité ces der-
nières années, tant sur le plan instrumental que sur les
compétences des opérateurs, si bien que, dans les centres
spécialisés, le traitement de premier choix est devenu la
perforation à la radiofréquence de la valve pulmonaire
atrétique suivie au besoin d’une mise de stent dans le
canal artériel [6]. Cette technique, bien qu’elle soit sédui-
sante, demande un équipement de pointe.
Depuis quelques années, notre équipe a élaboré une
technique de perforation particulière, ayant comme avan-
tage non seulement un coût moins élevé adapté aux pays
en voie de développement, mais aussi d’autres supério-
rités en termes de sécurité et peut-être d’efficacité. Notre
méthode mécanique économise le prix de l’appareil de
perforation à radiofréquence [7]. Par ailleurs, l’utilisation
du lasso évite la dilatation progressive avec plusieurs bal-
lonnets et permet d’intervenir avec un seul ballon de dia-
mètre final. D’autre part, l’accrochage au lasso placé dans
l’artère pulmonaire est une preuve que le bout du guide
rigide est bien placé dans la lumière de l’artère pulmo-
naire et non pas dans le péricarde, ce qui baisse considé-
rablement le risque d’épanchement péricardique par per-
foration au cathéter de la paroi infundibulaire. Cependant,
le guide rigide introduit dans le sens inverse aboutit à un
redressement du bout distal du cathéter et à la perte de sa
position prévalvulaire. La manœuvre de « préformer » ce
dernier pour lui donner la courbure du cathéter, permet
de surmonter cette complication. L’utilisation d’un guide
de perforation spécial moins rigide a été décrite par une
équipe espagnole et pourrait être une alternative [8].
L’application de la méthode mécanique a été un succès
chez quatre des cinq patients dans notre série. L’échec
est survenu chez le quatrième patient indépendamment
du niveau d’expertise acquis. La survenue de troubles du
rythme cardiaque avec instabilité hémodynamique a fait
opter pour l’arrêt de la procédure et par la suite pour la
décision chirurgicale.
D’autre part, cette manœuvre est difficile et longue
(temps de procédure : 80, 135, 45 et 110 minutes dans les
quatre cas successivement). L’acquisition de la technique
« biplan » de scopie pourrait dans l’avenir raccourcir le
temps de procédure et minimiser ainsi le taux d’irradiation.
L’utilisation des stents dans les cardiopathies ducto-
dépendantes a débuté à la fin des années 80. Durant cette
dernière décennie, et grâce aux avancées techniques,
plusieurs publications ont souligné l’efficacité de ce traite-
ment palliatif comme alternative non chirurgicale autant
pour remplacer le shunt de Blalock-Taussig que pour gar-
der une circulation systémique dans le canal artériel de
l’hypoplasie du cœur gauche [9-11].
La levée d’obstacle dans les APSI aboutit paradoxale-
ment à une aggravation du shunt droite-gauche à l’étage
auriculaire suite à une altération de la fonction diastolique
du VD. Cette détérioration, généralement transitoire, né-
cessite quelques mesures thérapeutiques comme les rem-
plissages et les bétabloquants. Malgré ces manœuvres,
quelques patients restent ducto-dépendants et ceci pendant
quelques semaines ou mois. Chez ces derniers, la mise de
stent dans le canal artériel serait une alternative non chirur-
gicale au shunt de Blalock-Taussig.
Cette technique est un défi pour l’interventionniste au-
tant pour la délicatesse des manœuvres effectuées, que
pour le choix du matériel et le timing de la procédure. La
manipulation des cathéters exigent des compétences de
pointe pour vaincre la tortuosité des trajectoires miniatu-
risées chez les nouveau-nés. Les stents utilisés sont ceux
initialement conçus pour les coronaires de l’adulte. Les
caractéristiques requises pour ces endoprothèses sont
aussi la haute malléabilité et la haute densité des cellules
pour éviter la redondance du tissu ductal réduisant la
lumière du stent.
Pour éviter la migration secondaire du stent, il doit être
implanté dans un canal en voie de fermeture avec une
restriction anatomique à son bout pulmonaire. Le « juste
temps » d’implantation, défini par le délai entre l’arrêt de
PGE1 et la formation d’une sténose ductale suffisante, est
retrouvé par les tests répétitifs de sevrage en PGE1.
Dans notre série, nous avons réussi à stenter le canal
artériel chez les deux patients qui l’ont nécessité. Leur
perméabilité a été démontrée un an après l’implantation.
CONCLUSION
Le traitement percutané de l’APSI permet d’éviter la
chirurgie à cœur ouvert dans un groupe sélectif de nou-
veau-nés. La particularité de la méthode mécanique de la
perforation a été soulignée dans notre étude. La mise de
stent dans le canal artériel remplace le shunt Blalock-
Taussig classique. Le pronostic par ailleurs à moyen terme
reste lié à la gravité de la maladie elle-même [12].
RÉFÉRENCES
1. Vernant F, Saliba Z, Vouhe P. Sténose et atrésie pulmo-
naire à septum interventriculaire intact. EMC-Cardiologie
2002 ; 11 : 940-90.
2. Daubeney PEF, Delany DJ, Anderson RH et al. Pulmonary
atresia with intact ventricular septum : range of morpholo-
gy in a population-based study. JACC 2002 ; 39 : 1670-9.

G. CHEHAB et al. – Traitement percutané de l’atrésie pulmonaire Journal Médical Libanais 2012 •
Volume 60 (2)
69
3. Daubeney PE, Wand D, Delany DJ et al. Pulmonary atre-
sia with intact ventricular septum : predictors of early
and medium-term outcome in a population-based study.
J Thorac Cardiovasc Surg 2005 ; 130 ; 1071-8.
4. El Louali F, Villacampa C, Aklebert P et al. Sténose pul-
monaire et atrésie pulmonaire à septum interventriculaire
intact. Arch Pediatr 2011 ; 18 : 331-7.
5. Naoki Y, Masahiro Y. Surgical strategy for pulmonary
atresia with intact ventricular septum : initial manage-
ment and definitive surgery. Gen Thorac Cardiovasc Surg
2009 ; 57 : 338-46.
6. Lee M, Tsao L, Chiu HY, Chen M, Chiu IS. Outcomes in
neonates with pulmonary atresia and intact ventricular
septum underwent pulmonary valvulotomy and valvulo-
plasty using flexible 2-French radiofrequency catheter.
Yonsei Med J 2009 ; 50 : 245-51.
7. Saliba Z, Fadous Khalifé MC, Noun P, Chehab G,
Malouf I. Traitement transcutané de l’atrésie pulmonaire
à septum ventriculaire intact : une première au Liban.
Congr Soc Franc Pédiatrie, Nantes, Juin 04-07, 2008.
Abstr 058 in Arch Pediatr 2008 ; 15.
8. Alcibar-Villa J, Rubio A, Pena N et al. Pulmonary atresia
with intact ventricular septum. Perforation and pulmo-
nary valvuloplasty using a modified mechanical tech-
nique. Medium-term follow-up. Cardiologia 2007 ; 60 :
833-40.
9. Gewillig M, Boshoff DE, Dens J, Mertens L, Berson LN.
Stenting the neonatal arterial duct in duct-dependant pul-
monary circulation : New techniques, better results. J Am
Coll Cardiol 2004 ; 43 : 107-12.
10. Santoro G, Gaio G, Castaldi B et al. Arterial duct stent-
ing in low-weight new borns with duct-dependent pul-
monary circulation. Cathet Cardiovasc Interv 2011 ; 78 :
1002/ccd-23076.
11. Ruiz CE, Bailey LL. Stenting the ductus arteriosus: a
“wanna-be” Blalock Taussig. Circulation 1999 ; 99 :
2608-9.
12. Marasini M, Gorrieri PF, Tuo G et al. Long-term results
of catheter-based treatment of pulmonary atresia and
intact ventricular septum. Heart 2009 ; 95 : 1520-4.
1
/
5
100%