Newsletter 6

Endocardite+Infectieuse+(EI)+et+TAVI+
!"#$%&'()*#()#+"#$%&,-&*-.%.#
#
!"#$%&'(#)%"*
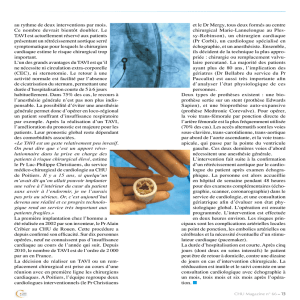
/.#0%0&'1)*%.#-2.2,1'(3#'4*.5*6(.5(#6(#'4/7#(8)#6(#9:#518#01,#;*''*%.#64<1=*)1.)8#()#
)%&5<(#0,2>2,(.)*(''(;(.)#'(8#<%;;(8#()#'(8#01)*(.)8#?-28#@AB:#518C;*''*%.#5<(D#
'(8#<%;;(8#(.),(#EF#()#EB#1.8G#A"###
H(8#01)*(.)8#0%,)(&,8#6(#0,%)<I8(#%.)#(&J#&.(#*.5*6(.5(#64/7#6(#9KKKC;*''*%.#6(#
01)*(.)8#8%*)#L#>%*8#0'&8#6(#,*8M&(#M&4(.#518#6(#N1'N&'%01)<*(#.1)*N(#()#AKK#>%*8#
0'&8#M&4(.#0%0&'1)*%.#-2.2,1'("#
#
O*#%.#8(#0'15(#61.8#&.(#0%0&'1)*%.#6(#01)*(.)8#1P1.)#&.#+QR73#%.#),%&N(S#
T &.#?-(#U#,*8M&(#1N(5#&.(#;%P(..(#1&J#1'(.)%&,8#6(#VK#1.8##
T 018#01,)*5&'*I,(;(.)#6(#0,26%;*.1.5(#;185&'*.(#1N(5#FAW#64<%;;(8#
0%&,#'(#,(-*8),(#X,1.5(#Y#01,#(J(;0'(#Y"##
T '(#0%*68#;1Z(&,#6(#'1#0,28(.5(#64&.(#0,%)<I8(#N1'N&'1*,(S#
#
7'#(8)#6%.5#'*5*)(#6(#0(.8(,#M&(#'4/7#,(0,28(.)(#&.#,2('#0,%='I;(#61.8#5())(#
0%0&'1)*%.#-,1.6*881.)("#[1*8#'(#6*1-.%8)*5#64/7#8&,#+QR7#(8)T*'#>*1='(#61.8#5())(#
0%0&'1)*%.#),I8#01,)*5&'*I,(#6(#01)*(.)8#?-283#62=*'*)28\#
#
H(8#Y#5,*)I,(8#;1Z(&,8#6(#'1#5'188*>*51)*%.#6(#]&^(#8%.)#'(#6*1-.%8)*5#
;*5,%=*%'%-*M&(#()#'(8#'28*%.8#6(#'4(.6%51,6(#U#'425<%-,10<*(#51,6*1M&(#
@N2-2)1)*%.83#1=5I83#62<*85(.5(#0,%)<2)*M&(#%&#.%&N(''(#>&*)(G#9"#
_,3#'425<%-,10<*(#5<(D#'(8#0%,)(&,8#6(#0,%)<I8(8#(8)#;%*.8#8(.8*='(#M&(#8&,#
N1'N&'%01)<*(#.1)*N(#(.#,1*8%.#.%)1;;(.)#6(#'1#,2>,*.-(.5(#6(8#0,%)<I8(8"#
H(8#5,*)I,(8#;*.(&,8#8%.)#'1#0,28(.5(#64&.(#0,%)<I8(3#'1#)%J*5%;1.*(3#'(8#
6*>>2,(.)8#0<2.%;I.(8#N185&'1*,(8#()#'1#>*IN,("#
_,3#61.8#5())(#0%0&'1)*%.#6(#01)*(.)8#?-283#>,1-*'(8#'1#0,28(.)1)*%.#5'*.*M&(#(8)#
8%&N(.)#)%,0*6(#1N(5#.%)1;;(.)#;%*.8#6(#>*IN,(`:TF#
H(#6*1-.%8)*5#64/7#8(;='(#6%.5#a),(#0'&8#6*>>*5*'(#5<(D#'(8#01)*(.)8#+QR73#64%b#&.(#
0%)(.)*(''(#8%&8T(8)*;1)*%.#61.8#5())(#0%0&'1)*%."#H(8#9#82,*(8#,25(.)(8#0&='*2(8#
8&,#/7#()#+QR7#,100%,)1*(.)#&.(#*.5*6(.5(#1..&(''(#(.),(#K3E#()#Y3AW#LTV"#
#
+*,-$).,*)/0%$#1"#.,*,'$*2!*.#*345!*
T c.(#2)&6(#,2),%80(5)*N(#*)1'*(..(#8&,#A:#5(.),(8#1#*.5'&#YFEY#0)8#(.),(#
d1.N*(,#YKKV#()#QN,*'#YKA9"#H1#,201,)*)*%.#(.),(#O10*(.#()#!%,(R1'N(#2)1.)#
6(#:KTLKW"#]&,1.)#&.#8&*N*#;26*1.#6(#A3A#1.3#YB#/7#%.)#2)2#
6*1-.%8)*M&2(8#L"#
T c.(#2)&6(#,2),%80(5)*N(#6(#'42M&*0(#6(#e%6(8T!1=1&#(8)#01,&(#(.#YKAF#
61.8#!*,5&'1)*%.#,(0,28(.)(#'1#82,*(#'1#0'&8#*;0%,)1.)(#U#5(#Z%&,#1N(5#
EB::#01)*(.)8#8&,#YA#5(.),(8#(.),(#YKKE#()#YKA:"#H(#,100%,)#(.),(#N1'N(8#
O10*(.#()#!%,(N1'N(#2)1*)#5())(#>%*8#*.N(,8(#U#VKTYKW"#H(#8&*N*#;%P(.#2)1*)#
6(#A3A#1.8#1N(5#F9#/7#6*1-.%8)*M&2(8#E"#
T (.>*.3#&.(#2)&6(#;%.%5(.),*M&(#61.%*8(3##1#*.5'&#FKB#01)*(.)8#(.),(#YKKE#
()#YKA:"#H4&.(#6(8#01,)*5&'1,*)28#2)1*)#'4(;0'%*#(J5'&8*>#6(#!%,(N1'N("#H(#
8&*N*#;26*1.#2)1*)#6(#A3:#1.8#()#AV#/7#%.)#2)2#6*1-.%8)*M&2(8#V"#
#
*

6%0'71#)%"*&.,*01#)."#,*345!*181"#*'".*2!*931:7.*;<*
7'#841-*)#6(#01)*(.)8#?-28#()#U#<1&)#,*8M&(#5<*,&,-*51'3#6%.5#&.(#0%0&'1)*%.#6(#
+QR7#188(D#5'188*M&(3#H1#,201,)*)*%.#<%;;(8C>(;;(83#.42)1*)#018#62)1*''2(#61.8#
'(#dQ!!3#61.8#'(#!*,5&'1)*%.#%.#.%)1*)#&.(#0()*)(#0,26%;*.1.5(#;185&'*.(#@FEWG#
()#61.8#'1#82,*(#61.%*8(3#&.(#.())(#;1Z%,*)2#64<%;;(8#@B:WG"#7'#8(;='(#6%.5#M&(#
'(8#<%;;(8#+QR7#8%.)#0'&8#U#,*8M&(#64/7#;1*8#1N(5#6(8#6%..2(8#U#*.)(,0,2)(,#
1N(5#0,&6(.5("##
#
#
JACC+2014#
Circ+2015#
Circ+Cardiovasc+
int+2015#
f=#%>#7/#
YB#
F9#
AV#
Q-(#@P,8G#
VKgL#
EBgV#
EVgE#
[1'(#8(J#@WG#
T#
FE#
B:#
/&,%85%,(#@WG#
Y9gA9#
YFgA:#
T#
X(N(,#@WG#
EL#
EY#
T#
h(1,)#X1*'&,(#@WG#
99#
FV#
T#
/;=%'*8;#@WG#
YE#
B#
T#
#
6$-,."#1#)%"*(7)")='.*931:7.*;<*
H1#>*IN,(#.42)1*)#0,28(.)(#M&(#61.8#EFW#6(8#518#5(#M&*#(8)#*.>2,*(&,#1&J#VFTBKW#
,100%,)28#(.#0%0&'1)*%.#-2.2,1'(#A"##
i1,#1*''(&,83#'(#8%&>>'(#6(#,2-&,-*)1)*%.#(8)#6*>>*5*'(;(.)#*.)(,0,2)1='(#10,I8#+QR7#
(.#,1*8%.#6(8#>&*)(8#02,*0,%)<2)*M&(8#1&6*='(8#(.#6(<%,8#6(#)%&)#5%.)(J)(#
*.>(5)*(&J"#
/)#(.>*.3#5%.5(,.1.)#'4*.8&>>*81.5(#51,6*1M&(#()#'(8#(;=%'(83#6(8#5<*>>,(8#
6*85%,61.)8#8('%.#'(8#2)&6(8"##
#
>)1?"%,#)(*
O('%.#'(8#5,*)I,(8#6(#]&^(3#*'#P#1N1*)#ACL#6(#6*1-.%8)*58#0%88*='(8#0%&,#'(#dQ!!3#
;%*.8#6(#FW#0%&,#'(#!*,5&'1)*%.#()#0'&8#6(#j#0%&,#'1#82,*(#61.%*8(`#
k#/.#)(,;(#6425<%-,10<*(#51,6*1M&(3#%.#,(),%&N1*)S#
T EEW#6(#01)*(.)8#1N(5#6(8#N2-2)1)*%.8#61.8#'1#82,*(#6(#!*,5&'1)*%.#
T VLW#6425<%-,10<*(8#0%8*)*N(8#61.8#'(#dQ!!#;1*8#81.8#'(#62)1*'#6(#
N2-2)1)*%.8#%&),(#
T 8(&'8#FLW#6(8#01)*(.)8#1N1*(.)#6(8#N2-2)1)*%.8#61.8#'1#82,*(#61.%*8("#7'8#
,21'*81*(.)#61.8#'(8#518#.2-1)*>8#&.(#25<%-,10<*(#*.),151,6*1M&(3#5(#M&*#1#
0(,;*8#641;(.(,#'(#6*1-.%8)*5#(5<%-,10<*M&(#U#EYW#
#
Q&5&.(#6(8#9#82,*(8#.(#;(.)*%..(#64*;1-(,*(#.&5'21*,(#@i()T851.#%&#
85*.)*-,10<*(#1&J#'(&5%5P)(8#;1,M&28G3#6%.)#%.#81*)#0%&,)1.)#M&4(''(#0(&)#1*6(,#
1*1-.%8)*5#5<(D#'(8#0%,)(&,8#6(#0,%)<I8(8#BTAK"##
#
#
#

k#H1#,201,)*)*%.#6(8#;*5,%%,-1.*8;(8#(8)#188(D#5%.5%,61.)(#(.),(#
'(8#6*>>2,(.)(8#82,*(8#1N(5#&.(#.())(#0,26%;*.1.5(#6(#
8)10<P'%5%M&(8#6%,28#()#5%1-&'18(#.(-1)*N(#@(.),(#AC9#()#'1#;%*)*2#
6(8#-(,;(8#,(),%&N28G3#()#&.(#0,%0%,)*%.#*;0%,)1.)(#64(.)2,%5%M&(8#@YK#U#9KW#
6(8#518G"##
#
H(#;%)#6<*,&,-*(.#S#!(5*#(8)#&.#1,-&;(.)#0%&,#0,l.(,#'1#,(5<(,5<(#6(#
0%,)(&,8#81*.8#6(#8)10<P'%5%M&(8#1&#.*N(1&#.181'#5<(D#5(8#01)*(.)8#?-28#
82Z%&,.1.)#(.#*.8)*)&)*%.3#8%&N(.)#5%'%.*828"#!4(8)#2-1'(;(.)#&.#1,-&;(.)#U#
'4(.5%.),(#6%.61-(#N28*51'#8P8)2;1)*M&("#
[a;(#8*#'(8#-(,;(8#=&55%6(.)1*,(8#8%.)#'1,-(;(.)#;*.%,*)1*,(8#@LW#61.8#'1#
82,*(#6(#Q;1)TO1.)%83#A:W#5<(D#H1)*=#()#1'3#9:W#5<(D#_'8(.#()#1'G3#'1#
,(5<(,5<(#()#'42,16*51)*%.#6(#)%&)#>%P(,#6(.)1*,(#1N1.)#+QR7#01,1m)#2-1'(;(.)#
Z&8)*>*2(3#6(#'1#;a;(#>1n%.#M&41N1.)#&.(#5<*,&,-*(#51,6*1M&("##
#
#
@A$%"%7%?).*&'*&)1?"%,#)(*&B2!*,'$*345!*
O&,#'(8#9#2)&6(83#0'&8#6(#'1#;%*)*2#6(8#/7#8&,N*(..(.)#61.8#'(8#L#;%*8#0%8)T+QR7#
5(#M&*#(8)#&.#62'1*#),I8#5%&,)3#()#'1#0,%0%,)*%.#64/7#),I8#0,25%5(8#(8)#2'(N2(#1N(5S#
T AVW#6(8#01)*(.)8#M&*#%.)#&.(#/7#'(#A(,#;%*8#61.8#'(#!*,5&'1)*%.#
T YVW#0%&,#'1#82,*(#61.%*8(#
T YEW#8&,#'(8#Y#0,(;*(,8#;%*8#61.8#'(#dQ!!#
5(#M&*#0(&)#2N%M&(,#&.(#51&8(#*1),%-I.(3#1N(5#0%&,#'(8#-(,;(8#(.#51&8(#&.(#
0,26%;*.1.5(#6(#8)10<P'%5%M&(8#()#64(.)2,%5%M&(8"#
#
](#0'&83#5(8#/7#),I8#0,25%5(8#8&,N*(..(.)#1'%,8#M&(#)%&8#'(8#01)*(.)8#%.)#(&#&.(#
Q+$0,%0<P'1J*(#1N1.)#+QR73#5%;;(#,(5%;;1.62#61.8#'(8#-&*6('*.(8#/O!#YKAF#
@5'188(#771G#AA"#
#
6$-C."#)%"*&.,*2!*,'$*345!*
Antibioprophylaxie+
+%&8#'(8#01)*(.)8#%.)#(&#&.(#Q+$0,%0<P'1J*(#;1*8#(''(#.42)1*)#018#8)1.61,6*82("#
H1#82,*(#61.%*8(#;(.)*%..(#S##o1&#N(8#/7#),I8#0,25%5(8#10,I8#+QR7#1N(5#&.(#
01,)#.%.#.2-'*-(1='(#64(.)2,%5%M&(83#0(&)Ta),(#>1&6,1*)T*'#;%6*>*(,#
'4Q+$0,%0<P'1J*(3#'(8#520<1'%80%,*.(8#(.#A#0,*8(#.(#5%&N,1.)#018#'(8#
(.)2,%5%M&(8"#o#Q#6*85&)(,`#
#
Salle+de+cathéthérisme/hybride+
H1#;1Z%,*)2#6(8#0,%526&,(8#2)1*(.)#,21'*82(8#(.#81''(#6(#51)<2)<2,*8;(#@FFW#
0%&,#'(#dQ!!#()#LAW#0%&,#!*,5&'1)*%.G"#H(8#81''(8#<P=,*6(8#0,28(.)(.)#&.(#
;(*''(&,(#18(08*(#()#0(,;()),1*(.)#6%.5#6(#'&))(,#0'&8#(>>*515(;(.)#5%.),(#'(8#
*.>(5)*%.8#.%8%5%;*1'(8"#
#
3$1)#./."#*&.,*2!*,'$*345!#
H1#-,1.6(#;1Z%,*)2#6(8#01)*(.)8#1N1*)#&.(#*.6*51)*%.#)<2%,*M&(#64*.)(,N(.)*%.#
5<*,&,-*51'(#8('%.#'(8#-&*6('*.(83#1N(5#01,#(J#VEW#6(8#01)*(.)8#61.8#'(#
!*,5&'1)*%.3#'1#0'&01,)#(.#,1*8%.#64&.(#*.8&>>*81.5(#51,6*1M&(#@FBWG#%@&.#5<%5#
8(0)*M&(#@YVWG"#

Q&#>*.1'3#L#U#A9W#8(&'(;(.)#6(8#01)*(.)8#%.)#(&#&.(#*.)(,N(.)*%.3#M&(#5(#8%*)#&.(#
5<*,&,-*(#%&#&.(#0,%526&,(#6(#N1'N(#*.#N1'N(#61.8#'(8#6*>>2,(.)(8#82,*(8"##
!(8#5<*>>,(8#8%.)#=*(.#*.>2,*(&,8#U#5(&J#%=8(,N28#61.8#'(8#82,*(8#64(.6%51,6*)(8#
8&,#0,%)<I8(8#N1'N&'1*,(8#5<*,&,-*51'(8#AY"#]410,I8#'(#/&,%#h(1,)#O&,N(P3#FKW#6(8#
01)*(.)8#0,28(.)1.)#&.(#(.6%51,6*)(#8&,#0,%)<I8(#8%.)#),1*)28#01,#5<*,&,-*(#A9"##
#
!())(#6*>>2,(.5(#61.8#'1#0,*8(#(.#5<1,-(#0(&)#84(J0'*M&(,#U#9#.*N(1&J#S#
T6(8#01)*(.)8#>,1-*'(83#5%.),(T*.6*M&28#U#'1#5<*,&,-*(#%&#Z&-28#U#),%0#<1&)#,*8M&(#
0%&,#&.#,(;0'15(;(.)#N1'N&'1*,(#1%,)*M&(#8)1.61,63#6%.5#U#>%,)*%,*#0%&,#&.(#
5<*,&,-*(#64(.6%51,6*)(#
T&.(#0,28(.)1)*%.#5'*.*M&(3#=15)2,*%'%-*M&(#()#25<%-,10<*M&(#1)P0*M&(3#1;(.1.)#
U#6(8#,()1,68#6(#6*1-.%8)*5"#H4(.6%51,6*)(#(8)#625%&N(,)(#1)16(#6(8#
5%;0'*51)*%.8#-,1N(8#()#6(8#'28*%.8#62'1=,1.)(8#
T&.(#>%,;(#1.1)%;*M&(#01,)*5&'*I,(#S#5%.),1*,(;(.)#1&J#0,%)<I8(8#5<*,&,-*51'(8#
%b#'(#8)(.)#(8)#1&#.*N(1(#'41..(1%,)*M&(3#'1#0%,)*%.#;2)1''*M&(#6(8#
(.6%N1'N(8#,(;%.)(#1(88&8#6(8#8*.&8#6(#R1'81'N1#61.8#'(#518#6(#'1#!%,(N1'N(3#
6(85(.6#8%&8#'(#0'1.#6(#'41..(1&#@!%,(N1'N(#()#O10*(.G3#1N(5#0'&8#6(#,*8M&(#
64(J)(.8*%.#1&J#)*88&8#1N%*8*.1.)8"#H(#)1&J#641=5I8#6(#'1#,15*.(#1%,)*M&(3#6(#
>*8)&'(#1*.8*#M&(#6(#0(,>%,1)*%.#6(#'1#N1'N(#;*),1'(#1.)2,*(&,(#(8)#
01,)*5&'*I,(;(.)#2'(N2#V"#/.>*.3#'4(J0'1.)1)*%.#6(#'1#0,%)<I8(#+QR7#0(&)#a),(#
,(.6&(#6*>>*5*'(#8*#'(#8)(.)#(8)#=*(.#1.5,2#61.8#'41%,)("#!(5*#(J0'*M&(#0,%=1='(;(.)#
M&4U#85%,(#6(#,*8M&(#2-1'3#'4*.)(,N(.)*%.#5<*,&,-*51'(#8%*)#6(&J#>%*8#0'&8#>,2M&(.)(#
61.8#'(#518#64&.(#(.6%51,6*)(#8&,#0,%)<I8(#O10*(.3#5%;01,2(#1&J#0,%)<I8(8#
!%,(N1'N(#A:"#
H%8M&4(''(#(8)#,21'*81='(3#'1#0,*8(#(.#5<1,-(#5<*,&,-*51'(#6(8#(.6%51,6*)(8#0%8)T
+QR7#(8)#-,(N2(#64&.(#;%,)1'*)2#1&J#1'(.)%&,8#6(#9KW3#(.#>%.5)*%.#6(8#82,*(83#
0%88*='(;(.)#8%&8T(8)*;2(#01,#6(8#=*1*8#6(#0&='*51)*%."#
7'#(8)#U#.%)(,#M&(#'%,8M&4&.#),1*)(;(.)#5<*,&,-*51'#.(#0(&)#a),(#,21'*823#&.#
),1*)(;(.)#;26*51'#5%.8(,N1)(&,#0(&)#.21.;%*.8#%>>,*,#6(8#,28&')1)8#
155(0)1='(8#S#H%N(,*J#()#1'#,100%,)(.)#LKW#6(#8&,N*(#U#L#;%*8#1N(5#),1*)(;(.)#
;26*51'#8(&'3#8&,#6(8#(>>(5)*>8#5(0(.61.)#,26&*)8#AF"#
Q#;%*.8#M&4*'#.4(J*8)(#&.(#5%.),(T*.6*51)*%.#5<*,&,-*51'(#1=8%'&(3#*'#01,1m)#6%.5#
,1*8%..1='(#6(#,(6*85&)(,#'(8#6%88*(,8#1Ȇ#01,#518#1(*.#6(#'1#h(1,)#+(1;"#
#
D'$C).#
H(#)1&J#6(#625I8#*.),1<%80*)1'*(,#(8)#),I8#2'(N2S#:EW#0%&,#!*,5&'1)*%.#()#:FW#
0%&,#'(#dQ!!3#5(#M&*#(8)#'1,-(;(.)#8&02,*(&,#1&J#5<*>>,(8#,100%,)28#(.#0%0&'1)*%.#
-2.2,1'(#@1&J#1'(.)%&,8#6(#AFWG#%&,#6(8#82,*(8#5<*,&,-*51'(8#@Y9W#61.8#'(#
,(-*8),(#7!/G#A9"##H1#82,*(#]1.%*8(#0,28(.)(#6(8#5<*>>,(8#=183#;1*8#8&,#&.#0,%>*'#6(#
01)*(.)8#6*>>2,(.)#@&.#0(�'&8#Z(&.(83#85%,(8#6(#,*8M&(#*.5%..&8#()#YVW#6(#
6*1-.%8)*58#0%88*='(8G"#O(&'(#'1#82,*(#6(#!*,5&'1)*%.#,100%,)(#&.(#8&,N*(#0'&8#
0,%'%.-2(3#1N(5#&.#)1&J#6(#8&,N*(#U#A#1.#6(#9:W"#
#
E1(#.'$,*0$-&)(#)F,*&.*71*,'$C."'.*&B'".*2!*
H(8#,28&')1)8#2)1*(.)#188(D#5%.),16*5)%*,(8#(.),(#'(8#82,*(8#()#8&,)%&)#5(8#>15)(&,8#
0,26*5)*>8#%.)#2)2#1.1'P828#8&,#&.#>1*='(#.%;=,(#642N2.(;(.)83#U#81N%*,#
&.*M&(;(.)#'1#;%*)*2#6(#'1#0%0&'1)*%.#0%&,#'(#!*,5&'1)*%.#()#8&,#8(&'(;(.)#AV#/7#
61.8#'1#82,*(#61.%*8(3#6%.5#U#*.)(,0,2)(,#1N(5#=(1&5%&0#6(#0,&6(.5("##
_.#0(&)#.21.;%*.8#,201,)*,#5(8#>15)(&,8#(.#9#-,%&0(8#S#

T'*28#1)*(.)#S#?-(3#8(J(#;185&'*.#@(>>()#0,%)(5)(&,#6(8#%(8),%-I.(8G3#
5%;%,=*6*)283#%=28*)23#6*1=I)(3#5%,)*5%)<2,10*(#
T'*28#U#'1#0,%526&,(S#'4*.)&=1)*%.#%,%),15<21'(#>1N%,*8(,1*)#'(8#=15)2,*2;*(8#61.8#
'1#82,*(#6(#!*,5&'1)*%.#E3#81.8#M&(#'1#5<,%.%'%-*(#%&#'(8#-(,;(8#*.5,*;*.28#.(#
8%&)*(..(.)#&.(#51&81'*)2#6*,(5)(#p#'1#6&,2(#6(#'1#0,%526&,(#1*.8*#M&(#'1#0,28(.5(#
6(#5%;0'*51)*%.8#N185&'1*,(8#@<2;1)%;(#5%;;(#8%&,5(#6(#=15)2,*2;*(G#8%.)#
2-1'(;(.)#8&80(5)2(8"#
T'*28#U#'1#0,%)<I8(#S#'1#!%,(N1'N(#8(,1*)#0'&8#U#,*8M&(#61.8#'(#!*,5&'1)*%.#E3#)1.6*8#
M&4*'#P#1N1*)#0'&8#64/7#8&,#O10*(.#61.8#'1#82,*(#6&#dQ!!#L"#H1#0,28(.5(#64&.(#>&*)(#
01,10,%)<2)*M&(#%@&.#-,16*(.)#),1.80,%)<2)*M&(#2'(N2#>1N%,*8(,1*)#2-1'(;(.)#
'1#-,(>>(#=15)2,*(..(#(.#5,21.)#6(8#)&,=&'(.5(8#E"#!('1#.41#.21.;%*.8#Z1;1*8#0&#
a),(#5'1*,(;(.)#62;%.),23#P#5%;0,*8#0%&,#'(8#0,%)<I8(8#5<*,&,-*51'(8"#
#
2"*(%"(7',)%"3#%.#,()*(.)#&.(#*.5*6(.5(#1..&(''(#6(#'4/7#8&,#+QR7#6(#K3E#U#Y3AW#
8('%.#'(8#82,*(83#815<1.)#M&4*'#841-*)#6(#01)*(.)8#?-283#>,1-*'(83#1N(5#&.(#
0,28(.)1)*%.#5'*.*M&(#*.8*6*(&8("##H4162M&1)*%.#6(8#5,*)I,(8#6(#]&^(#.41#018#2)2#
8025*>*M&(;(.)#2N1'&2(##61.8#5())(#0%0&'1)*%.#()#'4*.5*6(.5(#6(8#/7#8&,#+QR7#
0%&,,1*)#a),(#8%&8T(8)*;2("##
i1,#1*''(&,83#'1#0,%0%,)*%.#64/7#),I8#0,25%5(8#(8)#2'(N2(3#j#8&,N(.1.)#6&,1.)#'(8#Y#
0,(;*(,8#;%*8#6(#;1.*I,(#5%.5%,61.)(#8&,#'(8#9#2)&6(83#1N(5#&.(#;1Z%,*)2#6(#
8)10<P'%5%M&(8#;1*8#&.(#>,2M&(.5(#64(.)2,%5%M&(8#0'&8#2'(N2(#M&(#61.8#'1#
0'&01,)#6(8#1&),(8#(.6%51,6*)(8#@P#5%;0,*8#8&,#0,%)<I8(G"#
!())(#5<,%.%'%-*(#()#'(8#;*5,%%,-1.*8;(8#8&--I,(.)#&.(#01,)#.%.#.2-'*-(1='(#
64/7#.%8%5%;*1'("#!('1#0%8(#'(#0,%='I;(#6(8#;%61'*)28#64Q+$#0,%0<P'1J*(#M&*#
6(N,1*(.)#a),(#8)1.61,6*82(8#()#0%)(.)*(''(;(.)#;*(&J#1610)2(8#1�,%>*'#
;*5,%=*%'%-*M&(#()#'1#.25(88*)2#6(#5%.6*)*%.8#6418(08*(#0'&8#8),*5)(8#.%)1;;(.)#
01,#'1#6*>>&8*%.#6(8#81''(8#<P=,*6(8"#
q&1.6#(''(#(8)#,21'*81='(3#'1#5<*,&,-*(#(8)#,(.6&(#5%;0'*M&2(#01,#6(8#5%.6*)*%.8#
01,)*5&'*I,(8#'*2(8#1)*(.)3#U#'1#>%,;(#1.1)%;*M&(#()#1&#;1)2,*('#0,%)<2)*M&(3#
;1*8#,(8)(#.21.;%*.8#&.(#%0)*%.#U#6*85&)(,#(.#h(1,)#+(1;"#
H1#0,2N(.)*%.#(8)#641&)1.)#0'&8#.25(881*,(#5%;0)(#)(.�,%.%8)*5#(>>,%P1='(#
6(8#/7#8&,#+QR7"#
#
Bibliographie#
A#S#D.7#%"GD'#8*@*.#*17H*@7)"*!"F.(#*>),*IJ;IKLMN;I+JGO*
Y#S*P)71$&*Q*.#*17H*R*2"?7*S*Q.&*IJ;I*K+TT*N;UJLG;L*
9#S*>'$1(V*>3*.#*17H*4/*S*Q.&*;OOM*K*OT*N*IJJGO**
:#S!W.$".$*PD*.#*17H*4/*S*Q.&*;OOTK*;JJ*N*OJGU*#
F#S#X%0.YGW%7F*>*.#*17H*Z.C*2,0*@1$&)%7*IJ;;KTM*N*+IOG++**
L#S!X1#):*4*.#*17H*S*4/*@%77*@1$&)%7*IJ;M*KTM*NI;UTG[*
E#S!4/1#GD1"#%,*!S*.#*17H*@)$('71#)%"*IJ;L*K*;+;*N;LTTGUM#
V#S!\7,."*R3*.#*17H*@)$(*@1$&)%C1,(*!"#.$C*IJ;L*40$*K[9M<H*0))*N.JJ;O+OH**
B#S#D1:8*.#*17H*S*4/*@%77*@1$&)%7*IJ;+KI+NI+UMG[I#
AK#S#Z%'Y.#*E*.#*17H*S*R'(7*Q.&H*IJ;M*>.(KLLN;O[JGL*#
AA#S!]1:):*P*.#*17H*2'$*].1$#*S*IJ;L*K+T*N+JULG;I[#
AY#S#W1"?*4*.#*17H*S4Q4*IJJUKIOUN;+LMGT;##
A9" 3%$"%,*6*.#*17H*].1$#H*IJJLKO;NLU;^L*
A:" *4/1#GD1"#%,*!H*S*4/*@%77*@1$&)%7*IJ;L*K[N++M^MT*
AF" #X%C.$)_*.#*17H*!"#.$"1#)%"17*S%'$"17*%F*@1$&)%7%?8**IJ;L*K;U[*NTU^[#
1
/
5
100%