C o n g r è s

La Lettre du Sénologue - n° 33 - juillet-août-septembre 2006
Revue de presse
31
Congrès
Congrès
31
Ces rencontres annuelles, destinées aux chirurgiens
spécialisés dans la prise en charge des cancers du sein,
ont eu lieu les 11 et 12 mai 2006. Cette réunion déli-
bérément interactive a été l’occasion d’échanges sur différents
aspects de la prise en charge pluridisciplinaire du cancer du
sein. Les présentations étaient suivies d’une mise en pratique
autour de cas cliniques discutés en ateliers pour permettre à
chacun de se positionner dans sa pratique quotidienne.
LES RECOMMANDATIONS DE L’INSTITUT NATIONAL
DU CANCER (INCa)
Dans le cadre des recommandations de l’INCa aux chirur-
giens, les grands principes garants d’une bonne pratique de la
chirurgie oncologique ont été présentés par le Pr Serge Uzan,
de l’hôpital Tenon (Paris). Ces principes reposent sur :
– la loyauté et l’information objective dues aux patients ;
– une formation initiale et continue adéquate ;
– une expérience et une activité suffisantes dans la pathologie
concernée ;
– des moyens à la hauteur dans la pathologie tant en ce qui
concerne le matériel que l’équipe ;
– une rigueur dans la gestion des données du dossier et un
compte-rendu des résultats ;
– le traitement des patients selon les informations et les
connaissances actuelles ;
– la multidisciplinarité indispensable ;
– un contrôle de qualité continu des pratiques ;
– l’honnêteté d’assumer ses difficultés et de savoir “passer la
main” à un confrère.
Mise en application et conséquences engendrées
au sein d’un Centre régional de Lutte
Contre le Cancer (CLCC)
D’après Jacques Dauplat (Clermont-Ferrand)
Les critères de qualité d’un service de chirurgie du cancer du
sein sont fondés sur :
L’activité annuelle du service (composé d’au moins deux
chirurgiens) qui doit être d’au moins de 20 interventions pour
cancer du sein. Or, dans les CLCC, la chirurgie du cancer du
sein représente plus de 21% des séjours hospitaliers en France
(12 à 49% selon les régions).
Les compétences des chirurgiens qui doivent avoir une for-
mation spécifique en chirurgie mammaire, suivre une forma-
tion médicale continue une fois par an (dont les congrès no-
tamment de la Société Française de Sénologie et de Pathologie
Mammaire) et participer aux Réunions de Concertation Pluri-
disciplinaire (RCP) de sénologie. De plus, une compétence en
chirurgie plastique est préférable.
Le plateau technique du bloc opératoire qui doit comprendre : un
mammographe et un écran, une table en position semi-assise
et une table de stéréotaxie dédiée, une salle d’anatomopatho-
logie à proximité pour permettre une analyse extemporanée,
un service de médecine nucléaire à proximité et une sonde de
détection au bloc, pour la technique de détection du ganglion
sentinelle, les tumeurs doivent pouvoir être conservées dans
une tumorothèque.
La pluridisciplinarité avec des réunions de concertations
pluridisciplinaires et la continuité des soins en accord avec le
Plan Cancer sont obligatoires (mise en place du dispositif d’an-
nonce). Les ERI (Espace Rencontres Information) destinés aux
patients et leur famille sont un exemple de cette démarche.
Enfin, les comptes-rendus opératoires et histologiques doi-
vent être standardisés et les délais de prise en charge courts.
Le point de vue de praticiens en secteur libéral
D’après Véronique Vaini (Aix-en-Provence)
et Bernard Flipo (Nice)
Au même titre que leurs collègues du secteur public, les mé-
decins du secteur libéral approuvent et souscrivent au Plan
Cancer qui, avec son ensemble de mesures positives et effica-
ces, est perçu comme un tournant décisif et qui fait de la prise
en charge des patients l’affaire de tous.
Cependant, ce changement important et nécessaire des pra-
tiques qui est demandé aux praticiens peut parfois engendrer
quelques difficultés d’ordre pratique essentiellement “chrono-
phages”. Dans les faits, les contraintes s’appliquent pour cha-
que patient (présentation de chaque cas en RCP) et le risque
de retards à la prise en charge est réel. De plus, la nomencla-
ture mériterait d’être mise à jour afin d’actualiser la cotation
de ces actes supplémentaires.
L’exemple de la mise en place du dispositif d’annonce fait ap-
paraître, qu’aux exigences légitimes des patients en vue d’ob-
tenir plus de prise en charge personnalisée mais qui implique
plus de temps avec leurs médecins, se traduit par une consul-
tation infirmière, compte tenu de la dotation qui est faite pour
l’établissement et non pour le médecin.
Les critères d’accréditation en tant que centre de soins de
chirurgie cancérologique peuvent parfois paraître flous ou
peu adaptés (figure 1).
Les troisièmes Rencontres de Chirurgie
du Cancer du Sein
Anne Ponzio-Prion* »
* Institut Gustave-Roussy, Villejuif.

La Lettre du Sénologue - n° 33 - juillet-août-septembre 2006
Congrès
Congrès
32
Figure 1.
De l’état des lieux aux buts xés par l’INCa.
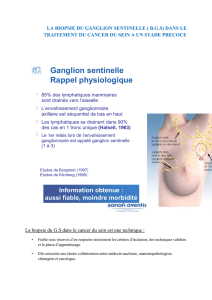
Figure 2.
Exérèse moyenne d’une tumeur supérieure.
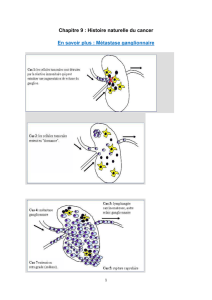
Figure 3.
Exérèse moyenne d’une tumeur centrale incision en
“round block”.
Aspects médico-légaux ou comment
s’intègrent-elles dans le mécanisme juridique ?
D’après ierry Casagrande (Analys-Santé)
L’INCa, aboutissement de la volonté présidentielle représentée
par le Plan Cancer, a vu le jour dans un contexte nouveau d’une
politique législative de santé publique, du développement de la
qualité, de l’évaluation et d’une démocratisation sanitaire avec la
prise en compte des droits et des attentes des patients. Parmi ses
rôles multiples, cet organisme, à titre d’institution référente, doit
définir des référentiels de prise en charge en cancérologie.
En cas de litige ou faute professionnelle, les recommandations
représentent une source professionnelle majeure et accessible
qui permet de dater les règles de bonne pratique et de déter-
miner les contours de la notion de faute. En revanche, elles
sont moins évolutives que la notion de données de la science
sur lesquelles se fondent habituellement le juge et ne représen-
tent qu’une approche collective des soins. Il peut y avoir une
discussion autour de la valeur et de la pertinence des critères
de jugement (niveau de preuve). Enfin, le risque de confusion
entre droit et recommandations existe.
Par exemple, une décision prise en RCP constitue une aide,
mais n’est pas suffisante à valider une stratégie thérapeutique
en cas de litige.
Ainsi, s’il existe une tendance du droit à confier à des organisa-
tions professionnelles le soin de définir des recommandations
ayant un caractère “opposable” pour le juge, les recomman-
dations ne constituent qu’un simple étalon de mesure de la
responsabilité médicale et la valeur, la pertinence et l’actualité
d’une recommandation peuvent toujours se discuter.
LA CHIRURGIE ONCOPLASTIQUE DU CANCER DU SEIN
La chirurgie oncoplastique consiste en l’utilisation de techniques
de chirurgie plastique dans le même temps que l’exérèse d’un
cancer. Dans le cadre du cancer du sein il peut s’agir d’une recons-
truction totale, après mastectomie, en vue de réduire les séquelles
ou d’une reconstruction partielle dont les objectifs sont multiples
et qui permet d’élargir les indications du traitement conservateur.
Parfois, les techniques sont relativement simples, dans d’autres
cas plus complexes et les indications sujettes à discussion.
Évolution des techniques chirurgicales unilatérales
ou bilatérales dans le cadre d’un traitement
conservateur
D’après Sylvia Giard (Lille)
Lors d’une exérèse d’une partie de la glande, il y a rupture du
galbe, bascule de l’aréole et réduction du volume mammaire
dont l’importance varie selon le volume de l’exérèse par rap-
port à celui du sein et selon la localisation tumorale. Ainsi,
dans le cas d’une exérèse tumorale petite ou moyenne, il fau-
dra soit libérer, soit transposer la plaque aréolo-mamelonnaire
sur l’équateur inverse de la localisation de l’éxérèse. Dans le cas
d’une exérèse moyenne d’une tumeur sus-aréolaire, la techni-
que employée est celle de la “Batscare”, incision qui permet de
recentrer l’aréole lorsque le geste est limité (figure 2).

La Lettre du Sénologue - n° 33 - juillet-août-septembre 2006
Revue de presse
33
Congrès
Congrès
33
Dans les tumeurs centrales, on peut combler le “defect” cen-
tral en libérant toute la glande mammaire de l’étui cutané
avec la technique du “round block”, redonner du volume puis
reconstruire la plaque aréolo-mamelonnaire dans un second
temps (figure 3).
Dans le cas d’une exérèse plus importante, un geste bilatéral
s’impose afin de symétriser les deux seins en réduisant l’étui
cutané controlatéral. Enfin, en cas d’exérèse majeure, un lam-
beau musculocutané s’impose.
Toutes ces interventions sont prévues à l’avance, avec réalisa-
tion d’un schéma préopératoire, prévision de la position opé-
ratoire et de la durée de l’intervention, information et discus-
sion préalable avec la patiente.
Indications : extension du traitement conservateur
D’après Philippe Rouanet (Montpellier)
Les objectifs du traitement conservateur sont d’ordre carci-
nologique avec, notamment, la prise en compte de la maladie
microscopique, esthétique et psychologique.
Plusieurs situations sont particulièrement difficiles où l’indi-
cation de l’oncoplastie est encore en discussion ou à l’étude,
mais en tout état de cause, elle doit être réservée à des équipes
entraînées collaborant étroitement avec les anatomopatholo-
gistes. Il s’agit par exemple du cas d’un carcinome canalaire
infiltrant étendu au quadrant ou avec une forte composante
intracanalaire : la question entre une mastectomie avec re-
construction immédiate qui guérit la patiente et une chirurgie
oncoplastique se pose.
Dans le cas des carcinomes intracanalaires localisés, la chirur-
gie oncoplastique peut se discuter malgré le standard reconnu
qu’est la stratégie résection-radiothérapie.
Après un traitement néoadjuvant, de nombreuses questions
restent en suspens : faut-il systématiquement enlever la zone
de localisation tumorale ? En cas de mauvaise réponse à la
chimiothérapie, faut-il systématiquement réaliser une mas-
tectomie chez une patiente de mauvais pronostic ? Que faire
en cas de disparition de la zone tumorale ? Les carcinomes
lobulaires ne sont pas une bonne indication à l’oncoplastie. Il
y a donc une nécessité de réaliser des études sur des grandes
séries après une homogénéisation des techniques, notamment
dans certaines indications.
Enseignement et apprentissage
D’après Krishna Clough (Paris)
Dans certains cas, des consensus internationaux sont d’ores
et déjà établis. En 2001, l’intérêt de la chirurgie oncoplasti-
que pour un carcinome intracanalaire, permettant un taux de
conservation mammaire plus important tout en réduisant les
séquelles, était établi (1).
La conférence de Philadelphie, en 2005, s’est prononcée en fa-
veur du développement d’une chirurgie conservatrice pour les
carcinomes infiltrants, avec une extension des indications (2).
Cela requiert une période d’acquisition des techniques indis-
pensable, mais parfois délicate.
Mises à part des techniques très particulières, la plupart des
interventions sont facilement réalisables et devraient être large-
ment proposées après un apprentissage relativement simple.
Pour les techniques sophistiquées, l’apprentissage est sujet à
une démarche personnelle avec participation à des cours, des
workshops et l’intégration d’une équipe pluridisciplinaire.
ACTUALITÉS DU GANGLION SENTINELLE
Les études en cours
D’après Jean-Marc Classe (Saint-Herblain)
Plusieurs questions demeurent en suspens auxquelles tentent
de répondre de nombreuses études internationales.
Quel est l’impact de la technique du ganglion sentinelle (GS)
sur la survie globale et la survie sans récidive ? L’étude du
NSABP B-32 randomise des patientes avec un T1-3 N0 entre
cette technique innovante seule ou suivie d’un curage : sur plus
de 5000 patientes, le taux de détection est de 97% et les faux
négatifs de 9,7%. Un quart des tumeurs de moins de 2 cm ont
un envahissement ganglionnaire. D’autres études comme celle
conduite par le groupe français d’étude du ganglion sentinelle
ou l’étude allemande KISS ne sont pas disponibles à ce jour.
L’étude ALMANAC a démontré que l’impact du ganglion
sentinelle sur la morbidité axillaire semble moindre que celui
d’un curage axillaire complet mais n’est, néanmoins, pas nul.
Plusieurs études testent actuellement l’intérêt du traitement com-
plémentaire de l’aisselle dans le cas d’un GS + : les études ACOZOG
Z10 et ACOZOG Z11, l’étude AMAROS de l’EORTC.
Des études françaises s’intéressent à des situations particuliè-
res : GS et chimiothérapie néoadjuvante (étude GANEA), GS
et tumeur multicentrique (étude IGASSU), GS après tumorec-
tomie préalable (étude GATA), GS et évaluation médico-éco-
nomique (étude STIC).
Ganglion sentinelle et micrométastase :
valeur pronostique et déductions thérapeutiques
D’après Gilles Houvenaeghel (Marseille)
La micrométastase du ganglion sentinelle est loin d’être rare :
elle est retrouvée, en effet, en moyenne dans 13% des techni-
ques pratiquées et dans 40 % des GS +.
Malgré son coût, l’immunohistochimie doit être pratiquée sys-
tématiquement à la recherche d’une micrométastase, puisqu’elle
permet de réduire les faux négatifs en détectant près de la moitié
des micrométastases. Les ganglions axillaires sont envahis dans
11% des cas lors du curage complet où le GS était positif unique-
ment en immunohistochimie. Ces chiffres concordent avec les
taux de faux négatifs décrits dans les études initiales.
Un certain nombre d’arguments plaident en faveur du curage
axillaire systématique en cas de micrométastase du ganglion sen-
tinelle, notamment lors d’une tumeur de plus de 20 mm (seule la
taille tumorale a une valeur prédictive), même si toutefois, le taux
de récidives demeure relativement faible et nettement inférieur au
taux de faux négatifs : de l’ordre de 0,21% à 3 ans. Certaines situa-
tions nécessitent encore des études avant de statuer, comme dans
le cas des tumeurs de type tubuleux/colloïde/médullaire (3).

La Lettre du Sénologue - n° 33 - juillet-août-septembre 2006
Congrès
Congrès
34
Figure 4.
Bénéce signicatif du docétaxel après réponse partielle
aux anthracyclines en néoadjuvant.
Enfin, la valeur pronostique de la micrométastase, proche de
celle d’un N+, semblerait suffir à poser l’indication de chimio-
thérapie adjuvante.
En définitive, de nombreuses questions ne sont pas encore
résolues et la participation aux études en cours permettrait
d’obtenir quelques réponses.
Ganglion sentinelle et carcinome canalaire in situ
D’après Catherine Bouteille (Saint-Étienne)
Le risque d’atteinte ganglionnaire dans les carcinomes canalaires
in situ est théoriquement nul, mais il existe en réalité dans environ
1,5% des cas et dépend de la taille clinique, identifiée comme le seul
facteur prédictif indépendant (4). Il n’y a ainsi, selon les auteurs,
aucune indication à réaliser un ganglion sentinelle et les Standard
Option Recommandations ne préconisent pas le ganglion senti-
nelle en cas de traitement conservateur, mais il peut être proposé
si les lésions sont étendues et relèvent d’une mastectomie ou en
cas de suspicion de microinvasion sur la biopsie percutanée.
Là encore, certaines questions se posent quant à l’attitude à
adopter lors d’un GS+ dans le cadre d’une mastectomie avec
reconstruction mammaire immédiate ou d’une oncoplastie ;
ou lors d’une récidive sous forme d’un carcinome canalaire in
situ après traitement conservateur sans curage ou après réali-
sation d’un ganglion sentinelle.
Traitements néoadjuvants : pour quelles patientes ?
D’après Brigitte Sigal-Zafrani (Paris),
Lydie Aimard (Marseille), Bruno Coudert (Dijon),
Sylvia Giard (Lille), Anne Tardivon (Paris)
Si le traitement néoadjuvant permet une augmentation du
taux de conservation mammaire, en revanche, il n’influence
pas la survie globale, ni la survie sans récidive. Toutefois, le
concept de traitement néoadjuvant évolue : c’est une situation
clinique unique qui permet d’analyser la réponse tumorale in
vivo ainsi que des facteurs prédictifs de réponse morphologi-
ques, immuno-phénotypiques et génomiques.
Dans le cas d’une patiente avec tumeur d’apparition récente de
35 mm, la question d’un traitement néoadjuvant doit être abor-
dée. Si la patiente informée est d’accord pour cette stratégie, le
bilan initial (mammographie et échographie) va permettre de
vérifier si la lésion est unique ou multifocale, si les lésions sont
mesurables de manière fiable et le statut ganglionnaire. Dans ce
cadre, la réalisation d’une IRM peut être intéressante à chaque
fois que l’on se retrouve devant des seins denses ou hétérogènes.
L’IRM a également un intérêt pour l’évaluation de la réponse
tumorale en cours et en fin de traitement néoadjuvant. À venir,
l’IRM à 3 Tesla et le TEP pour mieux évaluer la réponse.
Le prélèvement biopsique est le document histologique de
référence qui, outre le type histologique et le grade, nous ren-
seigne sur des critères prédictifs de réponse aux traitements :
l’index de prolifération, les récepteurs hormonaux et le statut
Her2. Une cytoponction ganglionnaire est souhaitable en cas
de ganglion palpable. L’histologie sera répétée lors de l’exérèse
chirurgicale afin dévaluer la réponse au traitement et, notam-
ment, la réponse complète histologique.
L’ensemble de ces renseignements oriente vers le type de
traitement néoadjuvant : chimiothérapie ou non, le type
de chimiothérapie, hormonothérapie ou non et sa place. La
chimiothérapie peut être 6 cycles de FEC 100 ou un schéma 3
FEC 100- 3 docétaxel 100. En effet, certaines études plaident
en faveur du schéma séquentiel avec le docétaxel qui a démon-
tré un bénéfice en survie sans récidive locale et sans maladie,
voire en survie globale à 5 ans (5-7) (figure 4).
Quant à la radiothérapie, les associations radio-chimiothé-
rapie n’ayant pas démontré d’avantage substantiel, elle reste
réservée au traitement postopératoire.
Les nouvelles voies de développement en matière de radiothé-
rapie consistent en l’association aux thérapies ciblées qui of-
friraient l’avantage d’une activité sur l’hétérogénéité tissulaire
résiduelle par la diversité de leurs modes d’actions. En effet,
l’administration d’inhibiteurs au récepteur de l’EGF laisse en-
trevoir une radio sensibilisation par altération des réparations
des lésions radio induites, facilitation de l’apoptose et action
sur la repopulation en cours de traitement.
PRISE EN CHARGE LOCORÉGIONALE
APRÈS TRAITEMENT NÉOADJUVANT
Critères et conditions d’une chirurgie de qualité
D’après Jean-Yves Seror (Paris)
La biopsie, parfois échoguidée, nous renseigne non seulement
sur le type histologique, mais aussi sur les facteurs pronostiques.
Le bilan initial radiologique est primordial pour apporter une
précision sur la taille de la tumeur nécessitant parfois une IRM
comme dans les carcinomes lobulaires. Elle apporte, en outre,
des éléments prédictifs de la conservation mammaire. En revan-
che, il peut y avoir une sur- ou une sous-estimation de la lésion : la
réponse complète en IRM ne permet pas d’éviter l’exérèse chirur-
gicale. L’IRM peut compléter la mammographie et l’échographie
dans l’évaluation de la réponse au traitement néoadjuvant.

La Lettre du Sénologue - n° 33 - juillet-août-septembre 2006
Revue de presse
35
Congrès
Congrès
35
Figure 5.
Essai EVA : GS avant chimiothérapie néoadjuvante.
Enfin, la pose de clips de repérage sous échographie est néces-
saire au chirurgien.
Conduite à tenir sur la tumeur ?
Conduite à tenir sur les aires ganglionnaires ?
D’après Bernard Flipo (Nice)
Le traitement néoadjuvant s’il permet d’augmenter le taux de
traitements conservateurs, pose quelques questions sur les li-
mites géographiques du geste chirurgical pour éviter le maxi-
mum de récidives locales.
Quant à la chirurgie des aires ganglionnaires, le curage axil-
laire pourrait être évité et le ganglion sentinelle aurait une va-
leur prédictive intéressante. Le protocole français EVA étudie,
après chimiothérapie néoadjuvante par un schéma séquen-
tiel FEC100 suivi de docétaxel 100, la pertinence et l’intérêt
du curage axillaire, le taux d’identification et de stérilisation
du ganglion sentinelle et la concordance entre GS et curage
axillaire négatif, corrélée à la réponse histologique mammaire
(figure 5).
Place d’un traitement adjuvant
après un traitement néoadjuvant
D’après David Azria (Montpellier)
La radiothérapie sur le sein est systématique en cas de chirur-
gie conservatrice, mais l’oncoplastie complique l’application
du “boost” qui nécessitera des techniques de simulation vir-
tuelle. En cas de mastectomie, il n’y a aucune recommandation
claire sur les indications de la radiothérapie. De même, l’atti-
tude sur les aires ganglionnaires n’est pas univoque, surtout
en cas de pN-.
La chimiothérapie adjuvante après une chimiothérapie pre-
mière a été étudiée par l’équipe d’Hortobagyi qui a démontré
un bénéfice en survie sans récidive (8). Mais si le traitement
néoadjuvant est optimal, il ne semble pas nécessaire de le
compléter en adjuvant. Après une hormonothérapie néoad-
juvante, la question de la chimiothérapie adjuvante demeure
sans réponse.
Quant aux thérapies ciblées, le trastuzumab, notamment, doit
bien sûr être poursuivi en adjuvant, la question reste posée en
cas de radiothérapie concomitante…
GÉNÉTIQUE ET CANCER
Quelle prise en charge conseiller aux femmes
avec une mutation BRCA1/2
D’après Pascal Pujol (Montpellier)
L’identification du risque de cancer du sein et de l’ovaire par
l’oncogénétique entraîne la nécessité d’un dépistage précoce, dès
30 ans, compte tenu de la précocité de l’apparition des tumeurs
dans cette population. À cet égard, l’IRM apparaît comme l’exa-
men radiologique de choix du fait de sa très grande sensibilité
et de sa spécificité équivalente à celle de la mammographie. La
mastectomie prophylactique, proposée parfois en cas de pre-
mier cancer du sein, réduit le risque élevé de cancer controlaté-
ral, mais compte tenu de l’impact de ce geste, c’est la demande
de la patiente qui pèsera dans la balance bénéfice-risque.
En revanche, la validité du dépistage ovarien est controversée.
L’ovariectomie prophylactique peut ainsi être proposée après
40 ans en l’absence de projet parental. Elleréduit le risque de
plus de 95%. L’ovariectomie réduit également le risque de can-
cer du sein par l’effet anti-estrogénique. Le traitement préven-
tif hormonal par les SERM ou les inhibiteurs de l’aromatase
constitue une alternative probablement efficace.
Prise en charge multidisciplinaire
des patientes à haut risque
D’après Rémy Salmon (Paris)
Chez des femmes porteuses des gènes BRCA1/2 mutés, il
existe quatre situations cliniques :
En l’absence de lésion maligne, la prise en charge multidisci-
plinaire s’impose, de même que les délais de réflexion de la
patiente. Le poids de l’histoire familiale est majeur dans la dé-
cision thérapeutique.
En cas de lésion in situ unilatérale, le traitement est classique
et le geste sur le sein controlatéral dépend, là encore, de l’his-
toire familiale.
En cas de carcinome invasif, le geste controlatéral prophylac-
tique est réalisé dans le même temps ou secondairement selon
la taille de la tumeur actuelle.
Sur une récidive après traitement conservateur, la mastecto-
mie prophylactique pourra être réalisée secondairement.
CONCLUSION
Ces troisièmes Rencontres de Chirurgie du Cancer du sein ont
ainsi été l’occasion de mises au point, de présentations d’ac-
tualités dans le cadre de la prise en charge du cancer du sein à
un stade précoce. Elles ont permis aux chirurgiens, massive-
ment présents à cette réunion, de prendre connaissance des
dernières avancées dans ce domaine et d’échanger sur leurs
 6
6
1
/
6
100%