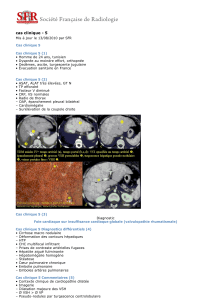
Méthodes pharmacologiques d’évaluation du dépôt pulmonaire des traitements inhalés

20 | La Lettre du Pneumologue • Vol. XII - n° 1-2 - janvier-février-mars-avril 2009
MISE AU POINT
Méthodes pharmacologiques
d’évaluation du dépôt
pulmonaire des traitements
inhalés1
Pharmacological assessment of inhaled drug delivery
to the lung
P.O. Girodet*, M. Molimard*
1 La Lettre du Pharmacologue 2008;
22(4):5-11.
* Département de pharmacologie, uni-
versité Victor-Segalen, Bordeaux-2.
L
es médicaments inhalés sont fréquemment
utilisés pour le traitement de l’asthme ou de
la bronchopneumopathie chronique obstruc-
tive (BPCO). Après l’administration, une propor-
tion importante de la dose émise (25 % à 90 %) se
dépose dans l’oropharynx (1). Pour cette fraction,
le passage dans la circulation systémique s’effectue
via une absorption locale dans la cavité buccale ou,
après déglutition, dans le tractus gastro-intestinal.
Concernant la fraction de dose délivrée dans l’arbre
trachéo-bronchique, la clairance des particules
inhalées est régulée par le transport mucociliaire
et l’absorption dans la circulation systémique par
l’épithélium des voies aériennes. La fraction absorbée
par voie digestive ou respiratoire peut induire des
effets systémiques mais seule la fraction inhalée
est responsable d’effets thérapeutiques. Il est donc
important d’étudier le dépôt pulmonaire des théra-
peutiques administrées par voie inhalée.
De nombreux facteurs déterminent le dépôt pulmo-
naire des traitements inhalés, tels que l’utilisation
des systèmes d’inhalation par les patients, le débit
inspiratoire lors de l’inhalation, la dose émise, la
taille des particules inhalées et les caractéristiques
géométriques des voies aériennes variables selon la
sévérité des maladies respiratoires. Par conséquent,
les variations de quantité de médicaments attei-
gnant le poumon et les variations de distribution
des particules émises impliquent des différences
dans la distribution du médicament dans les voies
aériennes, l’efficacité clinique, la biodisponibilité
systémique et les effets indésirables des traite-
ments inhalés. Les impacteurs en cascade sont
utilisés en tant que modèle du dépôt pulmonaire
in vitro (2). Une telle évaluation des propriétés
aérodynamiques par cette méthode est intéressante
pour les phases de développement et le contrôle
de la qualité des médicaments, mais ses résultats
ne sont pas toujours transposables in vivo (3). Par
conséquent, il est important d’utiliser des méthodes
cliniques pour déterminer le dépôt pulmonaire,
principalement pour les nouveaux systèmes d’in-
halation et les nouvelles formes galéniques avant
l’Autorisation de mise sur le marché. De nombreux
essais cliniques comportent une étude du dépôt
pulmonaire pour démontrer une équivalence
entre de nouveaux dispositifs d’inhalation ou de
nouvelles formules galéniques et le produit d’ori-
gine. Par exemple, l’évaluation du dépôt pulmo-
naire est une étape nécessaire pour comparer un
aérosol-doseur pressurisé (pMDI) conventionnel
ABRÉVIATIONS
ACTH : hormone adrénocorticotrope – ASC : aire sous la courbe – BDP : béclométasone dipropionate
– BPCO : bronchopneumopathie chronique obstructive – Cmoy : concentration moyenne – Cmax :
concentration plasmatique maximale – CFC : chlorofluorocarbone – DPI : inhalateur de poudre
sèche (dry powder inhaler) – DEMM25-75 % : débit expiratoire maximal moyen de 25 % à 75 %
de la capacité vitale forcée – DEP : débit expiratoire de pointe – fL : fraction de dose déposée et
absorbée par le poumon – FO : biodisponibilité orale – fret : fraction de dose retenue par le système
d’inhalation – Fsyst : -biodisponibilité -systémique – GC/MS : chromatographie en phase gazeuse
couplée à la -spectrométrie de masse – HFA : hydrofluoroalkane – HPLC : chromatographie liquide
haute performance (high performance liquid chromatography) – pMDI : aérosol-doseur pressurisé
(pressurized metered-dose inhaler) – T1/2 : demi-vie plasmatique – Tmax : temps nécessaire pour
atteindre la concentration maximale – Vd : volume de distribution – VEMS : volume expiratoire
maximum seconde.

La Lettre du Pneumologue • Vol. XII - n° 1-2 - janvier-février-mars-avril 2009 | 21
Résumé
Le dépôt pulmonaire des traitements inhalés peut être évalué par des méthodes pharmacocinétiques et pharma-
codynamiques. Le choix de la méthode dépend de la classe médicamenteuse étudiée. Pour les médicaments sans
effet de premier passage hépatique, tels que les bêta-2 agonistes de courte durée d’action, l’étude pharmaco-
cinétique du dépôt pulmonaire doit être effectuée rapidement après l’inhalation afin de minimiser l’absorption
gastro-intestinale. Pour les molécules subissant un métabolisme important en rapport avec un premier passage
hépatique, telles que les corticostéroïdes inhalés, la concentration plasmatique de médicament est un reflet
indirect du dépôt bronchique. L’effet pharmacodynamique peut être évalué par les effets cliniques et les effets
indésirables potentiels des traitements inhalés. Chez l’asthmatique et le patient affecté de bronchopneumopa-
thie chronique obstructive, la réversibilité de l’obstruction bronchique après inhalation de bronchodilatateur
permet d’estimer le dépôt bronchique si l’obstruction bronchique initiale est significative. Pour comparer l’effet
dose-réponse entre corticoïdes inhalés sur des périodes supérieures à six semaines, la référence actuelle est la
méthode de Finney. L’analyse des effets indésirables des bêta-2 agonistes ou des corticostéroïdes administrés à
fortes posologies peut également être utilisée pour comparer le dépôt bronchique de différentes molécules.
Mots-clés
Voies aériennes
Biodisponibilité
Dépôt
Médicaments inhalés
Poumon
Pharmacodynamie
Pharmacocinétique
Summary
The assessment of drug delivery
to the lung in vivo may be
performed using either pharma-
cokinetic or pharmacodynamic
techniques. The choice of phar-
macological method depends
on drug class specificities. Phar-
macokinetic determination of
deposition to the lung for drugs
without hepatic first-pass, such
as short acting β2-agonist,
has to be performed shortly
after inhalation to minimize
the effect of gastrointestinal
absorption. For medication
undergoing important hepatic
first-pass metabolism such as
inhaled corticosteroid, plas-
matic concentration indirectly
reflects bronchial deposition.
Pharmacodynamic profile
should be assessed through
clinical effect and adverse
events induced by inhaled
drugs. Dose ranking of lung
deposition for bronchodilators
requires patient selection with
sufficient bronchial obstruction
to maintain room for improve-
ment after the first dose. To
assess dose effect relationship
between inhaled corticosteroid,
the Finney parallel line bioassay
is the reference method in at
least six weeks period study.
Analysis of side effect with high
doses of β2-agonist or inhaled
corticosteroid may also be used
to compare lung deposition.
Keywords
Airways
Bioavailability
Deposition
Inhaled drugs
Lung delivery
Pharmacodynamic
Pharmacokinetic
et un inhalateur de poudre sèche (DPI) ou un gaz
propulseur chlorofluorocarbone (CFC) à un gaz
propulseur, plus respectueux de l’environnement,
tel que l’hydrofluoroalkane (HFA). Actuellement,
les deux principales techniques disponibles in vivo
sont les études du dépôt pulmonaire des aérosols
radiomarqués et les méthodes pharmacologiques.
L’inhalation des aérosols radiomarqués implique
une mesure de la radioactivité pulmonaire par une
gammacaméra ou un compteur corporel total. Bien
que les études scintigraphiques constituent un outil
valable pour prédire le dépôt pulmonaire régional
et total, ainsi que le dépôt oropharyngé, la préci-
sion de cette technique est limitée par le processus
de détection en deux dimensions de ce système
(4). Des développements futurs sont nécessaires
pour l’utilisation en pratique courante de méthodes
d’imagerie en trois dimensions (tomographie par
émission de positons) [5]. Les études scintigra-
phiques présentent de nombreux inconvénients :
exposition aux irradiations, en particulier chez les
enfants (6), obtention compliquée de molécules
radiomarquées, difficultés pour interpréter le dépôt
dans certaines zones anatomiques dans l’espace
et accès limité aux dispositifs développés par les
firmes pharmaceutiques.
Par conséquent, les approches pharmacocinétiques
et pharmaco-dynamiques fournissent potentielle-
ment des informations complémentaires sur le dépôt
pulmonaire et sur les effets cliniques des thérapeuti-
ques administrées par voie inhalée. L’objectif de cette
revue est de présenter les principales méthodes phar-
macocinétiques et pharmacodynamiques utilisées
pour évaluer le dépôt pulmonaire des traitements
inhalés en précisant les limites et les intérêts de
chaque méthode.
Méthodes pharmacocinétiques
Les mesures pharmacocinétiques constituent des
indicateurs utiles pour établir une corrélation entre
le dépôt pulmonaire et la distribution plasmatique
des traitements inhalés. Certains paramètres phar-
macocinétiques tels que la demi-vie plasmatique
(T
1/2
) et le volume de distribution (Vd) dépendent
de la molécule et ne sont pas influencés par le dépôt
pulmonaire. Cependant, la variabilité du dépôt
pulmonaire entre plusieurs molécules peut résulter
des différences liées à la concentration plasmatique
maximale (Cmax) et à l’aire sous la courbe (ASC) des
concentrations plasmatiques. Il existe également
des caractéristiques pharmacocinétiques spécifiques
selon la classe médicamenteuse en question, en
particulier les traitements inhalés les plus fréquem-
ment utilisés en pneumologie, à savoir les bêta-2
mimétiques et les corticostéroïdes.
Agonistes des récepteurs
β2-adrénergiques inhalés
Concernant les bêta-2 mimétiques de courte durée
d’action, le paramètre pharmacocinétique le plus
simple pour calculer la biodisponibilité pulmonaire
est la mesure de l’absorption précoce du salbutamol
dans les 20 minutes suivant l’inhalation. Le subs-
tratum pharmacologique de cette mesure est que
l’absorption gastro-intestinale contribue seulement
à 0,3 % de l’absorption systémique globale dans
les 30 minutes suivant l’inhalation (7). À partir des
courbes de concentration plasmatique exprimées
en fonction du temps, un certain nombre de para-
mètres, tels que la C
max
, la concentration moyenne
pendant 20 minutes (Cav) et le temps nécessaire
pour atteindre la concentration maximale (T
max
)
permettent d’estimer le dépôt pulmonaire. Par
exemple, après inhalation de salbutamol (1 200 µg),
les valeurs de Cmax et Tmax sont respectivement
de 2,93 ng/ml et 10 minutes pour dix volontaires
sains dont la moyenne d’âge est de 20,5 ans avec
un volume expiratoire maximum seconde (VEMS)
à 112,1 % de la théorique (8). L’ASC est également
considérée comme un critère primaire pour évaluer
l’absorption systémique (9). Dans les essais cliniques,
l’absorption gastro-intestinale peut être réduite par
un rinçage buccal ou prévenue par l’administration
de charbon activé avant et après l’inhalation. Ainsi,
l’absorption gastro--intestinale étant exclue, les
taux plasmatiques reflètent le dépôt pulmonaire
et l’absorption.
L’utilisation de telles méthodes pharmacocinétiques
dans les études de bioéquivalence in vivo permet
de calculer un rapport de différence de Cmax, ce qui

22 | La Lettre du Pneumologue • Vol. XII - n° 1-2 - janvier-février-mars-avril 2009
Méthodes pharmacologiques d’évaluation du dépôt
pulmonaire des traitements inhalés
MISE AU POINT
constitue un indicateur de dose relative délivrée aux
poumons. Cet indice relatif permet la comparaison
de différentes formulations de médicaments inhalés,
de divers systèmes d’inhalation ou des inhalations
retardées en chambres d’inhalation.
Néanmoins, l’interprétation des paramètres phar-
macociné-tiques impose de prendre en compte
l’existence d’une maladie pulmonaire et la fonction
respiratoire. Le profil d’absorption pulmonaire d’une
inhalation de fénotérol (4 mg) a été évalué dans
deux études différentes utilisant le même système
d’inhalation et une posologie identique chez des
volontaires sains et des sujets asthmatiques (VEMS
moyen à 56 % de la théorique). Le pic de concen-
tration plasmatique de fénotérol est diminué d’un
facteur 2 pour les patientes asthmatiques (1,6 ng/ ml)
par rapport aux sujets témoins (3,1 ng/ml) [10]. Des
résultats similaires ont été publiés avec les nébuli-
sations de salbutamol, ce qui soulève l’hypothèse
selon laquelle un rétrécissement du calibre des voies
aériennes peut affecter le dépôt pulmonaire des
β2-mimétiques inhalés (11).
En pratique clinique, les études pharmacocinéti-
ques présentent un intérêt limité pour les agonistes
des récepteurs β2-adrénergiques inhalés, car les
doses administrées sont généralement faibles et
les concentrations plasmatiques qui en résultent
sont le plus souvent dans les limites des seuils de
détection. Cependant, la sensibilité des dosages est
améliorée par la chromatographie en phase gazeuse
couplée à la spectrométrie de masse (GC/MS). Alors
que le seuil de détection de la chromatographie
liquide haute performance (HPLC) avec détection
ultraviolet pour la concentration plasmatique de
salbutamol est de 0,2 ng/ml (12), la linéarité de la
méthode GC/MS est validée pour des concentrations
de salbutamol comprises entre 50 et 10 000 pg/ml
(13). Dans les études de bioéquivalence, les para-
mètres pharmacocinétiques sont nécessaires, mais
insuffisants pour évaluer la distribution pulmonaire
des molécules étudiées. Les méthodes granulomé-
triques constituent un complément nécessaire dans
cette optique.
Corticostéroïdes inhalés
Une faible proportion de la dose émise peut
atteindre la circulation systémique, puisque la
fraction de médicament avalé subit un important
effet de premier passage hépatique : 90 % pour
le budésonide et 99 % pour la fluticasone. O.J.
Dempsey et al. ont démontré que l’absorption
oropharyngée de fluticasone ne contribue pas
à l’activité systémique (14). L’intérêt du rinçage
buccal suivant l’inhalation est la prévention des
candidoses oropharyngées et non pas la réduction
des effets systémiques. La biodisponibilité systé-
mique des corticostéroïdes inhalés dépend donc de
la fraction médicamenteuse absorbée par les voies
aériennes via la vascularisation pulmonaire. Par
conséquent, pour ces médicaments métabolisés
de manière intense, le passage systémique dans
la circulation générale reflète le dépôt pulmo-
naire.
Cependant, la mesure des concentrations séri-
ques ne correspond pas aux besoins de techniques
précises pour évaluer la dose de médicament déli-
vrée au niveau du tissu pulmonaire. Étant donné
les propriétés lipophiles des corticostéroïdes, le
Vd est variable selon les molécules (tableau I).
Les valeurs de Cmax dépendent de ce paramètre.
Suivant l’inhalation de molécules avec une biodis-
ponibilité identique, les concentrations plasma-
tiques sont inversement proportionnelles au Vd
(figure 1). Ainsi, les médicaments hautement lipo-
philes avec un Vd élevé, tels que la fluticasone, ont
une activité systémique pour des concentrations
plasmatiques plus faibles par rapport à des médi-
caments moins lipophiles. Une simple mesure de
l’ASC n’est donc pas directement corrélée à la
distribution systémique.
Un correctif peut être apporté par une approche
méthodologique qui identifie le dépôt pulmonaire
en fonction du rapport de la fraction de la dose
déposée et de celle absorbée par le poumon (fL)
sur la biodisponibilité systémique (Fsyst) [15]. Ce
calcul, impliquant une évaluation de la biodis-
Tableau I. Caractéristiques pharmacocinétiques des corticostéroïdes inhalés.
T1/2 (h) Vd (l/kg) Clairance (l/mn) Disponibilité orale (%)
Béclométasone-17-monopropionate 2,7 6,1 2 41
Béclométasone dipropionate 0,5 < 1 2,5 –
Budésonide 2-3 2,7 0,9-1,3 6-13
Flunisolide 1,6 1,8 1 21
Fluticasone propionate 8-14 12,1 0,9-1,3 < 2
Triamcinolone acétonide 1,5 1,3 0,7 23
Abréviations : T1/2 : demi-vie plasmatique ; Vd : volume de distribution.

La Lettre du Pneumologue • Vol. XII - n° 1-2 - janvier-février-mars-avril 2009 | 23
Figure 1. Représentation schématique de la distribution systémique des corticostéroïdes
inhalés. Les corticostéroïdes hautement lipophiles (A) ont un volume de distribution (Vd)
potentiellement élevé, alors que les corticostéroïdes faiblement lipophiles (B) ont un Vd
inférieur. Considérant que la dose x est équivalente pour les médicaments A et B, la compa-
raison des concentrations plasmatiques (C) implique de tenir compte des valeurs de Vd.
Corticostéroïde inhalé
Médicament A x µg Médicament B x µg
Vd élevé Vd faible
C plasmatique faible
C plasmatique élevée
MISE AU POINT
ponibilité orale (F
O
) et l’absence de métabo-
lisme pulmonaire des médicaments étudiés (16),
s’énonce comme suit :
fL = Fsyst – FO.(1-fret)/(1-FO)
Les concentrations plasmatiques et urinaires de
médicament reflètent le dépôt pulmonaire global,
sans fournir d’information sur des profils de dépôts
localisés dans certaines régions anatomiques. Consi-
dérant la taille des particules, il a été démontré que
le dépôt pulmonaire des médicaments inhalés a
tendance à décroître avec l’augmentation de la
distance par rapport à la trachée. Un tel profil de
distribution pulmonaire a été établi pour des patients
ayant bénéficié d’une intervention chirurgicale thora-
cique, avec une administration préopératoire de trai-
tement inhalé (17). Par exemple, les concentrations
de fluticasone dans le tissu pulmonaire proximal sont
3 à 4 fois plus élevées que celles du poumon péri-
phérique après une inhalation d’une dose de 1 mg. Il
est bien évident que ces techniques ne permettent
pas la comparaison de différentes formulations en
pratique courante.
Méthodes
pharmacodynamiques
Selon une approche complémentaire des méthodes
pharmacocinétiques, les études pharmacodyna-
miques permettent dans certaines conditions
d’évaluer le dépôt pulmonaire des traitements
inhalés (tableau II). Les paramètres pharma-
codyna-miques étudiés varient en fonction de
la classe médicamenteuse, bronchodilatateurs
(β2-adrénergiques inhalés) ou anti-inflammatoires
(corticostéroïdes inhalés). Les critères de jugement
principaux comportent l’effet thérapeutique et
les événements indésirables induits par les trai-
tements inhalés.
Tableau II. Comparaison des méthodes pharmacocinétique et pharmacodynamique pour évaluer le dépôt pulmonaire des médicaments inhalés.
Études pharmacocinétiques Études pharmacodynamiques
Avantages
Reproductibilité Variables d’efficacité
Relation dose-réponse Mesure des effets indésirables
Comparaison entre le dépôt pulmonaire relatif et l’exposition systémique
relative
Relation dose-réponse pour les effets indésirables
Inconvénients
Absorption intestinale Variabilité interindividuelle
Faibles concentrations plasmatiques des médicaments Nécessité d’une marge d’amélioration pour les critères d’efficacité
Absence d’évaluation des variations régionales de dépôt pulmonaire Études à long terme pour les corticostéroïdes inhalés

24 | La Lettre du Pneumologue • Vol. XII - n° 1-2 - janvier-février-mars-avril 2009
Méthodes pharmacologiques d’évaluation du dépôt
pulmonaire des traitements inhalés
MISE AU POINT
Agonistes des récepteurs β2-
adrénergiques inhalés
Effets cliniques des agonistes β2-adrénergiques ◆
Les variables d’efficacité des bronchodilatateurs
de courte durée d’action sont souvent évaluées
avant et après l’inhalation d’une dose unique
(18). Par exemple, pour comparer deux agonistes
β2-adrénergiques administrés par aérosol-doseur
pressurisé dont la formulation diffère par le gaz
propulseur utilisé, la variation du VEMS par rapport
à l’état initial constitue fréquemment le critère de
jugement principal (13). Une diminution de l’hy-
perréactivité bronchique (effet bronchoprotecteur)
induite par les β2-adrénergiques peut être évaluée
par un test de provocation ventilatoire avec un
agent bronchoconstricteur tel que la métacholine.
Les scores de dyspnée et la consommation d’ago-
niste β2-adrénergique de courte durée d’action sont
susceptibles d’être pris en compte pour déterminer
l’effet des bronchodilatateurs de longue durée d’ac-
tion dans l’asthme et la BPCO. Ces paramètres sont
cependant des critères de jugement secondaires par
rapport au VEMS.
Les explorations fonctionnelles respiratoires ne
détectent pas de réponses significatives en termes
de bronchodilatation si le sommet de la courbe dose-
réponse est facilement atteint. Par exemple, pour
les bronchodilatateurs de courte durée d’action, la
première dose administrée ne doit pas induire une
réversibilité complète de l’obstruction. Ainsi, il est
important que les patients inclus dans les essais clini-
ques aient une obstruction des voies aériennes signi-
ficative avec une marge substantielle pour permettre
une amélioration de la fonction ventilatoire.
Effets indésirables des agonistes β2- ◆
adrénergiques
L’analyse des effets indésirables représente un outil
complémentaire pour étudier les caractéristiques
pharmacodynamiques des médicaments inhalés.
Chez les asthmatiques intermittents et persistants
légers, la plus faible dose d’agoniste β2-adrénergique
est à même de provoquer une réversibilité complète
d’une obstruction bronchique spontanée ou pharma-
cologiquement induite. Par conséquent, la compa-
raison des effets cliniques exercés par de fortes doses
de bronchodilatateurs est difficile à établir. L’analyse
des effets indésirables des β2-agonistes représente
une alternative intéressante par rapport aux critères
d’efficacité clinique classiques. Étant donné que les
effets indésirables des agonistes β2-adrénergiques
sont négligeables aux doses pharmacologiques,
de telles études sont conçues pour reproduire les
effets adverses potentiels induits par une consom-
mation importante de bronchodilatateurs lors d’un
asthme aigu grave. Pour les β2-agonistes, le pouls, le
tremblement des extrémités (19), l’hypokaliémie et
l’hypoglycémie sont classiquement étudiés bien que
leur survenue soit particulièrement rare en cas d’uti-
lisation à des doses pharmacologiques. S.J. Fowler et
al. ont comparé les paramètres pharmacocinétiques
validés antérieurement et la réponse systémique
aux agonistes β2-adrénergiques dans un échantillon
de volontaires sains (20). Suivant l’inhalation de
fortes doses de salbutamol (1 200 µg) par différents
systèmes -d’inhalation, les concentrations plasma-
tiques maximales et moyennes de salbutamol sont
corrélées positivement avec -l’hypokaliémie et le
tremblement. Une telle corrélation n’est pas mise
en évidence pour les pulsations cardiaques.
Corticostéroïdes inhalés
Effets cliniques des corticostéroïdes inhalés ◆
Par contraste avec les études portant sur les agonistes
β2-adrénergiques, des études menées sur le long
terme sont nécessaires pour mettre en évidence une
réponse clinique significative induite par les corticos-
téroïdes inhalés (21). Il est classiquement admis que
des modifications de la fonction ventilatoire appa-
raissent chez des patients traités par corticostéroïdes
inhalés pendant au moins 6 semaines. Les varia-
tions du VEMS et du DEMM 25-75 % représentent
les critères d’efficacité primaires pour cette classe
médicamenteuse. Dans un essai multicentrique,
W.W. Busse et al. ont comparé l’effet induit par des
doses croissantes de béclométasone dipropionate
(BDP) avec des gaz propulseurs de type CFC ou HFA
sur le contrôle de l’asthme (22). Les études scin-
tigraphiques antérieures ont démontré un dépôt
pulmonaire supérieur du BDP-HFA en raison d’une
plus faible distribution de taille des particules par
rapport au BDP-CFC (23). Les sujets affectés d’un
asthme persistant sont assignés de manière aléatoire
dans chacun des six groupes étudiés : 100 µg par jour,
400 µg par jour ou 800 µg par jour de BDP-HFA, ou
100 µg par jour, 400 µg par jour ou 800 µg par jour
de BDP-CFC-BDP pendant six semaines. Le résultat
principal est une amélioration significative de la
courbe dose-réponse pour le DEMM 25-75 % après
six semaines de traitement par BDP-HFA par rapport
au BDP-CFC. Cette étude indique que la posologie
de BDP-CFC doit être multipliée par 2,6 pour obtenir
une augmentation du VEMS, exprimé en pourcen-
 6
6
 7
7
1
/
7
100%