I) Les acides carboxyliques

1) Présentation :
I) Les acides carboxyliques :
Chapitre 8 : LES ACIDES CARBOXYLIQUES ET LEURS DERIVES S 5 F
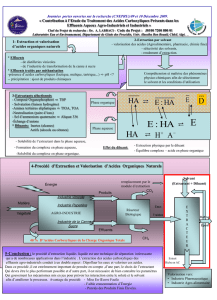
Le groupe fonctionnel acide carboxylique est
constitué d'un groupe carbonyle et d'un groupe
hydroxyle porté par le premier atome de carbone
d'une chaîne (carbone fonctionnel) :
R est un groupe résiduel, c’est soit une chaîne
commençant par un atome de carbone C, soit un
atome d'hydrogène H.
Pour un acide carboxylique qui dérive des alcanes, on pourra écrire une
formule semi-développée : CmH2m + 2 CnH2n + 1COOH (attention n = m - 1)
Le groupe carboxylique ─ COOH est relié à un groupe alkyle CnH2n + 1
linéaire ou ramifié qu'on notera R : R ─ COOH
groupe fonctionnel
acide carboxylique
groupe
hydroxyle
groupe
carbonyle

2) Nomenclature :
I) Les acides carboxyliques :
Chapitre 8 : LES ACIDES CARBOXYLIQUES ET LEURS DERIVES S 5 F
Pour nommer un acide carboxylique :
-
on remplace le e final du nom de l'hydrocarbure de même structure par le
suffixe oïque et l'on fait précéder le nom ainsi obtenu par le mot acide.
-
on numérote les atomes de carbone en attribuant le numéro 1 au carbone
fonctionnel, ce qui permet de préciser la position des ramifications.
Exemple : HCOOH acide méthanoïque ; CH3 ─ COOH acide éthanoïque ;
CH3 ─ CH2 ─ COOH acide propanoïque ;
HOOC ─ COOH acide éthanedioïque.
Exemple : acide 2-méthylpropanoïque.
Exemple : acide benzoïque.

3) Caractérisation des acides carboxyliques :
I) Les acides carboxyliques :
Chapitre 8 : LES ACIDES CARBOXYLIQUES ET LEURS DERIVES S 5 F
On peut caractériser l'apparition d'un
acide carboxylique par le fait que le
milieu devient acide : le B.B.T. (bleu
de bromothymol) donne une teinte
jaune.
La D.N.P.H. permet de caractériser la
présence du groupe carbonyle, ce
qui constitue la principale différence
avec un acide non carboxylique.

4) Propriétés physiques des acides carboxyliques :
I) Les acides carboxyliques :
Chapitre 8 : LES ACIDES CARBOXYLIQUES ET LEURS DERIVES S 5 F
La liaison O ─ H est davantage polarisée que dans le cas des alcools et il
peut s'établir un pont hydrogène entre l’atome d’hydrogène de ce groupe
hydroxyle et l’atome d’oxygène du groupe carbonyle plus riche en électrons
que l'atome d'oxygène d'un alcool.
Les températures d'ébullition des acides carboxyliques sont
supérieures à celles des alcools de masse molaire comparable.
A l'état solide ou liquide, les acides sont associés
sous forme de dimères dans lesquels il existe
deux liaisons hydrogène :
Alcool Formule qéb
(°C) Acide Formule qéb
(°C)
éthanol C2H5 ─ OH 78,8 éthanoïque CH3 ─ COOH 100,5
propan-1-ol C3H7 ─ OH 97,2 propanoïque C2H5 ─ COOH 118,0
butan-1-ol C4H9 ─ OH 117,7 butanoïque C3H7 ─ COOH 141,0
a) Température d’ébullition :

4) Propriétés physiques des acides carboxyliques :
I) Les acides carboxyliques :
Chapitre 8 : LES ACIDES CARBOXYLIQUES ET LEURS DERIVES S 5 F
Nous retiendrons que, comme pour les alcools :
La température d'ébullition augmente avec la masse molaire de l'acide.
Pour un même nombre d'atome de carbone, la température d'ébullition
diminue légèrement avec le nombre de ramifications.
Nom
Formule
Nom trivial
Masse
molaire
(g.mol-1)
qfus
(°C)
qéb
(°C)
méthanoïque
HCOOH
formique
46
8
100,5
éthanoïque
CH3 ─ COOH
acétique
60
17
118
propanoïque
C2H5 ─ COOH
propionique
74
- 22
141
butanoïque
C3H7 ─ COOH
butyrique
88
- 5
163
pentanoïque
C4H9 ─ COOH
valérique
102
- 35
187
hexanoïque
C5H11 ─ COOH
caproïque
116
- 2
205
a) Température d’ébullition :
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
1
/
17
100%