Traitement chirurgical D

DOSSIER THÉMATIQUE
La Lettre de l’Hépato-Gastroentérologue - n° 4 - vol. II - septembre 1999184
ous avons récemment assisté à un changement
considérable des modalités du traitement chirurgi-
cal du cancer du rectum et, de ce fait, des résultats
carcinologiques et fonctionnels. Les indications d’amputation
abdominopérinéale, suivie d’anus artificiel définitif, ont consi-
dérablement diminué. L’amputation est maintenant réservée aux
patients dont le cancer se situe dans les derniers centimètres du
rectum, et même dans certains centres spécialisés, aux seules
lésions qui envahissent le canal anal. Parallèlement, la fréquence
des récidives pelviennes a été réduite. La preuve de l’intérêt de
la radiothérapie préopératoire n’est plus à faire alors que l’exé-
rèse totale de l’environnement cellulo-lymphatique du rectum
(mésorectum) semble réduire plus encore le taux de récidive pel-
vienne. La préservation de l’innervation pelvienne, sympathique
et parasymphatique, évitant les séquelles urinaires et sexuelles,
est souhaitable. Elle n’altère pas les impératifs carcinologiques,
mais les facilite plutôt.
L’importance de ces changements, la rapidité avec laquelle ils ont
eu lieu expliquent qu’il y ait une disparité considérable dans la
prise en charge des cancers du rectum. La conférence de consen-
sus de 1994 avait été justifiée par une grande disparité des pra-
tiques. Le recours à la radiothérapie adjuvante, l’utilisation de la
chirurgie conservatrice, etc. variaient considérablement d’une
filière thérapeutique à une autre, sans que le stade évolutif de la
lésion ne le justifie, mais seulement parce que les habitudes thé-
rapeutiques étaient différentes. On constate aujourd’hui que selon
l’expérience et la formation du chirurgien qui prend le patient en
charge, les résultats, qu’ils soient carcinologiques ou fonction-
nels, sont très différents. Cela signifie, pour un patient, que le
risque d’avoir un anus artificiel et des troubles sexuels, ainsi que
ses chances de guérison sont influencés autant par le choix de ses
médecins que par la gravité de sa maladie.
EXTENSION DES INDICATIONS
DE LA CHIRURGIE CONSERVATRICE
Envahissement néoplasique
Aux débuts de la chirurgie du cancer du rectum, il a été rapporté
des cas d’extension microscopique de plusieurs centimètres au-
dessous du pôle inférieur de la lésion. Cette constatation avait
justifié que l’exérèse soit large, vers le bas, enlevant au moins
5 cm de tissu apparemment sain, et sacrifie de ce fait volontiers
le sphincter. Il est maintenant admis que ces cas sont l’exception
et correspondent à des lésions évoluées qui bloquent les relais
lymphatiques et entraînent une extension rétrograde. Aucune exé-
rèse aussi large soit-elle ne permet de les guérir (1, 2).
En fait, dans environ 80 % des cas, les limites microscopiques
distales du cancer correspondent aux limites macroscopiques.
Dans 10 à 15 % des cas, il existe une extension microscopique
limitée à quelques millimètres. Pour cette raison, on doit enlever
par sécurité 2 cm de rectum sain au-dessous de la lésion.
Ainsi, le cancer du rectum, à la différence des autres cancers du
tube digestif, notamment ceux de l’œsophage et de l’estomac, a
rarement une extension intra-pariétale microscopique au-delà de
la lésion, et cette extension, lorsqu’elle existe, est très limitée.
Certes, il y a des cas où l’extension peut aller au-delà de cette
limite, jusqu’à 5 voire 7 cm, mais ces cas sont exceptionnels. Ils
correspondent à des lésions évoluées. Dans aucun cas, le sacri-
fice du sphincter n’a permis de les guérir (39).
Traitement chirurgical
●
F. Lazorthes
*
* Service de chirurgie générale et digestive, hôpital Purpan, Toulouse.
■La prise en charge thérapeutique des cancers du rectum a
fait l’objet au cours des quinze dernières années de change-
ments majeurs. La rapidité avec laquelle ils sont survenus est
à l’origine d’une disparité considérable des pratiques ainsi que
des résultats thérapeutiques.
■Le risque de récidive pelvienne et la survie à long terme sont
peu influencés par l’exérèse de tissu sain au-dessous du pôle
inférieur de la tumeur : c’est ce qui assure l’essor de la chi-
rurgie conservatrice.
■L’exérèse totale du mésorectum réduirait la fréquence des
récidives locales à environ 5 à 10 %, même en l’absence de
radiothérapie.
■La préservation de l’innervation pelvienne évite les séquelles
urinaires et sexuelles et est la façon la plus sûre d’enlever la
totalité du mésorectum.
■Il est prouvé que la réalisation d’un réservoir colique lors
d’une anastomose colo-anale améliore le résultat fonctionnel.
POINTS FORTS
POINTS FORTS
N

La Lettre de l’Hépato-Gastroentérologue - n° 4 - vol. II - septembre 1999 185
Ces constatations ont assuré l’essor de la chirurgie conservatrice
de la fonction sphinctérienne.
Évolution des techniques chirurgicales
L’amputation abdominopérinéale suivie d’anus artificiel définitif
a été longtemps le traitement standard des cancers du rectum, en
particulier de ceux accessibles au toucher rectal. Il y a eu, au cours
des vingt dernières années, une augmentation explosive des indi-
cations de chirurgie conservatrice, au point que l’amputation est
devenue l’exception.
Les raisons sont multiples. Elles sont d’abord carcinologiques. Le
fait que les limites microscopiques et macroscopiques distales du
cancer du rectum soient généralement superposées explique que
de multiples études aient montré, de façon concordante, que l’éten-
due de l’exérèse distale de tissu apparemment sain n’a pas d’in-
fluence pronostique au-delà d’une marge minimum de 2 cm (2, 3).
L’essor de la chirurgie conservatrice a aussi, et sans doute tout autant,
été liée aux possibilités apportées par de nouvelles modalités d’ana-
stomose digestive. Il s’agit des sutures mécaniques et des anasto-
moses endo-anales. Elles permettent d’effectuer des anastomoses
basses dans de bonnes conditions de sécurité. La mortalité et les
complications de la chirurgie conservatrice n’ont pas été altérées
par rapport à celles de l’amputation abdominopérinéale (2).
La question consistant à savoir si les résultats carcinologiques de
la chirurgie conservatrice sont comparables à ceux de l’amputa-
tion est posée depuis les débuts de cette chirurgie. Il n’y a eu
aucune étude randomisée comparant ces deux techniques. La vali-
dation de la chirurgie conservatrice s’est donc basée sur des études
historiques, souvent rétrospectives. En raison des biais inhérents
à ce type d’étude, et en particulier du fait que le choix de l’une
ou de l’autre technique a sans doute été sélectif, on doit conti-
nuer à contrôler que la préservation sphinctérienne n’altère pas
la survie et le risque de récidive. Les études les plus récentes,
comme la plupart des précédentes le confirment (2, 4).
Dans ses recommandations, la conférence de consensus de 1994
considérait validée la chirurgie conservatrice des cancers du tiers
supérieur du rectum et du tiers moyen. À l’inverse, elle jugeait
que pour les lésions les plus basses, l’amputation abdomino-
périnéale restait le “Gold standard”. Depuis, plusieurs séries pros-
pectives de proctectomie totale avec anastomose colo-anale pour
cancer du bas rectum ont été publiées ; elles ont concerné, soit
exclusivement des cancers du tiers inférieur du rectum (5), soit
des cancers du tiers inférieur et du tiers moyen (6-8). La survie
à cinq ans a été dans ces séries de 70 à 75 %, c’est-à-dire au moins
égale à celle qui est obtenue habituellement après amputation. Il
semble donc que la chirurgie conservatrice des cancers du tiers
inférieur du rectum (c’est-à-dire ceux qui sont situés à 7 cm et
moins de la marge de l’anus) est aussi justifiée que celles des
lésions sus-jacentes. Heald considère même que c’est le traite-
ment de choix et que l’amputation ne doit plus être considérée
comme le “Gold standard” (9). Il a relevé 47 % de récidives après
amputation et 4 % après chirurgie conservatrice. Il considère que
l’amputation ouvre des plans de dissection favorisant les greffes
Tumeur primitive (T)
Tis Carcinome in situ : tumeur intra-épithéliale
ou envahissant la
lamina propria
(intra-muqueuse)
sans extension à la sous-muqueuse à travers
la
muscularis mucosae.
T1 La tumeur envahit la sous-muqueuse
sans la dépasser
T2 La tumeur envahit la musculeuse sans la dépasser
T3 La tumeur envahit, à travers la musculeuse,
la sous-séreuse (sans atteinte du revêtement
mésothélial) et le tissu péricolique non
péritonéalisé ou le tissu périrectal
T4 La tumeur perfore le péritoine viscéral
et/ou envahit les organes de voisinage
Ganglions régionaux (N)
N0 Absence de métastase ganglionnaire
N1 Métastase(s) ganglionnaire(s) lymphatique(s) ≤3
N2 Métastases ganglionnaires lymphatiques > 3
Nx Statut ganglionnaire non évaluable
Métastases (M)
M0 Absence de métastase
M1 Métastases à distance (l’atteinte des ganglions
iliaques externes ou iliaques communs
est considérée comme M1)
Mx Statut métastatique inconnu
Cancers du rectum : état des limites d’exérèse proximale,
distale et latérale (notion de résidu tumoral)
R0 Limites d’exérèse toutes saines
(absence de résidu tumoral microscopique)
R1 Limites d’exérèses non saines
(quand il existe des résidus tumoraux micro-
scopiques sur une ou plusieurs limites d’exérèse)
R2 Présence d’un résidu tumoral macroscopique
mentionné par le chirurgien
Cancers colorectaux : classification TNM 1997.
Nombre minimum de ganglions examinés : 12
Nodule tumoral > 3 mm situé dans les tissus périrectaux
ou péricoliques (avec ou sans tissu ganglionnaire résiduel)
= ganglion métastatique (jusqu’à 3 mm : classer en T)
TNM Dukes Astler-Coller
Stade 0 Tis N0 M0 A A
Stade I T1 N0 M0 A A
T2 N0 M0 A B1
Stade II T3 N0 M0 B B2
T4 N0 M0 B B2
Stade III T1-T2 N1-2 M0 C C1
T3-T4 N1-2 M0 C C2
Stade IV tous T tous N M1 D
Équivalence entre les classifications.

DOSSIER THÉMATIQUE
La Lettre de l’Hépato-Gastroentérologue - n° 4 - vol. II - septembre 1999186
tumorales. En faveur de cette hypothèse, il constate que les réci-
dives périnéales sont exclusivement le fait de l’amputation.
Selon le niveau du pôle inférieur de la lésion et l’étendue de l’exé-
rèse, la continuité digestive est assurée par anastomose colorectale
ou colo-anale. La qualité du résultat fonctionnel dépend de la hau-
teur du rectum restant. Lorsqu’il reste 5 cm de rectum, le résultat
fonctionnel est généralement bon (10). En revanche, les anastomoses
colo-rectales basses et les anastomoses colo-anales n’ont pas tou-
jours le résultat fonctionnel attendu, surtout durant les premiers mois.
Le fractionnement des selles est le trouble le plus habituel. C’est
l’évacuation itérative de petites quantités de selles. Une sensation de
plénitude rectale et de besoin d’exonérer réapparaît à bref intervalle
et cela se répète sur une période de temps prolongé allant parfois jus-
qu’à une ou deux heures, notamment la nuit. Ce trouble est souvent
majoré par une incapacité à différer l’exonération. Elle altère la conti-
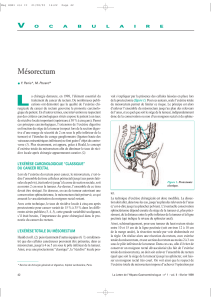
nence et entraîne des souillures. La reconstruction d’un réservoir rec-
tal par une poche colique en J permet d’éviter le fractionnement des
selles et les urgences (figure 1). Dans notre expérience, comme dans
celle de nombreux auteurs, les résultats ont été améliorés par rap-
port à ceux des anastomoses colo-anales sans réservoir. Par prudence,
la conférence de consensus de 1994 avait recommandé d’attendre le
résultat des études randomisées alors en cours. Elles ont depuis été
publiées et ont confirmé l’utilité du réservoir (11-15).
MODALITÉS D’EXÉRÈSE
Influence de l’opérateur
La variabilité du résultat carcinologique, à stade évolutif iden-
tique, est le problème majeur du traitement du cancer du rectum.
Une variabilité d’une telle ampleur n’est constatée dans le trai-
tement d’aucun autre cancer.
Le taux moyen de récidive pelvienne est, en l’absence de radio-
thérapie adjuvante, de l’ordre de 25 à 30 %. C’est ce qui a été
constaté dans le bras témoin de la plupart des essais thérapeutiques
de radiothérapie adjuvante, y compris le plus récent (16). C’était
d’ailleurs le taux retenu lors de la conférence de consensus. Les
variations sont toutefois considérables allant, selon les séries, de 4
à 40 %. Cette différence est réelle et ne s’explique pas seulement
par des biais de recrutement ou des critères de diagnostic de réci-
dive différents. Elle dépend de l’opérateur, c’est-à-dire de sa capa-
cité à enlever plus ou moins complètement la tumeur. Autrement
dit, beaucoup de cancers qui récidivent dans le pelvis auraient été
probablement guéris par une meilleure exérèse chirurgicale.
Sur la base d’études anglaises, la conférence de consensus de
1994 soulignait l’importance de la technique chirurgicale (17,
18). Dans les recommandations, il était dit : “la qualité de l’exé-
rèse chirurgicale est un facteur primordial du pronostic”, ainsi
que : “l’expérience du chirurgien est un facteur essentiel de réus-
site”. Plus récemment, trois études réalisées dans d’autres pays
ont confirmé l’influence de l’opérateur sur le résultat carcinolo-
gique et en ont précisé les raisons. Dans une étude coopérative
allemande, le taux de récidive a varié de 1 à 10 selon l’opérateur
(19). Le Stockholm Rectal Cancer Study Group, sur la base de
1 399 patients inclus dans deux essais prospectifs sur la radio-
thérapie préopératoire, a constaté que l’expérience de l’opérateur
influence le risque de récidive locale, mais aussi la survie à dis-
tance (20). Au Canada, Porter a constaté que le taux de récidive
et la survie varient considérablement avec le chirurgien (21). Il a
montré que la formation en chirurgie colorectale était un facteur
aussi important que l’expérience (tableau I).
La raison exacte de cette variabilité n’est pas connue avec certi-
tude. C’est dire l’intérêt de l’hypothèse de Heald qui l’a fait
dépendre de l’exérèse plus ou moins complète du mésorectum .
Bases anatomopathologiques de l’exérèse
Alors que l’on constatait l’influence pronostique minime de l’éten-
due de l’exérèse sous-jacente à la tumeur, au-delà de 2 cm, les ana-
tomopathologistes et les chirurgiens de Leeds montraient en 1986
l’importance décisive de l’envahissement des marges d’exérèses
latérales (22). Ils constataient que cet envahissement est le facteur
qui conditionne le plus le risque de récidive locorégionale.
Huit ans plus tard, ils confirmaient ces résultats par l’étude de
141 patients traités par exérèse potentiellement curative (23).
Trente-cinq avaient des marges périrectales envahies et 23 réci-
divaient dans le pelvis (66 %) ; 106 avaient des marges péri-
rectales saines et seulement 9 récidivaient, soit 8,4 %. L’enva-
Figure 1. A : Anastomose colo-anale ou colorectale basse directe.
B : Anastomose colo-anale ou colorectale avec réservoir en J.
Tableau I. Influence de l’opérateur (21).
Récidive (%) Survie 5 ans (%)
Chirurgien colorectal
Oui 13 60
Non 37 43
Plus de vingt résections
Oui 26 53
Non 42 38
AB

La Lettre de l’Hépato-Gastroentérologue - n° 4 - vol. II - septembre 1999 187
hissement des marges latérales avait multiplié par douze le risque
de récidive locale, mais aussi par trois le risque de décès par can-
cer. Ces résultats étaient confirmés par d’autres études (24, 25).
Mais, en 1998, l’équipe de Leeds refaisait pour la troisième fois
la même évaluation (26). Entre temps, leur technique chirurgicale
avait changé. L’exérèse totale du mésorectum avait remplacé l’exé-
rèse traditionnelle. Les résultats changeaient. Cent cinquante-deux
patients étaient traités à visée curative. Vingt avaient des marges
périrectales envahies et 3 récidivaient dans le pelvis (15 %), alors
que 132 avaient les marges saines et que 14 récidivaient (11 %).
La discordance entre les résultats de 1994 et ceux de 1998 semble
liée à la qualité de l’exérèse. Lorsque l’exérèse est défectueuse,
les marges d’exérèses périrectales sont souvent envahies et res-
ponsables d’un taux élevé de récidives pelviennes ; l’un et l’autre
témoignent de la mauvaise qualité de l’exérèse. En revanche, lors-
qu’une exérèse totale du mésorectum est réalisée, l’envahisse-
ment circonférentiel est plus un indicateur d’évolution de la mala-
die que de chirurgie inadéquate. Les patients avec un
envahissement des marges circonférentielles décèdent de méta-
stases à distance avant de faire une récidive locale. L’étude de
Cawthorn allait déjà dans ce sens (27).
Le mésorectum
Le mésorectum est une entité anatomique et embryologique. C’est
l’atmosphère cellulo-ganglionnaire périrectale circonscrite par le
fascia recti. Le fascia recti distingue la notion moderne de méso-
rectum de l’anatomie classique qui le méconnaît. Le méso-
rectum, c’est-à-dire la graisse du pelvis, appartient embryologi-
quement au rectum et non au petit bassin. Cela explique qu’il soit
le champ de dissémination initiale du cancer et que son exérèse
soit la meilleure façon de réséquer la maladie locorégionale. Cette
notion anatomique n’est pas une hypothèse, elle est confirmée
quotidiennement par les exérèses rectales réalisées selon la tech-
nique d’exérèse totale du mésorectum.
L’exérèse totale du mésorectum est celle qui passe dans le plan
avasculaire, situé entre le fascia pariétal qui recouvre les parois du
petit bassin et le fascia viscéral, ou fascia recti, qui enveloppe le
mésorectum. Ainsi est enlevé tout le tissu cellulo-embryonnaire
qui entoure le rectum, tissu dans lequel se développe la maladie
locorégionale qu’est le cancer du rectum au stade B et C de Dukes.
Le plan d’exérèse classique est plus interne. Il passe à travers ce
que les traités classiques nomment les ailerons du rectum, et qui
est en fait du mésorectum, laissant ainsi une partie de ce méso sur
les parois latérales du pelvis ; ce qui explique la fréquence des
récidives pelviennes de la chirurgie conventionnelle.
Les promoteurs de cette technique, Heald en Angleterre et Encker
au Sloan Kettering NC à New York, ont eu le plus faible taux de
récidive de la littérature (28-30). En particulier, pour les cancers
Dukes B et C, c’est-à-dire ceux qui sont à haut risque, le taux de
récidive a été de 5 et 8 %, alors qu’aucune radiothérapie adju-
vante n’était réalisée. En faveur de cette hypothèse, on constate
que les équipes qui ont changé de technique pour utiliser l’exé-
rèse totale du mésorectum ont obtenu des résultats similaires à
ceux de Heald (31, 32). De plus, lorsque ces résultats sont com-
parés à ceux qui étaient obtenus avec la chirurgie convention-
nelle, ils s’avèrent nettement supérieurs. Dans l’expérience de
Arbmann, le pourcentage de récidive locorégionale est passé de
14 à 6 %, lorsque l’ablation totale du mésorectum a remplacé la
chirurgie conventionnelle (31). Dans celle des chirurgiens de
Leeds, le pourcentage était de 23 % et 11 %, selon que cette tech-
nique était ou n’était pas utilisée (23, 26) (tableau II).
Bien sûr, les comparaisons historiques ont peu de valeur. Il fau-
drait, par rigueur scientifique, réaliser des études avec tirage au
sort, entre chirurgie conventionnelle et exérèse du mésorectum,
comme cela a été fait pour la radiothérapie adjuvante. Toutefois,
il est vraisemblable qu’un tel essai ne sera jamais réalisé car peu
éthique : la différence paraît trop importante et l’exérèse du méso-
rectum a d’autres avantages.
La préservation des nerfs
L’ablation totale du mésorectum est une exérèse large, c’est
même une exérèse beaucoup plus large que l’exérèse conven-
tionnelle. C’est aussi, de façon paradoxale, celle qui est la plus
conservatrice du point de vue fonctionnel. En effet, elle peut être
associée à la préservation des plexus autonomes. Elle permet
ainsi d’éviter les séquelles urinaires et sexuelles.
La fréquence des troubles sexuels : l’anéjaculation et les troubles de
l’érection sont élevés après chirurgie rectale pour cancer. Elle dépasse
généralement 50 % et peut même aller jusqu’à 90 %. Elle semblait,
jusqu’à une date récente, inhérente à la nature même de l’exérèse
carcinologique. Pour des générations de chirurgiens, les séquelles
urogénitales, avec l’anus artificiel, étaient le prix de la guérison.
Après les urologues qui préservent les nerfs lors des prostactec-
tomies radicales, on a constaté en chirurgie rectale que l’impor-
tance des séquelles est proportionnelle à l’importance des lésions
neurologiques. Plus le sacrifice neurologique est important, et
plus les séquelles sont fréquentes.
L’évolution dans ce domaine a été très rapide. Nous considérions, il
y a peu de temps “qu’il n’était pas sûr que la préservation des nerfs
soit compatible avec une exérèse carcinologique”, aujourd’hui, cette
certitude paraît acquise (33). Préserver les nerfs, en les visualisant et
en passant à leur contact, est la meilleure façon d’être dans le bon plan
de dissection et d’assurer une ablation complète du mésorectum. La
visualisation des nerfs a donc aussi un intérêt carcinologique en plus
de son intérêt fonctionnel. Voir les nerfs est la seule façon de les pré-
server : ils risquent sinon d’être sectionnés ou réséqués sans que l’on
s’en rende compte. Dans la chirurgie conventionnelle, les nerfs
n’étaient pas vus et les malades avaient souvent des troubles sexuels.
Tableau II. Récidive locorégionale.
Exérèse Exérèse
conventionnelle du mésorectum
Norrkoping
(31)
14 % (19/134) 6 % (8/128)
Leeds
(23, 26)
23 % (32/141) 11 % (17/152)

DOSSIER THÉMATIQUE
La Lettre de l’Hépato-Gastroentérologue - n° 4 - vol. II - septembre 1999188
Au début de notre expérience de la préservation de l’innerva-
tion, nous l’utilisions de façon sélective pour les lésions les moins
évoluées, en pratique dans la moitié des cas (34). Actuellement,
parce qu’elle paraît aussi être la meilleure sur le plan carcinolo-
gique, cette technique est devenue la règle. Bien sûr, il y a des
cas où une partie des nerfs autonomes est envahie et doit être
enlevée, de même qu’il y a des cas, où une partie de l’appareil
urogénital doit également être enlevée.
Dans les cas où la préservation de l’innervation paraît totale, la
préservation de la fonction sexuelle n’est pas toujours assurée.
Dans notre expérience, comme dans celles des autres auteurs,
80 % des patients ont eu une érection et une éjaculation normales
après préservation complète de l’innervation (34-36). L’âge des
patients et le type de l’intervention influencent les résultats. Les
sujets de plus de 60 ans et ceux qui ont eu une amputation abdo-
minopérinéale plutôt qu’une intervention conservatrice du sphincter
ont des résultats moins bons (35).
Cancer du tiers moyen : anastomose colorectale basse
ou colo-anale
L’exérèse du mésorectum est essentiellement circonférentielle,
allant jusqu’à ses limites marquées par le fascia recti, mais elle
est aussi distale. Lorsque la lésion est évoluée, l’extension
néoplasique peut, en effet, s’étendre vers le bas sur plusieurs
centimètres sous la forme d’embols ganglionnaires ou extra-
ganglionnaires indépendants. Pour les cancers du tiers supérieur,
c’est-à-dire les lésions intra-péritonéales, il convient d’enlever
5 cm de mésorectum et, par facilité technique, la même longueur
de rectum. C’est donc une anastomose colorectale qui est réali-
sée. À l’opposé, pour les cancers du tiers inférieur, la totalité du
rectum et de son méso est enlevée. On réalise ensuite une ana-
stomose colo-anale ou une amputation abdominopérinéale.
Les lésions intermédiaires, c’est-à-dire celles qui sont situées sur le
tiers moyen, peuvent être traitées de plusieurs façons. Tradition-
nellement, elles le sont par anastomose colorectale après exérèse de
2 à 3 cm de rectum et de méso distal ; mais cette longueur semble
insuffisante pour ce qui est du méso. Heald a proposé une exérèse
totale du méso vers le bas et partielle du rectum, laissant ainsi un
moignon rectal dépourvu de méso et moins bien vascularisé. C’est
sans doute pour cette raison qu’il a constaté un pourcentage élevé
de fistules anastomotiques (37). C’est pourquoi il est tentant d’en-
lever le moignon rectal mal vascularisé et d’effectuer une anasto-
mose colo-anale sur réservoir. Ce type d’anastomose paraît assurer
un résultat fonctionnel égal (38) ou supérieur (39) aux anastomoses
colorectales très basses. Le choix entre ces différentes techniques,
faute d’informations suffisantes, reste controversé.
CONCLUSION
L’extension des indications de préservation sphinctérienne, la
reconstruction rectale, la préservation de l’innervation sexuelle
permettent d’éviter le plus souvent les séquelles majeures qui
caractérisaient le traitement chirurgical du cancer du rectum.
Alors que l’on considérait depuis plusieurs dizaines d’années
qu’il fallait se tourner vers les thérapeutiques adjuvantes pour
améliorer le résultat carcinologique, c’est de façon inattendue
l’amélioration de l’exérèse chirurgicale qui a transformé le risque
de récidive pelvienne et les chances de guérison. ■
Mots clés : Cancer du rectum – Chirurgie – Mésorectum –
Récidive locale.
RÉFÉRENCES BIBLIOGRAPHIQUES
1. Williams N.S. The rationale for preservation of the anal sphincter in patients
with low rectal cancer. Br J Surg 1984 ; 71 : 575-81.
2. Williams N.S. Sphincter saving resection and total reconstruction for low rec-
tal cancer. Colorectal Cancer. Clinical Surgery International. Churchill
Livingstone Ed. 1996.
3. Pollet W.G., Nicholls R.J. The relationship between the extent of distal clea-
rance and survival and local recurrence rates after curative anterior resection for
carcinoma of rectum. Ann Surg 1983 ; 70 : 159-63.
4. Hugier M., Chastang C., Houry S. et coll. Sphincter-saving resection, or not,
for cancer of the midrectum. Am J Surg 1997 ; 174 : 11-5.
5. Lazorthes F., Gamagami R., Chiotasso P. Coloanal anastomosis for distal third
rectal cancer ; a prospective study of the carcinologic results S11. ASCRS Annual
meeting 1998, San Antonio, Texas.
6. Cavalière F., Pemberton J.H., Cosimelli M. et coll. Coloanal anastomosis for
rectal cancer. Long-term results at the Mayo and Cleveland Clinics. Dis Colon
Rectum 1995 ; 38 : 807-12.
7. Paty P.B., Enker W.E., Cohen A.M. The treatment of rectal cancer by low ante-
rior resection with coloanal anastomosis. Ann Surg 1994 ; 219 : 365-73.
8. Mohiuddin M., Marks G. Patterns of recurrence following high-dose preope-
rative radiation and sphincter-preserving surgery for cancer of the rectum. Dis
Colon Rectum 1993 ; 36 : 117-26.
9. Heald R.J., Smedh R.K., Kald A. et coll. Abdominoperineal excision of the rec-
tum : an endangered operation. Dis Colon Rectum 1997 ; 40 : 747-51.
10. Lewis W.G., Holdsworth P.J., Stephenson B.M. et coll. Role of the rectum in
the physiological and clinical results of coloanal and colorectal anastomosis after
anterior resection for rectal carcinoma. Br J Surg 1992 ; 79 : 1082-86.
11. Hallböck O., Pahlman L., Krog M. et coll. Randomized comparison of
straight and colonic J pouch anastomosis after low anterior resection. Ann Surg
1996 ; 224 : 58-65.
12. Kusunoki M., Shoji Y., Yanagi H. et coll. Function after anoabdominal rectal
resection and colonic J pouch-anal anastomosis. Br J Surg 1991 ; 78 : 1434-8.
13. Lazorthes F., Chiotasso P., Gamagami R. et coll. Late clinical outcome in
randomized prospective comparison of colonic J pouch and straight coloanal
anastomosis. Br J Surg 1997 ; 84 : 1449-51.
Poumon : radio pulmonaire
Foie : échographie
Côlon : coloscopie
Rectum : échographie endorectale
Le lavement baryté, l’urographie, la cystographie, l’IRM, etc. ne
sont pas indiqués, sauf exception.
Le scanner peut être envisagé si l’échographie hépatique est
insuffisante.
Bilan préthérapeutique dans le cancer du rectum
 6
6
1
/
6
100%