thématique D Thérapeutiques

L’INSUFFISANCE CARDIAQUE
CONGESTIVE
L’insuffisance cardiaque congestive
(ICG) est le problème cardiaque numéro
un aux États-Unis (selon le National Cen-
ter for Health Statistics et l’AHA) et en
Europe de l’Ouest. Avec le vieillissement
de la population, la prévalence de l’ICG
augmente. Actuellement,aux États-Unis,
le nombre de patients atteints d’ICG aug-
mente de 500 000 par an, et seuls 2 000
d’entre eux peuvent être transplantés.
Idéalement, tous ces patients devraient
bénéficier d’une transplantation car-
diaque seule permettant un résultat pré-
dictible. Cependant, du fait de la pénurie
d’organes, il n’existe pas d’adéquation
entre le nombre potentiel de receveurs et
le nombre possible de donneurs ; de plus,
il y a un âge limite pour les receveurs
cardiaques.
LA CARDIOMYOPATHIE DILATÉE
La cardiomyopathie dilatée (CMD) idio-
pathique ou postischémique est très sou-
vent associée à une régurgitation mitrale
(RM) ; celle-ci est en rapport avec une
altération de la géométrie ventriculaire
(1, 2). Les conséquences fonctionnelles
La régurgitation mitrale fonctionnelle est une complication fré-
quente des cardiomyopathies dilatées et peut altérer gravement
le pronostic vital des patients en défaillance cardiaque. La meilleure
compréhension des mécanismes physiopathologiques de la régur-
gitation mitrale, conséquence du remodelage ventriculaire, et les nouveaux traitements chirurgicaux
qui en sont issus permettent une excellente correction de l’insuffisance mitrale ainsi qu’un remode-
lage ventriculaire primaire par la plastie de la base du ventricule gauche et secondaire par la
diminution de la tension pariétale.
Mots-clés :
Cardiomyopathie dilatée - Plastie mitrale - Remodelage ventriculaire.
Résumé
Résumé
Le Courrier de la Transplantation - Volume II - n o2 - avril-mai-juin 2002
63
DOSSIER
thématique
Thérapeutiques
alternatives
dans le domaine
de la
transplantation
cardiaque
Coordinateur : J.C. Chachques,
hôpital Européen Georges-Pompidou,
75015 Paris.
!Assistance biologique de l’insuffisance cardiaque
par cardiomyoplastie (tissulaire et cellulaire) et aortomyoplastie
J.C. Chachques, B. Cattadori, A. Berrebi, M.C. Iliou, P. Meimoun, A. Carpentier
"Chirurgie valvulaire mitrale chez les patients
atteints de cardiomyopathie dilatée -J.P. Couetil
!Resynchronisation atrio-biventriculaire - C.Alonso,T. Lavergne,
J. Ollitrault, J.Y. Le Heuzey, J.M. Darondel, M. Aitsaid, L. Guize
!Reduction ventriculoplasty -R.J.V. Batista
!Ventricular containment (Acorn Wrap) -
M. Acker
!Left ventricular assist device as a bridge
to heart transplantation: the Cleveland Clinic experience
J.L. Navia, P.R.Vega, C. Faber, N.G. Smedira, P.M. McCarthy
* Service de chirurgie cardiaque, hôpital Bichat-
Claude Bernard, 75018 Paris.
Chirurgie valvulaire mitrale chez les patients
atteints de cardiomyopathie dilatée
!
J.P. Couetil*

sont graves, avec un très mauvais pro-
nostic à court terme. La survie à un an
dans la plupart des séries est de 20 % ou
moins. En fait, en présence d’une insuf-
fisance mitrale de haut grade, la survie
peut être de 0 % (3). Dans la série de Bol-
ling (4), les 1 421 patients présentaient
une CMD en classe IV et avaient une
fraction d’éjection inférieure à 35 %.
Parmi ce groupe de patients à haut risque
recevant un traitement médical optimal,
435 sont morts à un an (31 %), la morta-
lité à 5 ans était de 50 % et de 75 % à
10 ans. En analyse multivariée, le pré-
dicteur de mortalité chez ces patients était
l’insuffisance mitrale sévère fonction-
nelle (grades 3 et 4). En fait, en termes de
survie pour les patients atteints de CMD,
la régurgitation mitrale a un plus mauvais
pronostic que l’atteinte coronaire, les
troubles du rythme ventriculaire ou le
cancer. Les patients présentant une CMD
avec insuffisance mitrale sont ceux qui,
habituellement, décèdent sur la liste d’at-
tente de transplantation cardiaque dans la
plupart des séries (1-4) ; néanmoins, en
cas de traitement de l’insuffisance mitrale
par un remplacement valvulaire, le pro-
nostic théorique serait très mauvais, avec
une mortalité atteignant 50 à 75 % en
postopératoire (évaluation du risque
périopératoire de la Society of Thoracic
Surgery) (4). La réparation valvulaire
mitrale a un pronostic bien meilleur que
le remplacement valvulaire, avec une
mortalité cinq fois moindre (4). Pour une
équipe envisageant un programme de
réparation valvulaire mitrale pour les
patients atteints de CMD avec RM, l’ob-
jectif initial est la réduction de la morta-
lité hospitalière, puis les résultats inter-
médiaires en termes de survie, de qualité
de l’amélioration de la fonction cardiaque
et du remodelage ventriculaire, d’éva-
luation du degré d’insuffisance cardiaque
et du besoin résiduel de transplantation.
LE REMODELAGE VENTRICULAIRE
GAUCHE : PHYSIOPATHOLOGIE
DE LA RÉGURGITATION MITRALE
A. La restriction des mouvements val-
vulaires et la disparition de la coaptation.
En présence de CMD avec RM, la valve
mitrale est anatomiquement normale
(feuillets mitraux, cordages), mais pré-
sente une anomalie de fonction du fait
d’une dilatation annulaire constante et
d’une désorientation des piliers mitraux
(déplacements latéraux) secondaire au
remodelage ventriculaire de la CMD. Les
modifications géométriques entraînent un
excès de traction sur les cordages et aug-
mentent les forces qui leur sont appli-
quées (tethering forces), avec pour consé-
quences une restriction des mouvements
valvulaires (petite et grande valves) ainsi
qu’une diminution puis une disparition
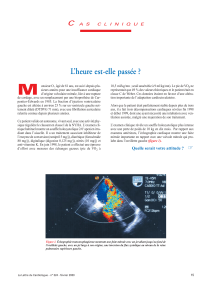
de la surface de coaptation (5) (figure 1).
En échographie, un aspect typique en
“aile de mouette” est bien visualisé sur
l’incidence parasternale grand axe. Selon
la classification fonctionnelle de Car-
pentier, on est en présence, dans la CMD,
d’une RM de type I-IIIb.
B. Le cercle vicieux : remodelage ven-
triculaire-insuffisance mitrale. L’aug-
mentation de la charge volumique chez
les CMD entraîne une augmentation de
la RM, qui entraîne elle-même une dila-
tation accrue de la chambre ventriculaire
avec excès des tensions sur les parois,
diminuant d’autant la performance ven-
triculaire, avec aggravation du pronostic.
Les techniques de réparation mitrale doi-
vent tenir compte de ces nouveaux
concepts physiopathologiques proches de
ceux récemment décrits pour les insuffi-
sances mitrales d’origine ischémique (6).
LA RÉPARATION VALVULAIRE MITRALE
Te c hnique
Compte tenu des mécanismes mieux com-
pris de la RM dans la CMD, le but de la
plastie mitrale est dès lors de restaurer une
surface de coaptation entre les feuillets
valvulaires par réduction de l’anneau
mitral natif par un anneau prothétique cir-
conférentiel sous-dimensionné pour obte-
nir une continence valvulaire. En effet, le
plan de coaptation des deux feuillets val-
vulaires, du fait de l’hypertraction des cor-
dages, est déplacé vers l’apex du ventri-
cule et s’éloigne du plan de l’anneau, avec
pour résultat un effet “tente” augmentant
la surface couvrante nécessaire des deux
feuillets mitraux pour obtenir la fermeture
de l’orifice mitral, et ce au détriment de la
surface de coaptation. Il nous semble
logique, en toute hypothèse, qu’une résec-
tion des cordages secondaires proposée
pour la RM ischémique soit indiquée éga-
lement dans ces cas de RM chez les CMD
(7). Le bien-fondé de cette hypothèse reste
néanmoins à démontrer.
Résultats
Dans la série pilote de Bolling (8, 9),
145 patients ont été inclus sur une
période de 7 ans ; l’âge moyen était de
63 ans (33 ans-81 ans), et aucun des
patients n’a subi de transplantation au
cours de cette période. La fraction
d’éjection moyenne était de 16 %
Le Courrier de la Transplantation - Volume II - n o2 - avril-mai-juin 2002
64
DOSSIER
thématique
Figure 1. Hypertraction sur la grande valve
mitrale avec aspect en “aile de mouette”
(flèche). Disparition de la surface de coap-
tation.

(6-26 %). Tous les patients étaient en
classe IV de la NYHA avec une RM
grade 4, 50 % des patients avaient une
CMD idiopathique et 50 % une CMD
ischémique. Les résultats intraopéra-
toires sont excellents, puisqu’il n’est
rapporté qu’un seul décès ; aucun n’a
nécessité d’assistance ventriculaire
gauche, et 10 % ont eu besoin d’un sup-
port immédiat par un ballon de contre-
pulsion aortique. La qualité des résul-
tats est, selon les auteurs, due à la
sélection des patients et à l’utilisation
de milrinone (inhibiteur des phospho-
diestérases) chez tous les patients. La
norépinéphrine est également utilisée
(elle fonctionne comme un agent non
bêta), les patients étant “rechargés” en
norépinéphrine pour augmenter son
niveau dans les myocytes (9). Les
récepteurs bêta-adrénergiques sont “
hypofonctionnels” et limités en nombre
chez les patients grands insuffisants
cardiaques, entraînant des non-
réponses aux bêtastimulants en termes
de contractilité cardiaque. Aucune RM
significative n’a été observée après
l’utilisation du plus petit anneau mitral
possible ; une seule sténose mitrale a
été rapportée. La mortalité à 30 jours
est de 4,8 % (7/145), avec une survie à
un an, 2 ans et 5 ans respectivement à
82 %, 71 % et 57 % ; la mortalité tar-
dive à 7 ans est de 26 patients. La sur-
vie à 5 ans est proche de celle des trans-
plantés cardiaques. Tous les survivants
à 7 ans sont en classe I et II. Concer-
nant 10 cas contrôles traités unique-
ment médicalement de façon optimale,
tous seraient morts à un an. La fraction
d’éjection est peu augmentée après
plastie mitrale, mais le débit cardiaque
(antérograde) l’est considérablement
du fait de la suppression de la RM. À
deux ans, le volume ventriculaire
gauche télédiastolique est très diminué
(1/3), démontrant le remodelage
ventriculaire post-plastie mitrale
(tableau I). Tous les patients reçoivent
un traitement médical et peuvent béné-
ficier des agents bêtabloquants et des
inhibiteurs de l’enzyme de conversion.
L’amélioration de ces patients capables
d’exercice physique se traduit par une
augmentation de la consommation
d’oxygène avec une VO2max passant de
14 ml O2/kg/mn à 19 ml O2/kg/mn.
L’index de sphéricité ventriculaire
gauche diminue (de 0,82 ± 0,1 à
0,74 ± 0,07 ; p = 0,005).
Sélection des patients
La démarche essentielle est de définir
quels patients peuvent bénéficier au
mieux de la plastie mitrale et de quels
paramètres dépendent les suites postopé-
ratoires. La mortalité à long terme est
dépendante des chiffres de pression pul-
monaire et du diamètre ventriculaire
gauche. En général, la géométrie du VG
détermine le devenir de ces patients. La
plastie mitrale est en fait une plastie de
remodelage de la base du ventricule
gauche, redonnant à celui-ci une forme
elliptique en postopératoire et lui per-
mettant de poursuivre ce remodelage
dans les suites. D’autres techniques chi-
rurgicales remodelant la géométrie du
VG offrent une alternative et peuvent
même être associées à la plastie mitrale.
Les techniques de remodelage ventricu-
laire actuelles sont l’opération de Dor,
pour la dilatation antérieure du VG en
rapport avec une maladie ischémique,
l’“Acorn”, réalisant un sac périventricu-
laire, et le “Myocor” (10, 11).
CONCLUSION
La plastie mitrale utilisant un anneau pro-
thétique circonférentiel sous-dimen-
sionné est une technique fiable, simple et
rapide. Les patients présentent une nette
amélioration fonctionnelle et un réel
bénéfice en termes de survie comparara-
tivement à ceux bénéficiant uniquement
d’un traitement médical. Le remodelage
ventriculaire primaire (VG elliptique en
postopératoire immédiat) et secondaire
permet en outre de réintroduire à terme
bêtabloquants et inhibiteurs de l’enzyme
de conversion. #
RÉFÉRENCES
BIBLIOGRAPHIQUES
1. Kono T, Sabbah HN, Rosman H, Alam M, Jafri S,
Goldstein S. Left ventricular shape is the primary
determinant of functional mitral regurgitation in
heart failure. J Am Coll Cardiol 1992 ; 20 : 1594-8.
2. Yellin T, Yoran C, Fréater R, Sonnern Blick E.
Dynamics of acute experimental mitral regurgitation. In :
Ionescu M, Cohn L, ed. Mitral valve disease : diagnosis
and treatment. Boston : ButterWorth ; 1985 ; 11-25.
3. Blondheim DS, Jacob LE, Kotler MN, Costacurta
GA, Pary WR. Dilated cardiomyopathy with mitral
regurgitation : decreased survival despite a low
frequency of left ventricular thrombus. Am Heart
J 1991 ; 122 : 763-71.
4.Kawachi Y,Ope M, Asou T, Tominaga R, Tokunaga K.
Comparative study between valve repair and replace-
ment for mitral pure regurgitation – early and late post-
operative results. Jp Circ J 1991 ; 55 : 443-52.
5. Kono T, Sabbah HN, Stein PO, Brymer JF, Khaja
F. Left ventricular shape as a determinant of functio-
nal mitral regurgitation in patients with severe heart
failure secondary to either coronary artery disease
or idiopathic dilated cardiomyopathy. Am J Cardiol
1991 ; 68 : 355-9.
6. Messas E, Guerro JL, Handschumacher MD et al.
Chordal cutting : a new therapeutic approach for
ischemic mitral regurgitation. Circulation 2001 ;
104 : 1958-63.
7.Couetil JP, Pouzet B, Abdel Shafy AB. A new method
to repair ischemic mitral valve regurgitation with basal
chordal cutting. Ann Thoracic Surg. Sous presse.
8.Bolling SF. Mitral reconstruction in cardiomyopa-
thy. J Heart Valve Dis 2002 ; 11 (suppl. 1) : 526-53.
9. Bolling SF, Pagani FD, Deeb GM, Bach DS.
Intermediate term outcome of mitral reconstruction
in cardiomyopathy. J Thorac Cardiovasc Surg 1998 ;
115 : 381-8.
10. Takagaki M, McCarthy PM, Ochiai Y et al.
Novel device to change left ventricular shape for
heart failure treatment ; device design and implanta-
tion procedure. ASAIO J 2001 ; 47 : 244-8.
11. McCarthy PM, Takayaki M, Ochiai Y et al.
Device-based change in left ventricular shape : a new
concept for the treatment of dilated cardiomyopathy.
J Thorac Cardiovasc Surg 2001 ; 122 : 482-90.
Le Courrier de la Transplantation - Volume II - n o2 - avril-mai-juin 2002
65
DOSSIER
thématique
Tableau I. Cardiomyopathie et réparation mitrale.
Paramètres Préopératoire 24 mois
Postopératoire
Volume télédiastolique (ml) 280 ± 86 206 ± 88*
Fraction d’éjection (%) 16 ± 5 26 ± 8*
Fraction de régurgitation (%) 70 ± 12 13 ± 10*
Débit cardiaque (l/mn) 3,1 ± 1,0 5,2 ± 08*
Classe NYHA 3,9 ± 0,2 1,8 ± 0,4*
*: p< 0,5.
1
/
3
100%