thématique D Thérapeutiques

Le Courrier de la Transplantation - Volume II - n o2 - avril-mai-juin 2002
56
DOSSIER
thématique
Le traitement des patients insuffisants cardiaques est un défi per-
manent. En effet, le traitement médical, la transplantation cardiaque
et l’assistance ventriculaire ne permettent pas d’apporter une solu-
tion thérapeutique à tous les patients. En 1985 et après cinq années
de recherche, la première cardiomyoplastie tissulaire (utilisant le muscle grand dorsal) est réalisée à l’hô-
pital Broussais (Paris). Depuis cette date, plus de 1 500 malades ont été opérés dans le monde. L’expé-
rience chirurgicale de notre équipe comporte 188 cas, 113 cardiomyoplasties réalisées à l’hôpital Brous-
sais-HEGP et 75 faisant partie d’un programme de coopération scientifique internationale. La technique
chirurgicale consiste à disséquer et transposer le muscle grand dorsal gauche à l’intérieur du thorax, puis
à l’enrouler autour du cœur. Un système d’électrostimulation musculaire développé dans notre labora-
toire (électrodes et myostimulateur implantables) permet une contraction chronique du muscle, afin de
renforcer la systole ventriculaire. Les indications concernent les malades atteints d’insuffisance cardiaque
chronique due à des cardiomyopathies ischémiques ou idiopathiques, réfractaires au traitement médi-
cal. Les résultats à long terme montrent une augmentation de la fonction systolique ventriculaire, une
limitation de la dilatation des ventricules, ainsi qu’une réduction de la tension pariétale ventriculaire.
L’aortomyoplastie consiste à envelopper le muscle grand dorsal droit autour de l’aorte ascendante ou
le grand dorsal gauche autour de l’aorte descendante. Une contraction musculaire diastolique induite
par électrostimulation provoque une contrepulsion biologique. Le concept de cardiomyoplastie cel-
lulaire repose sur un apport de cellules exogènes myogéniques dans le myocarde pour suppléer aux
cardiomyocytes disparus ou altérés. Le but recherché est la restitution d’une masse myocardique fonc-
tionnelle et une amélioration des fonctions systolique et diastolique. À partir de 1989, les principes
de la cardiomyoplastie tissulaire sont appliqués à la thérapie cellulaire. En 2001, les premières appli-
cations cliniques débutent en France, aux États-Unis et au Japon. La technique consiste à utiliser
des cellules musculaires indifférenciées (myoblastes) du malade, prélevées par biopsie, ou à utiliser
des cellules souches pluripotentes de la moelle osseuse, cultivées pendant trois semaines et implan-
tées dans le myocarde pathologique.
Mots-clés :
Insuffisance cardiaque - Cardiomyoplastie - Aortomyoplastie - Thérapie cellulaire -
Cardiomyoplastie cellulaire.
Résumé
Résumé
Thérapeutiques
alternatives
dans le domaine
de la
transplantation
cardiaque
Coordinateur : J.C. Chachques,
hôpital Européen Georges-Pompidou,
75015 Paris.
!Assistance biologique de l’insuffisance cardiaque
par cardiomyoplastie (tissulaire et cellulaire) et aortomyoplastie
J.C. Chachques, B. Cattadori, A. Berrebi, M.C. Iliou, P. Meimoun, A. Carpentier
"Chirurgie valvulaire mitrale chez les patients
atteints de cardiomyopathie dilatée -J.P. Couetil
"Resynchronisation atrio-biventriculaire - C.Alonso,T. Lavergne,
J. Ollitrault, J.Y. Le Heuzey, M. Aitsaid, J.M. Darondel, L. Guize
"Reduction ventriculoplasty -R.J.V. Batista
"Ventricular containment (Acorn Wrap) -
M. Acker
"Left ventricular assist device as a bridge
to heart transplantation: the Cleveland Clinic experience
J.L. Navia, P.R.Vega, C. Faber, N.G. Smedira, P.M. McCarthy
* Hôpital Européen Georges-Pompidou, 75015 Paris.
Assistance biologique de l’insuffisance
cardiaque par cardiomyoplastie
(tissulaire et cellulaire) et aortomyoplastie
"
J.C. Chachques*, B. Cattadori*, A. Berrebi*, M.C. Iliou*, P. Meimoun*, A. Carpentier*

Le Courrier de la Transplantation - Volume II - n o2 - avril-mai-juin 2002
57
DOSSIER
thématique
PROBLÉMATIQUE
Le traitement médical, la transplantation
cardiaque et l’assistance ventriculaire ne
permettent pas d’apporter une solution
thérapeutique à tous les patients présen-
tant une insuffisance cardiaque sévère,
d’où l’intérêt des recherches sur les tech-
niques reconstructrices en chirurgie
cardiovasculaire. C’est ainsi qu’à partir
de l’année 1981, dans le laboratoire
d’études des greffes et prothèses car-
diaques de l’hôpital Broussais, de nou-
velles techniques d’assistance circula-
toire biologique ont été développées (1,
2).
Le travail de recherche effectué concerne
l’étude du rôle des muscles squelettiques
électrostimulés, placés autour du cœur et
de l’aorte dans le but d’offrir une assis-
tance circulatoire biologique, totalement
implantable. Deux systèmes ont été déve-
loppés à partir du principe selon lequel
un muscle squelettique électrostimulé à
long terme devient résistant à la fatigue
par transformation de ses caractéristiques
métaboliques et électrophysiologiques,
tout en conservant une force de contrac-
tion appropriée capable de fournir un tra-
vail comparable à celui du myocarde. Ces
systèmes d’assistance autologues sont la
cardiomyoplastieet l’aortomyoplastie.
Le but de ces systèmes biomécaniques,
combinant chirurgie cardiaque et plas-
tique au génie biomédical, est de prolon-
ger et d’améliorer la qualité de vie des
patients atteints d’insuffisance cardiaque
chronique sévère, réfractaire au traite-
ment médical (figure 1).
#La cardiomyoplastie a été conçue
pour assister le cœur défaillant en l’en-
veloppant du muscle grand dorsal du
patient, électrostimulé de façon syn-
chrone à la systole ventriculaire. Son but
est de restituer ou d’augmenter la
contractilité myocardique (effet compa-
rable au massage cardiaque) et de limiter
la dilatation ventriculaire. La cardio-
myoplastie est indiquée chez les patients
en insuffisance cardiaque d’origine isché-
mique (malades ayant présenté des
infarctus successifs ou d’une grande
extension), ainsi que dans les cardio-
myopathies dilatées (généralement d’ori-
gine indéterminée) (3).
Après quatre années de recherche dans
notre laboratoire, le premier cas mondial
de cardiomyoplastie a été réalisé par
notre équipe en 1985. Cette technique a
été utilisée mondialement sur plus de
1 500 malades (4-7).
# L’aortomyoplastie consiste à enve-
lopper le muscle grand dorsal droit pédi-
culé autour de l’aorte ascendante ou le
muscle grand dorsal gauche autour de
l’aorte descendante. La stimulation mus-
culaire est réalisée pendant la diastole. Le
but de l’aortomyoplastie est de transfor-
mer l’aorte en une nouvelle cavité
(néoventricule) qui soit contractile et
hémocompatible, reproduisant ainsi
chroniquement les effets d’une contre-
pulsion par ballon intra-aortique. À ce
jour, l’expérience mondiale comporte
36 patients. Les résultats encourageants des
études expérimentales ont été confirmés par
les premiers résultats cliniques (8, 9).
Nos recherches ont porté non seulement
sur la mise au point de nouvelles tech-
niques chirurgicales, mais aussi sur la
création du matériel électronique néces-
saire à ces interventions. Ainsi, l’expéri-
mentation a abouti à la conception
de nouvelles électrodes de stimulation
musculaire et de détection du signal
ventriculaire, d’un cardiomyostimulateur
(pacemaker spécifique), et d’un protocole
d’électrostimulation progressive et
séquentielle du muscle grand dorsal afin
d’entraîner le muscle squelettique pour
une nouvelle fonction contractile, simi-
laire à celle du myocarde.
A
B
E
C
D
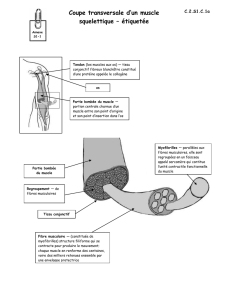
Figure 1. Différentes techniques d’assistance
biologique de l’insuffisance cardiaque, déve-
loppées dans le laboratoire d’études des
greffes et prothèses cardiaques de l’hôpital
Broussais :
A. cardiomyoplastie ; B. aortomyoplastie ;
C. néoventricule musculaire ; D. atriomyo-
plastie ; E. cardiomyoplastie cellulaire.

Le Courrier de la Transplantation - Volume II - n o2 - avril-mai-juin 2002
58
DOSSIER
thématique
INDICATIONS
La cardiomyoplastie est indiquée chez les
patients en insuffisance cardiaque chronique
sévère. Les défaillances myocardiques
ischémiques (malades ayant présenté des
infarctus successifs ou d’une grande exten-
sion) ainsi que les cardiomyopathies dila-
tées (généralement d’origine indéterminée)
sont concernées. Les cardiomyopathies
hypertrophiques ou obstructives et les car-
diomyopathies restrictives ne sont pas des
indications à la cardiomyoplastie.
Le choix du moment de la cardiomyo-
plastie intervient dans les résultats post-
opératoires. Le bénéfice hémodynamique
de la cardiomyoplastie n’étant acquis
qu’après un délai de quelques semaines
correspondant à la période d’adaptation
du muscle grand dorsal à sa nouvelle
fonction d’assistance cardiaque, la sélec-
tion des patients doit tenir compte de leur
fonction myocardique résiduelle.
TECHNIQUE CHIRURGICALE
Cardiomyoplastie du ventricule gauche
La technique consiste à disséquer la totalité
du muscle grand dorsal (MGD), son pédi-
cule vasculonerveux devant être soigneuse-
ment préservé. Deux électrodes intramus-
culaires de stimulation sont implantées au
niveau de la division du nerf du grand dor-
sal, afin de réaliser une électrostimulation
bipolaire spécifique à ce muscle. Le MGD
est ensuite transposé à l’intérieur du thorax
à travers une fenêtre réalisée dans le “gril
costal”, par résection partielle de la deuxième
côte. Le MGD sera alors fixé autour des ven-
tricules sans nécessité de circulation extra-
corporelle (figure 2). Deux électrodes seront
implantées dans la paroi ventriculaire, afin
de synchroniser la contraction musculaire et
la systole ventriculaire (3, 10).
Électrostimulation
Les électrodes sont reliées ensuite à un
générateur d’impulsions implantable
(cardiomyostimulateur), placé dans une
poche sous-cutanée. La stimulation du
muscle grand dorsal commence deux
semaines après la cardiomyoplastie. Ce
délai est nécessaire à une cicatrisation
musculaire, au développement d’une cir-
culation collatérale du grand dorsal et à
la formation d’adhérences entre le cœur,
le muscle et le péricarde. La stimulation
séquentielle et progressive du muscle
squelettique commence par des impul-
sions uniques suivies deux semaines
après par des trains d’impulsions. En
effet, une impulsion unique entraîne une
contraction modérée du muscle. Une
contraction forte et prolongée, mimant la
systole ventriculaire, est possible en uti-
lisant des trains d’impulsions électriques
de 30 hertz, fréquence proche de la
décharge physiologique du motoneurone
de fibres musculaires lentes. Ce train d’im-
pulsions permet une sommation tempo-
relle, avec recrutement de toutes les fibres
Figure 2. Technique chirurgicale de la cardio-
myoplastie : le muscle grand dorsal gauche est
fixé autour des ventricules et électrostimulé
chroniquement pendant la systole, à l’aide
d’un cardiomyostimulateur (pacemaker spé-
cifique).

Le Courrier de la Transplantation - Volume II - n o2 - avril-mai-juin 2002
59
DOSSIER
thématique
musculaires. Sa durée est physiologique-
ment adaptée à la systole ventriculaire.
Substitution de la paroi ventriculaire
Dans la technique de cardiomyoplastie,
le muscle grand dorsal peut servir à rem-
placer une partie du myocarde après
résection d’un volumineux anévrysme ou
d’une tumeur extensive. Cette recons-
truction est réalisée sous circulation
extracorporelle et comporte la fermeture
de la partie réséquée avec une pièce de
péricarde autologue comme néo-endo-
carde, et la couverture par le lambeau de
muscle grand dorsal comme néomyo-
carde. Cette pièce de péricarde utilisée
comme interface permet d’éviter les
risques de thrombose ou d’hématome
qu’entraînerait un contact direct du sang
avec le muscle (11).
Cardiomyoplastie du ventricule droit
Il est possible de réaliser une cardio-
myoplastie sélective du ventricule droit,
en cas de dysplasie arythmogénique,
tumeur, ou infarctus important du ventri-
cule droit. On utilise aussi le muscle
grand dorsal gauche que l’on enroule sur
la face antérieure et latérale du ventricule
droit. La partie distale du muscle est fixée
au diaphragme (12).
Atriomyoplastie
Cette technique a été créée pour assister
la fonction atriale dans certaines cardio-
pathies congénitales (figure 1D). L’in-
tervention de Fontan (dérivation atrio-
pulmonaire) est une option thérapeutique
valable dans la chirurgie des malforma-
tions cardiaques congénitales chez des
patients nés avec une absence de ventri-
cule droit fonctionnel (cas d’atrésie tri-
cuspidienne ou de ventricule unique). Si
l’intervention de Fontan a permis d’amé-
liorer de manière considérable le statut
clinique de ces malades, les résultats à
long terme sont moins favorables. Une
fonction ventriculaire droite absente
pourrait être à l’origine de ces résultats
décevants. Le but d’une cardiomyoplas-
tie sur l’oreillette droite est de restaurer
une fonction ventriculaire droite après
dérivation atriopulmonaire, et d’aug-
menter ainsi le débit cardiaque chez les
patients bénéficiant de ce type d’inter-
vention. La technique opératoire consiste
à fixer le lambeau du muscle grand dor-
sal gauche sur l’oreillette droite et à élec-
trostimuler le muscle pendant la systole
ventriculaire (13).
MÉCANISMES D’ACTION
DE LA CARDIOMYOPLASTIE
La cardiomyoplastie améliore la perfor-
mance cardiaque par plusieurs méca-
nismes (14, 15) :
#augmentation de l’éjection systolique
ventriculaire (effet comparable au mas-
sage cardiaque) ;
#limitation de la dilatation cardiaque ;
#réduction de la tension de la paroi des
ventricules ;
#inversion du remodelage postisché-
mique des cavités cardiaques.
CARDIOMYOPLASTIE :
RÉSULTATS À LONG TERME
La cardiomyoplastie a été utilisée dans
notre institution comme traitement de
l’insuffisance cardiaque. L’expérience de
notre équipe comporte 188 malades, dont
113 opérés à l’hôpital Broussais et 75
dans d’autres centres faisant partie d’un
programme de coopération international.
Méthodes
Cent treize patients âgés en moyenne de
51 ans (15-72) ont été opérés à l’hôpital
Broussais. Quatre-vingt-sept étaient en
NYHA classe III et 26 en classe IV. La
fraction d’éjection moyenne était de
17 %, et le volume télédiastolique du VG
était de 178 ± 31 ml/m2. L’étiologie de
l’insuffisance cardiaque était ischémique
chez 59 patients, une cardiomyopathie
dilatée chez 47 et une tumeur ventricu-
laire chez 7. La voie d’abord était initia-
lement double (voie postérieure pour dis-
section du grand dorsal puis sternotomie
médiane verticale pour le temps car-
diaque). Elle est actuellement unique
(minithoracotomie et vidéoassistance).
Treize patients ont été traités selon ce
protocole.
Résultats
La mortalité hospitalière est actuellement
de moins de 5 %. La survie actuarielle à
10 ans est de 70 % pour les patients opé-
rés en classe III de la NYHA et de 28 %
pour ceux de la classe IV. La classe
fonctionnelle NYHA moyenne était en
préopératoire de 3,3 et en postopératoire
de 1,4. Les explorations chez les survi-
vants ont montré une amélioration de la
fraction d’éjection (17 ± 4 % passant à
28 ± 6 %) et de l’index cardiaque (1,9
passant à 2,8 l/mn/m2). Dix patients ont
reçu une transplantation cardiaque entre
2 et 5 années après la cardiomyoplastie,
sans difficulté technique particulière et
sans mortalité périopératoire. L’indica-
tion de la transplantation cardiaque a été
la progression importante de la cardio-
pathie initiale, associée généralement à
une fibrillation auriculaire et à des
troubles sévères du rythme ventriculaire.
Conclusion
Les résultats de la cardiomyoplastie se
sont améliorés avec le temps en raison
d’une meilleure connaissance des fac-
teurs de risque, d’indications plus pré-
cises et des améliorations techniques
apportées, notamment, par l’utilisation de
stratégies moins invasives. Ces résultats
devraient inciter à relancer l’utilisation
de cette technique où la seule alternative,
la transplantation cardiaque, souffre d’un
manque critique de donneurs (16-18).
Deux nouveaux pacemakers sont actuel-
lement disponibles pour cette interven-
tion : “Myos”, distribué par Biotronik
(Berlin, Allemagne), et “LD-Pace II”,
distribué par Illini Group (Chicago, États-
Unis) (19), ainsi que des nouveaux pro-
tocoles d’électrostimulation postopéra-
toire, développés pour éviter la
surstimulation musculaire et le risque de
fibrose du muscle grand dorsal (20, 21).
ASSOCIATION
DE LA CARDIOMYOPLASTIE
AUX TRAITEMENTS
ÉLECTROPHYSIOLOGIQUES
Les patients ayant fait l’objet d’une car-
diomyoplastie, porteurs des cardiomyo-
pathies ischémiques ou idiopathiques
sévères, présentent un risque important
d’arythmies ventriculaires potentielle-
ment responsables de la survenue d’une
mort subite. En même temps, on observe

Le Courrier de la Transplantation - Volume II - n o2 - avril-mai-juin 2002
60
DOSSIER
thématique
fréquemment chez ces malades des
asynchronismes électriques et méca-
niques du cœur gauche et droit. Dans des
cas cliniques récents, la cardiomyoplas-
tie a été associée à la mise en place d’un
défibrillateur implantable ou à une sti-
mulation biventriculaire (stimulation
multisite). Les résultats obtenus, très
positifs, permettent de prévoir une
expansion importante de cette associa-
tion thérapeutique.
AORTOMYOPLASTIE
L’aortomyoplastie consiste à envelopper
le muscle grand dorsal droit autour de
l’aorte ascendante ou le muscle grand
dorsal gauche autour de l’aorte descen-
dante, en réalisant une contraction mus-
culaire pendant la diastole (figure 1B).
Le but de l’aortomyoplastie est de trans-
former l’aorte ascendante ou descendante
en une nouvelle cavité qui soit contrac-
tile et hémocompatible. Cette technique
produit une contrepulsion diastolique
biologique sans endommager la paroi
aortique. Le but de l’aortomyoplastie est
de reproduire chroniquement les effets
d’une contrepulsion par ballon intra-
aortique, à savoir :
#diminution de la postcharge du ventri-
cule gauche ;
#augmentation de la pression de perfu-
sion coronaire, avec augmentation de
l’apport en oxygène au myocarde.
Lorsque l’aorte est de petit diamètre, il
est possible de l’élargir avec une pièce
de péricarde autologue, et d’augmenter
ainsi le volume de ce néoventricule. La
dissection, la mobilisation du muscle
grand dorsal, l’implantation d’électrodes
de stimulation et son transfert à l’inté-
rieur de la cavité thoracique sont réali-
sés selon le même protocole que celui de
la cardiomyoplastie. En revanche, la pro-
grammation du cardiomyostimulateur
est particulière, de manière à assurer une
électrostimulation du muscle grand dor-
sal permettant la compression diasto-
lique de l’aorte. Cette programmation
permet également une inhibition transi-
toire de la stimulation musculaire en
présence d’extrasystoles ventriculaires
(8, 9).
Expérience clinique internationale
Trente-neuf patients, d’âge moyen 54
±7ans, ont fait l’objet d’une aortomyo-
plastie élective : quatre patients à l’hôpi-
tal Broussais, quatre à Marseille (hôpital
La Timone), trois à Londres, seize à
Djedda (Arabie saoudite), dix à Buenos
Aires (Argentine), un à La Corogne
(Espagne) et un au Caire (Égypte).
Après un suivi moyen de 19 mois, l’éva-
luation de la classe fonctionnelle
(NYHA) montre une amélioration signi-
ficative, passant de 3,6 en préopératoire
à 2,2 en postopératoire (p < 0,05). Des
questionnaires concernant la qualité de
vie ont montré, pour la plupart des
patients, une amélioration de l’activité
physique, de la performance au travail et
des activités sociales. Parallèlement, des
études hémodynamiques, ainsi que
l’échographie doppler, ont mis en évi-
dence la compression diastolique de
l’aorte et une augmentation de la pression
diastolique lors de l’électrostimulation du
muscle grand dorsal.
Une expérience clinique à plus long
terme ainsi qu’un nombre plus important
de malades semblent nécessaires afin de
définir la place de l’aortomyoplastie dans
le traitement de l’insuffisance cardiaque
sévère.
Un des avantages de l’aortomyoplastie
dynamique réside dans le fait qu’elle est
réalisée sans manipulation du cœur, sans
clampage aortique total et sans circula-
tion extracorporelle, situation d’extrême
importance chez des malades en insuffi-
sance cardiaque sévère, souvent très
instables.
NÉOVENTRICULE MUSCULAIRE
Une autre approche consiste à construire
des ventricules biologiques en associant
une poche en silicone ou en péricarde,
recouverte par le muscle grand dorsal
pédiculé. Ce néoventricule est anasto-
mosé à l’aorte et électrostimulé en contre-
pulsion (figure 1C). Plusieurs études
expérimentales utilisant ce dispositif
d’assistance circulatoire biologique ont
été réalisées (22).
CARDIOMYOPLASTIE CELLULAIRE
Le développement de la biologie cellu-
laire et moléculaire permet d’envisager
de nouvelles stratégies thérapeutiques des
maladies du myocarde. L’objectif de la
cardiomyoplastie cellulaire est d’obtenir
une réparation du myocarde lésé par
l’injection de cellules myogéniques
issues du même malade (autologues), afin
de restaurer la contractilité ventriculaire
(23).
Il faut tenir compte de ce que les cardio-
myocytes, passé les stades fœtaux du
développement, perdent leur faculté
de prolifération. Une lésion d’infarctus
myocardique ne peut donc se réparer par
la prolifération des cardiomyocytes
adultes, car le nombre de cellules souches
myocardiques est très limité (24). Le
concept de cardiomyoplastie cellulaire
repose ainsi sur un apport de cellules exo-
gènes myogéniques dans le myocarde
pour suppléer aux cardiomyocytes
disparus ou altérés.
Les différentes voies de thérapie cellulaire
comme traitement de l’insuffisance car-
diaque consistent en l’implantation à l’in-
térieur du muscle cardiaque de différents
types cellulaires cultivés in vitro pendant
trois semaines : myoblastes squelettiques
autologues, cardiomyocytes fœtaux,
cellules musculaires lisses ou cellules
souches de moelle osseuse (25-31).
Notre équipe travaille depuis 1996 dans
la cardiomyoplastie cellulaire. Sous le
patronage de l’Union européenne, des
études expérimentales sont en cours de
réalisation, avec des résultats très pro-
metteurs (contrat de la Commission
européenne [ERBFM]). Des myo-
blastes prélevés des muscles squelet-
tiques sont cultivés et ensuite injectés
dans le myocarde pathologique du
même individu. Ce traitement entraîne
un processus de régénération capable
de rendre réversible la fibrose myocar-
dique survenue lors d’un infarctus du
myocarde, réduisant ainsi la taille de la
cicatrice post-infarctus. L’élasticité
myocardique, la compliance et la
contractilité régionale du ventricule
sont améliorées.
 6
6
 7
7
1
/
7
100%