Lire l'article complet

104
Métabolismes Hormones Diabètes et Nutrition (XII), n°3, mai-juin 2008
Actualités
Actualités
Paradoxe : HDL élevé,
LDL bas, des décès en plus
La Cholesterol Ester Transfert Protein
(CETP) préside aux échanges d’esters
de cholestérol des HDL vers les autres
lipoprotéines. L’inhibition de son acti-
vité induit une élévation du taux de
HDL-cholestérol et une réduction de
celui du LDL. Ces modifications s’ef-
fectuent donc dans le sens d’un effet
antiathérogène. Des inhibiteurs de la
CETP ont été développés par certains
laboratoires, car il s’agit là d’une
nouvelle classe thérapeutique poten-
tielle d’intérêt pour la prévention du
risque vasculaire. P.J. Barter et al. ont
tout récemment publié les résultats
d’une étude randomisée sur une large
échelle (plus de 15000 patients inclus)
dont l’objectif était de tester l’intérêt du
blocage de la CETP chez des patients
aux antécédents cardiovasculaires et
traités par statine. Ces patients, âgés
de 45 à 75 ans, ont été répartis par
tirage au sort: la moitié d’entre eux
ont reçu uniquement de l’atorvastatine,
l’autre moitié une association d’ator-
vastatine et de torcetrapib, molécule
inhibitrice de la CETP. Douze mois
après l’instauration de la thérapeutique
combinée (torcetrapib plus atorvasta-
tine), le HDL-cholestérol s’est élevé
de 72% et le LDL-cholestérol s’est
abaissé de 25% par rapport aux valeurs
initiales. Ces résultats contrastent avec
ceux obtenus avec l’atorvastatine seule
avec laquelle il n’y a pas de modifica-
tion significative de ces paramètres. Il
faut cependant préciser qu’avant l’in-
troduction de l’inhibiteur de la CETP,
tous les patients ont reçu de l’atorvasta-
tine à dose suffisante pour abaisser leur
LDL-cholestérol au-dessous de 1 g/l.
Les effets observés sont donc bien ceux
de l’inhibition de la CETP. De façon
paradoxale, cet effet “antiathérogène”
du trocetrapib s’accompagne d’une
augmentation du risque d’évènements
cardiovasculaires et surtout de décès
toutes causes confondues. Parmi les
explications possibles, les auteurs en
retiennent deux: une stimulation de la
sécrétion d’aldostérone traduite dans
le groupe traité par trocetrapib par une
élévation de la pression artérielle, une
réduction significative de la kaliémie
et une inflation de la réserve alcaline.
L’autre explication impute des modifi-
cations de la composition de la structure
des particules de HDL par l’inhibition
de la CETP, ce qui limiterait leur rôle
épurateur vasculaire. Les résultats
fort instructifs de cet essai négatif en
termes de bienfait pour le patient, illus-
trent bien que la mission du thérapeute
dépasse de loin la recherche de l’obten-
tion d’un chiffre cible.
J.M. Kuhn,
service d’endocrinologie,
diabète et maladies métaboliques,
CHU de Rouen.
Barter PJ et al. N Engl J Med 2007;357:2109-22.
Un régime riche en graisse
perturbe l’horloge biologique
Dans toutes les espèces grandes ou
petites, simples ou complexes, l’hor-
loge biologique interne, réglée sur une
période de 24 heures, gouverne les
cycles activité-repos. Elle rythme la
prise alimentaire ainsi que beaucoup
d’autres fonctions métaboliques et
endocrines. Elle permet les adaptations
physiologique et comportementale de
l’organisme à l’alternance jour/nuit.
Joe Bass, endocrinologue à la Northwes-
tern University de Chicago, avait
rapporté, dans un article publié dans
Science, qu’un dérèglement de l’hor-
loge interne provoqué par l’invalidation
du gène clock chez la souris boulever-
sait le métabolisme et entraînait obésité
et diabète. Poursuivant cette étude, Bass
et al. s’interrogèrent sur la nature des
facteurs environnementaux suscepti-
bles de reproduire le phénotype des
souris clock–/– et de perturber le cycle
circadien. Étant donné que l’horloge
biologique influence le métabolisme, ils
envisagèrent dans un premier temps un
possible effet de l’alimentation.
Brièvement, la démarche de Bass et
son équipe a consisté à comparer deux
groupes de souris, un groupe main-
tenu dans des conditions d’alimen-
tation normale, l’autre soumis à un
régime alimentaire hyperlipidique. Ils
ont constaté en premier lieu un allon-
gement significatif de la période de
l’horloge biologique, qui normalement
se situe autour de 23,6 heures chez
la souris. Ces résultats suggéraient
effectivement que les mécanismes qui
contrôlent l’horloge biologique dans le
cerveau sont influencés par le contenu
de l’alimentation. Par ailleurs, alors que
les souris nourries normalement sont
d’ordinaire plus actives la nuit, celles
soumises à un régime gras pendant
deux semaines devenaient plus actives
de jour. Elles consommaient aussi plus
de nourriture de jour que de nuit, entraî-
nant une atténuation du rythme circa-
dien de l’alimentation.
Chez les animaux, le mécanisme molé-
culaire à la base de l’horloge biologique
est une boucle d’autorégulation négative,
conservée chez de nombreuses espèces.
Cette boucle est opérationnelle non seule-
ment au niveau du noyau suprachias-
matique de l’hypothalamus, mais aussi
dans la plupart des cellules. Les acteurs
principaux du cycle circadien sont les
gènes Per et Cry, dont les produits PER
et CRY forment des dimères capables
d’inhiber leur propre activation trans-
criptionnelle. Les complexes protéiques
PER/CRY se dégradent progressivement
et sont remplacés par d’autres complexes
formés par les produits des gènes Clock
et Balm1. Ces derniers sont des activa-
teurs de la transcription de Per et Cry,
capables de lever l’inhibition exercée par
PER/CRY au bout d’environ 24 heures
(figure).
Les travaux de Bass et al. ont montré
que les changements de la périodicité et
l’atténuation du rythme circadien chez
les souris soumises à un régime hyper-
lipidique s’accompagnaient au niveau
moléculaire d’une diminution d’ex-
pression des gènes de l’horloge interne
Clock, Balm1 et Per2. L’intensité de
l’inhibition était variable selon le gène
et le tissu étudiés (hypothalamus, tissu
adipeux et foie), la diminution la plus
importante étant observée au niveau du
tissu adipeux. Ils ont également montré
qu’un régime gras perturbait aussi les
rythmes circadiens de nombreux autres
facteurs incluant la leptine et l’insu-
>>>

106
Métabolismes Hormones Diabètes et Nutrition (XII), n°3, mai-juin 2008
Actualités
Actualités
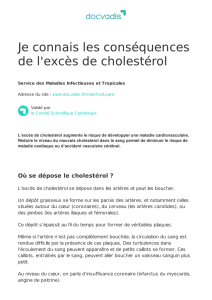
Figure. Les gènes de l’horloge interne. Chez
les animaux, le mécanisme moléculaire à la
base de l’horloge biologique est une boucle
d’autorégulation négative, conservée chez
de nombreuses espèces. Les acteurs princi-
paux du cycle circadien sont les gènes Per et
Cry, dont les produits PER et CRY forment
des dimères capables d’inhiber leur propre
activation transcriptionnelle. Les complexes
protéiques PER/CRY se dégradent progres-
sivement et sont remplacés par d’autres com-
plexes formés par les produits des gènes Clock
et Balm1. Ces derniers sont des activateurs de
la transcription de Per et Cry. Leur présence
lève l’inhibition exercée par PER/CRY. Cette
boucle d’autorégulation se déroule sur un cy-
cle de ≈ 24 heures.
Per
Cry
Per
Cry
Per
Cry
24 heures
Dégradation
Balm1
Clock
line circulantes, certains neuropeptides
hypothalamiques (AGRP, NPY, P0MC,
CART) et certains récepteurs nucléaires
(NR) impliqués dans l’horloge molé-
culaire au niveau du foie et du tissu
adipeux (Rev-erbα, RORα, RXRα,
PPARα, PPARγ).
Les résultats de Bass et son équipe
montrent donc que l’obésité induite
par un régime hyperlipidique perturbe
l’horloge interne et les variations circa-
diennes de nombreux gènes liés au
métabolisme. Au-delà des conséquences
d’un régime riche en graisse sur l’obé-
sité et ses complications (résistance à
l’insuline, syndrome métabolique), il
est clair qu’il faudra maintenant évaluer
plus globalement l’impact réel de l’ali-
mentation sur la santé humaine.
I. Lihrmann, Inserm U413,
université de Rouen
Turek FW, Joshu C, Kohsaka A et al. Science
2005;308:1043-5.
Kohsaka A, Laposky AD, Ramsey KM et al.
Cell Metab 2007;6:414-21.
Encore un “coup”
du gang des statines
Les traitements par statines réduisent
significativement la morbidité et la
mortalité cardiovasculaires et céré-
brovasculaires. Il a été parallèlement
démontré que les statines exerçaient des
effets pléiotropiques, indépendants de
leur impact bénéfique sur le profil lipi-
dique. Ils sont variés et peuvent aussi
bien se traduire par une influence directe
sur la fonction endothéliale, ou une
immuno-modulation, ou bien encore
une réduction des conséquences néfastes
des produits de glycosylation avancée,
etc. Certaines études longitudinales
prospectives et contrôlées suggèrent en
outre qu’une réduction de l’incidence
des cancers pourrait faire partie de cette
liste d’effets pléiotropiques. Passant
de la carcinogenèse à la tumorigenèse,
C. Capelli et al. (1) ont évalué de façon
rétrospective l’effet du traitement par
statine sur la fréquence et les dimensions
de nodules thyroïdiens chez 135 patients
dyslipidémiques traités par statine depuis
au moins 5 ans comparativement à une
population contrôle de 136 adultes non
traités par inhibiteur de l’HMG-CoA-
réductase. Les différences significatives
entre les deux populations concernent
l’usage de traitements au long cours
(statines exceptées), les antécédents
familiaux d’affection thyroïdienne
(plus fréquents dans le groupe statine)
et, bien entendu, le taux de cholestérol
total, significativement inférieur dans le
groupe traité par statine. Tous les adultes
inclus dans cette étude étaient clinique-
ment et biologiquement euthyroïdiens.
Volume et caractéristiques de la thyroïde
ont été évalués par échographie selon
des procédures standardisées. Les résul-
tats bruts sont les suivants: sous statine,
la fréquence des nodules est réduite
de moitié; le nombre et le volume des
nodules sont réduits de moitié; le volume
total de la thyroïde est réduit de 15% et le
volume nodulaire par rapport au volume
thyroïdien de 40%. L’analyse statistique,
qui a pris tous les facteurs confondants
en considération, relie directement les
modifications morphologiques observées
au traitement par statines. Le mécanisme
physiopathologique explicatif pourrait
résider dans l’effet indirect des statines
sur la voie pro-proliférative, impliquant
les protéines de la superfamille Ras/Rho.
S’ils étaient confirmés par des études
prospectives randomisées, les résultats
de cette étude rétrospective ouvriraient
une porte sur une nouvelle utilisation
potentielle et tout à fait inattendue des
statines.
JM Kuhn
Capelli C et al. Clin Endocrinol 2008;68:16-21.
Testostérone, marqueur
de longévité chez l’homme ?
Il est bien démontré que le taux plasma-
tique de testostérone décroît progressi-
vement avec l’âge chez l’homme. La
profondeur de ce phénomène, qui est loin
d’atteindre tous les hommes, est fonc-
tion de nombreux facteurs, au nombre
desquels il convient de citer les mala-
dies intercurrentes, les conditions de vie
et les interférences médicamenteuses. Il
est estimé qu’environ 30% des hommes
de plus de 60 ans ont un taux de testosté-
rone plasmatique total au-dessous de la
“norme” (1), dont la limite inférieure est
actuellement empiriquement déterminée
comme étant la moyenne réduite de
deux SEM de la testostéronémie d’une
population d’hommes adultes en bonne
santé. L’étude menée par GA Laughlin
et al. (2) a eu pour objectif d’évaluer
l’association éventuelle entre morta-
lité et taux plasmatique de testostérone
chez l’homme de plus de 50 ans. Sept
cent quatre-vingt quatorze hommes ont
été inclus dans cette étude prospective,
dont la durée moyenne d’observation a
été de 11,8 années. Sur les 885 hommes
initialement sélectionnés, ont été écartés
de l’analyse ceux dont le décès est
survenu dans les cinq premières années
de l’étude. Le taux de testostérone a été
déterminé au départ et le suivi assuré au
maximum sur 20 ans. Les principaux
facteurs de risque cardiovasculaire (taba-
gisme, alcoolisme, sédentarité, index de
masse corporelle, pression artérielle,
diabète ou syndrome métabolique, etc.)
ont été pris en considération. L’index
1.
>>>

107
Actualités
Actualités
Le Courrier Métabolismes Hormones Diabètes et Nutrition
vous souhaite un bel été sur la route des vacances
et vous donne rendez-vous à la rentrée
HOMA de sensibilité à l’insuline, le
taux ultrasensible de CRP, les taux de
testostérone et d’estradiol plasmatique
ont également fait partie des paramètres
étudiés. Les hommes dont la testostéro-
némie est inférieure à 2,4 ng/ml ont un
risque de mortalité dans les 20 années
suivantes supérieur de 40% à ceux dont
la testostéronémie est située au-dessus
de cette valeur seuil. L’exclusion des
hommes initialement atteints de diabète,
de syndrome métabolique ou d’affec-
tion cardiovasculaire ne modifie pas ce
résultat. Néanmoins, un taux initiale-
ment bas de testostérone plasmatique est
fortement associé aux causes ultérieures
de décès cardiovasculaires et respira-
toires. Les auteurs rappellent qu’il a
été montré qu’un abaissement du taux
de testostérone plasmatique précède le
développement de l’obésité viscérale,
du syndrome métabolique ou du diabète
dans les 10 à 15 années qui suivent
chez des patients dont l’index de masse
corporelle initial est normal (3, 4). Quel
que soit le lien (cause, conséquence
ou simple marqueur précoce d’un état
pathologique latent) entre taux bas de
testostérone plasmatique et risque ulté-
rieur de décès cardiovasculaire ou respi-
ratoire, deux points paraissent être à
retenir à partir de cette étude: en dehors
de toute explication liée au contexte
pathologique ou médicamenteux, un taux
de testostérone < 2,4 ng/ml est un des
paramètres biologiques qui doit inciter à
une vigilance accrue sur la détection ou
la prise en charge des facteurs de risque
cardiovasculaire; a contrario, le facteur
testostéronémie ne s’associe pas à un
risque accru de décès dans les 20 années
à venir si ce chiffre est supérieur à 3 ng/
ml. Reste à démontrer qu’une réascen-
sion du taux de testostérone plasmatique
hors de la zone à risque apporte un réel
bénéfice en termes de mortalité.
JM Kuhn
Harman SM et al. J Clin Endocrinol Metab
2001;86:724-31.
Laughlin GA et al. J Clin Endocrinol Metab
2008;93:68-75.
Derby CA et al. Clin Endocrinol
2006;65:125-31.
Oh JY et al. Diabetes Care 2002;25:55-60.
Mutation activatrice
du gène GPR54
Les études de biologie moléculaire effec-
tuées chez des patients atteints d’hypo-
gonadisme hypogonadotrope congénital
isolé ont permis d’identifier des muta-
tions de plusieurs gènes impliqués dans
le développement embryonnaire ou
dans la mise en route de la maturation
de la fonction gonadotrope. Ainsi, des
anomalies des gènes KAL-1, FGFR1,
GNRHR, GPR54 et NELF ont été identi-
fiées comme responsables de phénotypes
variables dont l’hypogonadisme hypo-
gonadotrope est une constante. Dans
tous les cas décrits, il s’agit de mutations
inactivatrices aboutissant à une perte de
fonction. Les exemples de mutation acti-
vatrice aboutissant à un gain de fonction
sont nombreux en endocrinologie. À cette
date, aucune n’avait été décrite pour les
gènes sus-cités. C’est désormais chose
faite, puisqu’une mutation activatrice de
GPR54 vient d’être identifiée. M.G. Teles
et al. (1) ont formulé l’hypothèse d’une
mutation activatrice du gène GPR54
chez une fillette de 8 ans sur la base de
l’apparition d’une puberté précoce vraie,
c’est-à-dire secondaire à l’initiation d’une
1.
2.
3.
4.
sécrétion gonadotrope. En physiologie,
le système kisspeptine-GPR54 apparaît
impliqué dans l’initiation de la maturation
pubertaire. Il activerait la fonction des
neurones à GnRH et, consécutivement,
la sécrétion gonadotrope. Une mutation
inactivatrice de ce système se traduit par
un déficit gonadotrope congénital, alors
que, image en miroir, une mutation acti-
vatrice doit en toute logique s’associer à
une précocité pubertaire, dépendante des
gonadotrophines, sans qu’aucune lésion
anatomique hypothalamo-hypophysaire
puisse être identifiée sur les examens de
visualisation. C’était le tableau observé
chez cette fillette. L’étude du gène GPR54
a permis d’identifier une mutation ponc-
tuelle, siégeant au niveau du codon 386
et aboutissant au remplacement de l’ar-
ginine par une proline. La transfection du
gène muté dans un systême d’expression
COS-7 a permis de démontrer le carac-
tère activateur de cette mutation. Dans les
conditions basales, cette mutation n’appa-
raît pas augmenter l’activité intrinsèque
constitutive du récepteur, à l’inverse de
ce qui a pu être montré pour le récepteur
LH/hCG au cours de la “testotoxicose”
responsable de pseudopuberté précoce
masculine. En présence de kisspeptine,
l’activité n’apparaît pas supérieure à celle
des cellules exprimant le gène non muté.
C’est au niveau de la mécanique intra-
cellulaire que la différence s’effectue par
rapport au récepteur “sauvage”. Après
stimulation par la kisspeptine, la décrois-
sance du taux d’inositol phosphate intra-
cellulaire est deux fois plus lente dans les
cellules exprimant le récepteur muté que
dans celles qui sont dotées du récepteur
“sauvage”. Ce fait explique très vrai-
semblablement l’activation précoce de
la sécrétion gonadotrope par le système
>>>

108
Métabolismes Hormones Diabètes et Nutrition (XII), n°3, mai-juin 2008
Actualités
Actualités
kisspeptinergique. Le mécanisme invoqué
serait une diminution des phénomènes de
désensibilisation entre la kisspeptine et
son récepteur GPR54. Il s’agit donc là
d’une étude qui jette un nouvel éclairage
sur les facteurs potentiels impliqués dans
certaines des pubertés précoces classées
jusqu’à maintenant dans la rubrique
“idiopathique”.
JM Kuhn
Teles MG et al. N Engl J Med 2008;358:709-15.
La contraception orale
contre le cancer de l’ovaire
La contraception orale a été considérable-
ment développée au cours de la deuxième
moitié du XXesiècle, permettant le
contrôle des naissances dans les pays
industrialisés. Sa pharmacologie a évolué
dans le même temps, donnant naissance
à des formulations de moins en moins
dosées de combinaisons d’œstroproges-
tatifs, ainsi qu’à des pilules contenant
uniquement des progestatifs. La contra-
ception orale a suscité de nombreuses
interrogations sur d’éventuels effets
bénéfiques ou délétères pour la santé. Les
études épidémiologiques visant à évaluer
ses effets à long terme sont rendues extrê-
mement difficiles par la variabilité de la
nature des hormones synthétiques, de
leur dosage, de l’âge de début de traite-
ment, de la durée des traitements et du
nombre de facteurs confondants.
Malgré ces difficultés, un groupe de
travail britannique s’est efforcé d’éva-
luer l’effet de la contraception orale sur
la prévalence du cancer de l’ovaire. Les
auteurs de cet article publié dans The
Lancet ont examiné les données provenant
de 45 études épidémiologiques réalisées
dans 21 pays, totalisant 23257 femmes
ayant eu un cancer de l’ovaire et 87303
n’ayant pas présenté cette pathologie.
Une partie de ces femmes avaient béné-
ficié d’une contraception orale (31% des
patientes et 37% des sujets témoins).
L’analyse des données révèle que
5 années de traitement réduisent de 20%
le risque de cancer de l’ovaire. Ce risque
est réduit de moitié chez les femmes
ayant pris un contraceptif oral durant
1.
15 ans. Cet effet protecteur s’amenuise
avec le temps; il est réduit de 15% 20 à
30 ans après l’arrêt du traitement. L’évo-
lution des formes pharmacologiques
des pilules entre les années 1960 et les
années 1980 n’a pas eu de répercussion
sur leur effet bénéfique. Globalement, les
auteurs estiment que, depuis sa mise sur
le marché, la contraception orale a permis
d’éviter 200000 cancers de l’ovaire, et ils
prévoient qu’elle préviendra l’apparition
de 30000 cas par an durant la prochaine
décennie.
E. Louiset, Laboratoire
de neuroendocrinologie cellulaire
et moléculaire, unité Inserm 413, Rouen
Collaborative Group on Epidemiological Stu-
dies of Ovarian Cancer. Lancet 2008;371:303-14.
Cholestérol et prématurité
Au cours de la grossesse, le métabo-
lisme lipidique est biphasique, avec
une première phase de mise en réserve
et une seconde phase de lipolyse afin
de répondre aux besoins du fœtus. En
clinique, nous nous intéressons peu au
métabolisme lipidique et à ses anomalies
au cours de la grossesse en raison des
difficultés d’interprétation, et surtout de
l’absence de possibilités thérapeutiques.
Il est vraisemblable que certains acteurs
du métabolisme lipidique puissent être
associés à la morbidité fœtale, comme
la macrosomie, même en dehors d’ano-
malies de la tolérance glucidique. La
question qui se pose est de savoir si des
anomalies du métabolisme lipidique,
que ce soit dans un sens ou dans l’autre,
peuvent être responsables d’une morbi-
dité materno-fœtale.
Edison et al. se sont intéressés au taux
de cholestérol de femmes enceintes de
Caroline du Sud, âgées de 21 à 34 ans,
non diabétiques et non fumeuses. Autour
du terme de 17,6 semaines, ce qui corres-
pond au deuxième trimestre de la gros-
sesse, le taux de cholestérol se situe entre
1,59 g/l et 2,61 g/l. Le taux de choles-
térol était ajusté sur l’âge gestationnel
au moment du dépistage. Ces auteurs
ont considéré que le taux de cholestérol
était bas lorsqu’il était inférieur à 1,59 g/l
(10epercentile) et qu’il était normal lors-
qu’il était entre 1,59 g/l et 2,61 g/l. Ils
ont évalué le devenir maternel et fœtal
chez 118 patientes avec cholestérol bas
et 940 femmes avec cholestérol normal,
ce qui constituait la population témoin. Il
a été mis en évidence une augmentation
significative de la prématurité chez les
femmes avec cholestérol bas comparati-
vement à la population considérée comme
normale (12,7% versus 5,0%; p = 0,001).
Le risque de naître prématurément était
plus important chez les nouveaux-nés
de mères avec un cholestérol bas que
chez les nouveaux-nés de mères avec
un cholestérol normal (OR = 2,93; IC95
[1,51-5,56]; p = 0,001). Le risque d’ac-
couchement prématuré était également
plus élevé chez les femmes avec hyper-
cholestérolémie que chez celles avec
un cholestérol normal (OR = 2,66; IC95
[1,39-5,09]; p = 0,003). Ce risque a été
mis en évidence uniquement chez les
femmes de race blanche. Les femmes
de race noire ne sont pas concernées.
Les poids de naissance des enfants de
mères avec cholestérol bas étaient infé-
rieurs en moyenne de 147 g comparati-
vement aux enfants nés de mères avec
cholestérol normal après ajustement sur
les facteurs confondants habituels. Il n’a
pas été démontré de relation entre niveau
de cholestérol chez la mère et malfor-
mations congénitales, ni entre niveau de
cholestérol et macrosomie.
Bien que ces résultats méritent d’être
confirmés, ce travail démontre que les
anomalies lipidiques peuvent être asso-
ciées à une morbidité materno-fœtale au
cours de la grossesse normale. L’hypo-
cholestérolémie serait plus particulière-
ment associée à un risque de prématurité,
pouvant par conséquent être un marqueur
de risque en dehors de ceux déjà connus.
Il semble donc nécessaire de réaliser des
études prospectives permettant d’évaluer
les profils lipidiques au cours de la gros-
sesse, ainsi que l’association à une morbi-
dité materno-fœtale. Il apparaît également
intéressant d’évaluer l’impact des anoma-
lies lipidiques au cours de pathologies
comme la grossesse diabétique.
A. Vambergue, CHRU de Lille.
Edison RJ et al. Pediatrics 2007;120:723-33.
>>>
1
/
4
100%