Télécharger

1
Introduction à la Physique des Matériaux
Correction du devoir 4 : La liaison cristalline
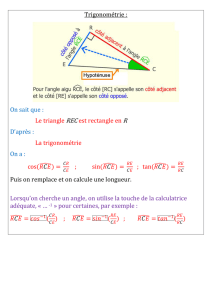
Exercice 1 : Calcul de l’énergie de cohésion d’un cristal moléculaire – Application au CO2
Partie A : Interaction entre deux dipôles électrostatiques
1.a. Le potentiel au point M :
00
44
qq
VM AM BM
0
4q BM AM
VM AM BM
Dans les triangle OAM et OBM :
2
22
4cos
a
AM r ar
2
22
4cos
a
BM r ar
1
22
2
14
cosaa
AM r rr
1
22
2
14
cosaa
BM r rr
Puisque a<<r, on effectue un développement limité de la racine carré au premier ordre ce qui donne :
12
cosa
AM r r
r
a
rBM 2
1
cos
2
AM BM r
D’où :
2
0
4
cosqa
Vr
b. On rappelle que
E gradV
,
1
r
VV
E e e
rr
33
00
1 2 1
44
cos sin
r
pp
E e e
rr
c. L’énergie potentielle d’un dipôle placé dans un champ électrique extérieur
0
E
:
0
EpUp
.
A
O
M
j
i
+q
-q
a
B
www.9alami.com

2
d. Le couple
qu’exerce ce champ sur le dipôle
p
:
0
pE
2. Considérons les deux dipôles de moments dipolaires
1
p
et
2
p
:
a. L’énergie potentielle des deux dipôles est :
12 EpUp
.
=
2 2 1 2 2 1
cos sin
r
p E p E
En remplaçant les coordonnées polaires du vecteur
1
E
par leur valeurs on obtient :
12 1 2 1 2
3
0
2
4cos cos sin sin
ppp
Ur
b. Les couples
1
et
2
sont perpendiculaires au plan contenant les deux dipôles :
12
1 1 2 1 2
3
20
12
4cos sin sin cos
p
Upp
r
12
2 1 2 1 2
3
10
12
4sin cos cos sin
p
Upp
r
c. Les positions d’équilibre correspondent à :
12
0
Soit :
12
12
0
0
12
12
0
0
sin
sin
L’équilibre est stable si
p
U
est négative.
2
1
0
2
32
0
stable
instable
2
instable
stable
instable
stable
32
stable
instable
3. Deux cas peuvent se présenter :
Cristal formé d’une molécule polaire
Dans ce cas chaque moment dipolaire va interagir avec les champs électriques crées par les autres moments
dipolaire.
O2
O1
2
p
1
p

3
Cristal atomique ou molécule apolaire
A cause du mouvement des électrons autour du noyau la distribution de charge électronique change au cours
du temps comme le montre la figure suivante pour le CO2 :
A la date t, la densité électronique au niveau de la molécule est uniforme, le moment dipolaire
p
=
0
.
A une date t’, la densité électronique au niveau de la molécule n’est plus uniforme, un moment dipolaire
p
0
est alors induit qui produira un champ électrique
E
au centre d’une autre molécule de CO2. Ce
champ engendrera un moment dipolaire instantané
p
’ ce qui entraînera une interaction entre les deux
moments
p
et
p
’ conformément à ce qui a été décrit dans les questions précédentes.
4. On a :
1
13
0
12
4p
Er
1
21 3
0
12
4p
pE r
D’après la question 2.a :
2
12 2
36
00
2 4 1
44
attractive p p p
Urr
6
attrctive C
Ur
La constante C est donnée par :
2
2
0
4
4
p
C
4. En négligeant l’énergie cinétique et les vibrations des deux dipôles, On a :
6 12
TCD
Ur rr
5. a. On a :
6 12
4UR RR
D’après la question 4 :
6 12
CD
UR RR
En identifiant les deux expressions :
6
12
4
4
C
D
Ce qui donne :
p

4
1
6
2
4
D
C
CD
b. Tracé de l’allure de la courbe :
4
UR fR
On pose :
4
UR y
xR
0.0 0.4 0.8 1.2
x
-1
0
1
2
3
4
5
6
y = x12 - x6
2
-1/6
x = 1
L’évolution de l’interaction évolue de la manière suivante :
- Lorsque les deux molécules sont éloignés R = ∞ (x = 0), dans ce cas le potentiel est nul ;
- quand la distance R diminue (x croit) l’énergie potentielle est négative (attractive) diminue et passe par un
minimum pour x =
1
6
2
qui correspond à la position d’équilibre ;
- pour
1
6
21x
, R décroît de
1
6
2
à
, l’énergie potentielle d’attraction diminue et l’énergie de répulsion
augmente ;
- à partir de x = 1 (R =
) l’énergie potentielle devient positive il y a répulsion.
6. Soit rij la distance entre deux molécules i et j et R la distance entre les premiers proches voisins et N le
nombre d’éléments du cristal.
a. On pose : rij = pij
R
12 6
12 6
11
4
ij ij ij ij
Ur rr

5
12 6
12 6
12 6
11
4 1 4 1
jj
Totale ij ij
jj
j i j i
NN
UR p R p
12 6
12 6
12 6
11
2 1 2 1
jj
Totale ij ij
jj
NN
UR p R p
b. Pour un réseau c.f.c, la contribution des proches voisins dans le premier cube :
Vue dans le plan (Oxy)
Couleur
Ordre
j
R
j
R
Nombre
pj
0
000,,
0
0
1
110
22
,,
12
12
1
2
1 0 0,,
1
6
2
3
11
122
,,
3
2
24
3
4
11 0,,
2
12
2
5
310
22
,,
10
4
24
5
6
111,,
3
8
6
6
6
A
=
6 6 6
6
66
1 1 1 1 1 1
12 6 24 12 24 8
1 2 3 2 5 6
= 14.05543
6
12
A
=
12 12 12
12
12 12
1 1 1 1 1 1
12 6 24 12 24 8
1 2 3 2 5 6
= 12.13131
c. On a :
6
A
=
6
1
1
j
ij
jp
= 14,45392
12
A
=
12
1
1
j
ij
jp
= 12,13188
On déduit que :
 6
6
 7
7
 8
8
1
/
8
100%