Lire l'article complet

6 | La Lettre de l’Hépato-gastroentérologue • Vol. XIV - n° 1 - janvier-février 2011
DOSSIER THÉMATIQUE
Gestion des traitements
des hépatites B et C
L’observance :
le principal facteur
d’efficacité du traitement
par les analogues anti-VHB
Adherence: the main factor associated with the efficacy
of antiHBV analogues
Philippe Sogni*, Vincent Leroy**
* Université Paris-Descartes, Inserm
U1016, et service d’hépatologie,
hôpital Cochin, Paris.
** Clinique universitaire d’hépato-
gastroentérologie, Inserm U823,
CHU de Grenoble.
E
n France métropolitaine, les taux de positi-
vité de l’AgHBs et de l’anticorps anti-HBc sont
estimés à 0,66 et 8,18 % respectivement
(1)
.
Les indications du traitement antiviral B ont été
récemment réévaluées par des experts européens
(2)
.
Les analogues de deuxième génération en monothé-
rapie, entécavir (ETV) ou ténofovir (TDF), ou l’inter-
féron pégylé apparaissent comme le meilleur choix
en première ligne pour les patients n’ayant jamais été
traités
(2)
. En France, la grande majorité des patients
traités pour le VHB le sont par analogues
(3)
.
Les analogues nucléos(t)idiques de deuxième généra-
tion permettent une réponse virologique, définie par
une indétectabilité de l’ADN-VHB après 48 semaines
de traitement (2), chez la plupart des patients, quels
que soient le type de virus (AgHBe+ ou AgHBe–), la
sévérité de l’hépatopathie sous-jacente (cirrhose
ou non) ou le statut immunitaire des malades.
Le but du traitement est alors de maintenir une
virosuppression, mesurée par des tests sensibles
(ADN-VHB < 10-20 UI/ml par PCR), sur le très long
terme, voire la vie durant. Avec les analogues de
deuxième génération, qui ont une puissance antivi-
rale élevée, le risque de résistance chez les patients
traités en première ligne ne se pose quasiment pas
en pratique clinique. Aucune mutation de résistance
n’a été décrite à 4 ans avec le TDF (4), et le taux de
résistance virologique est inférieur à 1 % avec l’ETV à
6 ans (5). À l’avenir, les deux problèmes seront donc,
d’une part, celui de la tolérance à long terme de ces
molécules et, d’autre part, celui de l’observance à
ce traitement chronique.
Quels sont les défauts
d’observance décrits
en pratique ?
Trois types de défauts d’observance sont décrits pour
les traitements chroniques : d’abord, l’absence de
début de traitement, malgré la prescription médi-
cale, correspondant à un défaut d’adhésion au projet
thérapeutique ; ensuite, l’arrêt prématuré du traite-
ment, dont la fréquence s’exprime comme l’opposé
du taux de rétention (ou de persistance) dans les
études d’observance ; enfin, la prise irrégulière du
traitement, qui peut aller du non-respect des horaires
de prise jusqu’à l’absence intermittente de prise.
C’est ce dernier point que nous allons détailler dans
cet article. Sur le plan quantitatif, l’observance est le
plus souvent définie comme le ratio entre le nombre
de comprimés prescrits et le nombre de comprimés
réellement pris par le malade pendant une période
donnée. Un défaut d’observance est défini par un
ratio inférieur à 100 %, ou d’autres seuils arbitraires
(80 ou 90 %) en fonction du niveau souhaité.
La mauvaise observance
est-elle fréquente au cours
d’un traitement chronique ?
Une observance non optimale est une situation
fréquente pour un traitement chronique, quelle que
soit la pathologie (6) [tableau I]. Pour le traitement
anti-VIH, il est bien démontré qu’une observance

La Lettre de l’Hépato-gastroentérologue • Vol. XIV - n° 1 - janvier-février 2011 | 7
Points forts
»Le traitement de l’hépatite chronique B par analogues est un traitement chronique.
»
L’observance est le principal facteur associé à la virosuppression et à son maintien dans la durée, surtout
avec les analogues anti-VHB de deuxième génération, pour lesquels le risque de résistance est faible ou
nul en première ligne.
»
La bonne observance doit être préparée et surveillée au cours du traitement par analogues anti-VHB
pour prévenir les risques d’échec virologique.
Mots-clés
Hépatite B
Analogues
Observance
Virosuppression
Keywords
Hepatitis B
Analogues
Adherence
Virosuppression
insuffisante est la première cause d’échec du traite-
ment et de développement de résistances (7). Si l’ori-
gine géographique et le niveau socio-économique
peuvent jouer un rôle, une méta-analyse a montré
que l’observance aux traitements anti-VIH était
meilleure dans les études menées en Afrique sub-
saharienne qu’en Amérique du Nord (8) [figure 1].
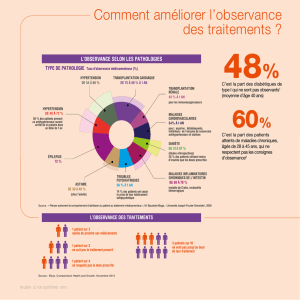
En dehors des études d’enregistrement, les données
“dans la vraie vie” pour le traitement chronique par
analogues anti-VHB sont peu nombreuses. Une
étude américaine récemment publiée a montré
qu’une observance de plus de 90 % était notée
uniquement chez 55 % des patients en cours de
traitement par analogues, et que l’observance était
plus faible chez les patients en début de traitement
que chez ceux qui étaient traités depuis plus d’un
an (9) [figure 2, p. 8]. Une étude de cohorte mono-
centrique française réalisée chez 190 patients traités
depuis au moins 3 mois par différents analogues a
montré qu’une observance totale n’était notée que
chez 61 % d’entre eux (10).
Comment mesurer
l’observance ?
L’observance est souvent difficile à évaluer. Il existe
des méthodes directes ou indirectes, chacune ayant
ses avantages et ses défauts. Les méthodes directes
ont l’avantage de donner des mesures objectives,
et elles sont habituellement réservées aux études
pré-AMM. Il est ainsi possible de doser dans le sang les
concentrations d’ADV et de TDF. L’interprétation des
dosages est toutefois difficile et nécessite de connaître
l’heure de la dernière administration du médicament.
En revanche, une concentration nulle de médicament
dans le sang signe un défaut d’observance récent.
Une technique alternative souvent utilisée dans les
essais cliniques est le compte des comprimés restants
dans les boîtes délivrées ou à l’aide de méthodes plus
sophistiquées telles que les piluliers électroniques. Les
méthodes indirectes sont habituellement réservées
aux études observationnelles de phase IV. Il peut
s’agir du compte des boîtes de médicaments délivrées
par les pharmacies (méthode souvent utilisée aux
États-Unis, où il existe des fichiers informatisés de
délivrance). En pratique clinique, les questionnaires
administrés par un tiers ou les autoquestionnaires ont
été les plus utilisés, notamment dans le VIH. Dans
l’étude de cohorte monocentrique française citée plus
haut (10), un autoquestionnaire était remis au patient.
Cet autoquestionnaire et l’algorithme permettant de
classer l’observance (trois classes : totale, modérée,
mauvaise) sont accessibles librement sur la page d’ac-
cueil du site de l’Association française pour l’étude
du foie (www.afef.asso.fr/).
Quelles sont les conséquences
d’une mauvaise observance
aux analogues anti-VHB ?
Une mauvaise observance apparaît clairement
comme un risque de réponse virologique partielle.
Tableau I. Observance rapportée dans les études cliniques en fonction de la pathologie (d’après 6).
Pathologies Observance moyenne (%) Extrêmes (%)
Cancer 80 35-97
Cardiovasculaires 71 39-93
Épilepsie 70 46-88
Infertilité 71 34-97
Glaucome 78 76-80
Maladies infectieuses 74 40-92
Médecine générale 75 51-85
Psychiatrie 78 75-83
Maladies respiratoires 54 37-92
Amérique du Nord
31 études (17 573 patients)
0,55 (0,49-0,62)*
0 0,2 0,4 0,6 0,8 1,0
*OR (IC95) : on retrouve une meilleure observance dans les études réalisées en Afrique subsaharienne que dans celles
réalisées en Amérique du Nord.
Afrique subsaharienne
27 études (12 116 patients)
0,77 (0,68-0,85)*
0 0,2 0,4 0,6 0,8 1,0
Figure 1. Proportion de patients VIH+ maintenant une bonne observance au traitement
antiviral tout au long des études (seuils variant de 80 à 100 %) en fonction de la région
où se déroulent ces études (d’après 8).

8 | La Lettre de l’Hépato-gastroentérologue • Vol. XIV - n° 1 - janvier-février 2011
DOSSIER THÉMATIQUE
Gestion des traitements
des hépatites B et C L’observance : le principal facteur d’efficacité
du traitement par les analogues anti-VHB
Dans l’étude de cohorte monocentrique française
citée plus haut, une mauvaise observance était, en
analyse multivariée, un facteur indépendant associé
à l’absence de virosuppression (10) [tableau II].
Dans une deuxième étude française menée chez
47 malades traités par ADV, un taux d’ADN-VHB
indétectable à 4 ans était plus souvent retrouvé chez
les malades ayant une bonne observance (68 %)
que chez ceux ayant une mauvaise observance
(32 %) [11].
Un défaut d’observance peut également être en
cause en cas d’échappement virologique. Très récem-
ment, Chotiyaputta et al. (12) ont montré, chez
111 malades traités par différents analogues, que le
risque d’échappement virologique était de 19 % chez
les malades ayant une observance inférieure à 100 %
et de 2 % chez ceux ayant une observance à 100 %
sur la période de suivi. Dans l’étude française précitée
concernant l’ADV, un échappement était observé
chez 35 % des malades à 4 ans (11). Au moment de
l’échappement, une mutation de résistance était
retrouvée dans la moitié des cas, alors que l’ADV était
indosable dans le sang chez la moitié des malades
restants (11). La situation semble toutefois différente
en fonction du type d’analogue utilisé et de son profil
de résistance. Une étude rétrospective a comparé
les causes d’échec du traitement chez les patients
traités par analogues de première génération – en
l’occurrence l’ADV – ou par analogue de deuxième
génération – en l’occurrence l’ETV (figure 3) [13].
Avec ce dernier traitement, étant donné la puissante
barrière génétique de ces molécules de deuxième
génération, les seuls échecs observés étaient dus
à une observance insuffisante. En revanche, avec
l’ADV, les échecs étaient dus soit à une mauvaise
< 50 % 51-60 % 61-70 % 71-80 %
81-90 % 91-95 % > 95 %
Nouveaux (n = 458)
La poursuite du traitement est plus assurée chez les patients en cours de traitement
que chez les patients débutant un traitement : 81 ± 3 % versus 73 ± 3 % (p < 0,05).
Une observance supérieure à 90 % est plus fréquente chez les patients en cours de traitement
que chez les patients débutant un traitement : 55 versus 50 % (p < 0,05).
En cours (n = 10 295)
40 %
11 %
18 %
9 %
10 %
5 % 9 %
6 %
4 % 6 %
46 %
9 %
19 %
11 %
Figure 2. Poursuite du traitement et observance mesurées par la délivrance en pharmacie
chez des patients traités par différents analogues de première ou deuxième génération
(d’après 9).
Tableau II. Facteurs associés à la virosuppression (ADN-VHB < 12 UI/ml) en analyse multivariée
dans une étude de cohorte monocentrique de 190 patients traités par différents analogues
(d’après 10).
OR IC95 p
ADN-VHB initial* 0,74 0,64-0,98 0,035
Au moins un changement d’analogue(s) 3,03 1,19-7,69 0,021
Mauvaise observance** 0,23 0,06-0,91 0,036
* ADN-VHB inférieur ou supérieur à 6 log UI/ml (médiane).
** Mauvaise observance comparée à observance totale et observance modérée.
1
000 0
0
Patients (%)
66
16
2
Années de suivi
Entécavir
Échecs virologiques
34
Résistance Mauvaise observance
1
02
13
22
1
Patients (%)
646
2
Années de suivi
Adéfovir
Échecs virologiques
34
Figure 3. Analyse de la cause des échecs virologiques (résistance ou mauvaise observance) dans une cohorte rétrospective de 149 patients asiatiques
AgHBe- traités par entécavir (0,5 mg/j) ou par adéfovir (10 mg/j) [d’après 13].

La Lettre de l’Hépato-gastroentérologue • Vol. XIV - n° 1 - janvier-février 2011 | 9
DOSSIER THÉMATIQUE
observance soit à la sélection de mutants résis-
tants à l’ADV. Dans ce dernier cas, d’ailleurs, on
peut suspecter le rôle favorisant d’une observance
non optimale préalable, favorisant la sélection d’un
mutant résistant. Ce rôle potentiellement favori-
sant d’une mauvaise observance sur la sélection de
mutants résistants, décrit dans l’infection à VIH, n’est
toutefois pas démontré dans l’hépatite B.
Quels sont les facteurs
jouant sur l’observance ?
Les facteurs qui déterminent l’observance dépen-
dent du patient, du traitement, de la maladie et du
médecin (tableau III) [14, 15]. Il est important d’ap-
précier toutes ces composantes avant de démarrer
le traitement et d’en tenir compte dans le suivi au
long cours. Notamment, il ne faut pas ignorer le rôle
du médecin, de sa conviction, de ses explications,
et celui du lien médecin-malade qu’il a su tisser,
sur l’optimisation de l’observance. Parmi les autres
éléments à prendre en compte, il ne faut pas oublier
que l’hépatite chronique B est le plus souvent asymp-
tomatique et que le traitement, donné le plus souvent
en prévention d’une complication, n’apporte pas de
bénéfice symptomatique perceptible pour le patient.
En conclusion : comment
améliorer l’observance ?
L’amélioration de l’observance passe avant tout par
la prise de conscience du fait qu’une bonne obser-
vance ne va pas de soi, et que toute prescription
thérapeutique justifiée sur le plan scientifique ne
s’accompagne pas obligatoirement d’une observance
à 100 % sur le long terme par le patient.
Tout d’abord, une bonne observance se prépare
en choisissant le bon moment pour le début
du traitement, non seulement du point de vue
médical, mais aussi en tenant compte du contexte
psychologique, familial ou socio-professionnel du
patient, qui pourrait obérer son adhésion au projet
thérapeutique.
Une bonne observance se surveille ensuite tout au
long du traitement, sur une plus longue période,
au terme de laquelle il sera possible de mesurer
les conséquences virologiques puis cliniques d’une
mauvaise observance. Cette surveillance peut se
faire par des autoquestionnaires (10). Elle peut se
faire également en posant les bonnes questions au
cours de la consultation. Ainsi, poser la question
“prenez-vous bien votre traitement ?” entraîne
une réponse invariablement positive. En revanche,
poser la question “vous est-il arrivé d’oublier une
fois la prise de votre traitement durant les 3 derniers
mois ?” apporte souvent son lot de surprises pour
le médecin curieux. ■
Tableau III. Principaux facteurs connus associés à une mauvaise observance (d’après 14, 15).
Présence de troubles psychologiques (dépression)
Présence de troubles cognitifs
Traitement d’une maladie asymptomatique
Suivi inadéquat
Effets indésirables du traitement
Le patient n’est pas convaincu du bénéfice du traitement
Le patient ne s’investit pas dans sa maladie
Mauvaise relation médecin-malade
Présence d’obstacles à la prise en charge
Rendez-vous manqués
Complexité du traitement
Coût du traitement ou surcoût pour le patient
1. Meffre C, Le Strat Y, Delarocque-Astagneau E et al.
Prevalence of hepatitis B and hepatitis C virus infections in
France in 2004: social factors are important predictors after
adjusting for known risk factors. J Med Viral 2010;82:546-55.
2. EASL Clinical Practice Guidelines: Management of chronic
hepatitis B. J Hepatol 2009;50:227-42.
3. Marcellin P, Cadranel JF, Fontanges T et al. High rate of
adefovir-lamivudine combination therapy in nucleoside-
naïve patients with chronic hepatitis B in France: results
of a national survey in 1730 patients. Eur J Gastroenterol
Hepatol 2010;22:1290-6.
4. Snow-Lampart A, Chappell B, Curtis M et al. No resistance
to tenofovir disoproxil fumarate detected after up to 144
weeks of therapy in patients monoinfected with chronic
hepatitis B virus. Hepatology 2011 (in press).
5. Tenney DJ, Pokornowski KA, Rose RE et al. Entecavir main-
tains a high genetic barrier to HBV resistance through 6
years in naïve patients. J Hepatol 2009;50(Suppl.1):S10.
6. Claxton AJ, Cramer J, Pierce C. A systematic review of
the associations between dose regimens and medication
compliance. Clin Ther 2001;23:1296-310.
7. Gardner EM, Burman WJ, Steiner JF, Anderson PL, Bangs-
berg DR. Antiretroviral medication adherence and the deve-
lopment of class-specific antiretroviral resistance. AIDS
2009;23:1035-46.
8. Mills EJ, Nachega JB, Buchan I et al. Adherence to antire-
troviral therapy in sub-Saharan Africa and North America:
a meta-analysis. JAMA 2006;296:679-90.
9. Chotiyaputta W, Peterson C, Ditah FA et al. Persistence
and adherence to nucleos(t)ide analogue treatment for
chronic hepatitis B. J Hepatol 2011;54:12-8.
10. Sogni P, Fontaine H, Mallet V et al. Adherence to
anti-HBV analogues in clinical practice is associated
with virological efficacy and depends on the duration
of treatments and the physician’s experience. J Hepatol
2010;52(Suppl.1):S395.
11. Hilleret MN, Larrat S, Stanke F et al. Le suivi pharmaco-
logique des antiviraux est un outil utile dans le dépistage
de la non-compliance au cours du traitement des hépatites
virales B. AFEF 2009;CA-43.
12. Chotiyaputta W, Oberhelman K, Hongthanakorn C et al.
Correlation between self-reported adherence to nucleos(t)
ide analog therapy for chronic hepatitis B and virological
breakthroughs. Hepatology 2010;52(Suppl.1): 542A.
13. Ha NB, Ha NB, Garcia RT et al. Noncompliance, anti-
viral resistance and virological response in treatment-naïve
HBeAg-negative patients with chronic hepatitis B on long-
term therapy with Entecavir 0.5 mg or Adefovir 10 mg in a
real-life clinical setting. Hepatology 2009;50(Suppl.):513A.
14. Osterberg L, Blaschke T. Adherence to medication.
N Engl J Med 2005;353(5):487-97.
15. Pol S, Sogni P. Traitement de l’hépatite chronique
B : observance et tolérance. Gastroenterol Clin Biol
2010;34:S142-9.
Références bibliographiques

10 | La Lettre de l’Hépato-gastroentérologue • Vol. XIV - n° 1 - janvier-février 2011
DOSSIER THÉMATIQUE
Gestion des traitements
des hépatites B et C L’observance : le principal facteur d’efficacité
du traitement par les analogues anti-VHB
Surveillance en pratique d’un patient traité pour une hépatite chronique B
Philippe Sogni (service d’hépatologie, hôpital Cochin, Paris)
Encadré.
La surveillance du traitement va dépendre de la gravité initiale de la
maladie et du type de traitement. Une évaluation initiale est importante
non seulement sur le plan hépatique mais également sur le plan rénal.
La surveillance va s’attacher à évaluer l’efficacité et la tolérance du trai-
tement ainsi que l’absence de survenue de complications hépatiques
de l’hépatite B.
Évaluation initiale d’un patient mono-infecté par le VHB avant
la mise en route du traitement
• L’évaluation initiale devra informer le patient du diagnostic et des
risques potentiels de la maladie mais également de la nécessité d’un
suivi et du fait que, le traitement n’étant pas obligatoire, sauf dans les
formes graves d’emblée, il sera décidé ou non après un suivi initial d’une
durée habituelle de 6 à 12 mois.
• Évaluation minimale initiale
– NFS, plaquettes, TP, bilan hépatique, créatinine, phosphorémie,
alpha-fœtoprotéine
– Bandelette urinaire
– Échodoppler du foie
• Suivi initial : tous les 3 mois pendant 1 an, le plus souvent avant de
commencer éventuellement un traitement
– Transaminases
– ADN-VHB (utiliser un test sensible avec un seuil de détection
10-20UI/ml)
• Évaluer le stade de fibrose (après le suivi initial puis en fonction de
l’évolution)
– Tests non invasifs si transaminases normales et ADN-VHB
<2 000UI/ml
– PBH si ALAT > normale ou si ADN-VHB > 2 000 UI/ml (en l’absence
de signe évident de cirrhose)
Suivi de l’efficacité pendant le traitement par analogues
• Un traitement par analogues est un traitement chronique. L’obser-
vance est donc un objectif majeur. L’adhésion au projet thérapeutique
doit être obtenue avant de commencer ce traitement, qui habituelle-
ment n’est pas une urgence thérapeutique.
• ADN-VHB tous les 3 mois initialement puis tous les 6 mois après
virosuppression, cela dépendant surtout de l’observance au traitement.
Avec un traitement par analogue de deuxième génération, le but est
d’avoir un ADN-VHB négatif (< 10-20 UI/ml) à 48 semaines. Si ce but
n’est pas atteint, le plus souvent la poursuite de ce traitement permettra
d’obtenir une virosuppression à 72 semaines.
• Les autres marqueurs d’efficacité sont :
– La normalisation des transaminases - En l’absence de normalisa-
tion malgré une virosuppression efficace, se posera la question d’une
autre cause à cette augmentation (syndrome métabolique, co-infec-
tion, comorbidités, etc.).
– La séroconversion HBe (si AgHBe+ initialement), puis séroconver-
sion HBs à long terme.
– La régression de la fibrose, qui est sans doute un but majeur pour
juger de l’efficacité du traitement au long cours et sur le risque de
complication, notamment chez les patients avec une cirrhose initia-
lement. Cependant, à l’heure actuelle, la seule méthode fiable pour
évaluer la régression de la fibrose est la biopsie à long terme chez un
patient virosupprimé.
• Préparer et vérifier la bonne observance au traitement chronique, qui
est le principal facteur associé à l’efficacité du traitement par analogues.
Suivi de l’efficacité pendant un traitement par interféron pégylé
• Le but est d’obtenir un ADN-VHB < 2 000 UI/ml à la fin du traite-
ment (48 semaines) et à distance de l’arrêt de celui-ci, ainsi qu’une
séroconversion HBe (si AgHBe+ initialement) et une séroconversion
HBs à distance. L’arrêt du traitement par interféron sera habituel dès
24 semaines (avec un changement pour un analogue) si l’ADN-VHB
reste > 2 000 UI/ml.
Suivi de l’absence de complications hépatiques
• Bilan hépatique et TP tous les 3 à 6 mois.
• Échographie et alpha-fœtoprotéine tous les 6 à 12 mois en fonction
de la gravité de la maladie hépatique (suivi habituel d’une cirrhose si
nécessaire).
Tolérance des traitements
• Tolérance à l’interféron pégylé – Le traitement par interféron pégylé
est habituellement de 12 mois. Les effets secondaires éventuels devront
être expliqués au patient et un suivi rapproché (médecin spécialiste,
médecin généraliste et éventuellement infirmière) devra être organisé,
et adapté à chaque patient. Les effets secondaires potentiels et le suivi
sont les mêmes que ceux rencontrés au cours du traitement de l’hépa-
titeC
(lire encadré, p. 23)
.
• Tolérance aux analogues anti-VHB – Les effets secondaires sont
détaillés dans les fiches d’AMM des produits. Néanmoins, ces molécules
sont habituellement bien tolérées, avec des effets secondaires ordinai-
rement non différents de ceux du placebo pour la majorité d’entre eux.
Il est important cependant de surveiller ces médicaments, qui vont être
poursuivis sur le long terme.
• Tolérance rénale
– Il est important d’adapter la dose de tout analogue à la fonction
rénale (à partir d’une clairance de la créatinine < 50 ml/mn). Donc,
pour toutes les molécules, il faudra vérifier la fonction rénale tous
les 3 à 6 mois en fonction de la molécule, de la fonction rénale, des
comorbidités (HTA, diabète, etc.) ou des traitements concomitants,
éventuellement pris en automédication (AINS).
– Mesure de la pression artérielle
– Bilan sanguin à jeun : créatinine, phosphore
– Analyse d’urine sur échantillon du matin : créatinine, phosphore,
protéine (ou, à défaut, bandelette urinaire).
– La question d’une éventuelle toxicité tubulaire rénale des
ana logues nucléotidiques (adéfovir et ténofovir) reste débattue et
nécessite la surveillance d’une possible fuite rénale de phosphore,
qui en est un signe précoce.
• Tolérance osseuse – Le risque de fuite urinaire de phosphore avec les
inhibiteurs nucléotidiques pourrait entraîner une diminution de la miné-
ralisation osseuse. À l’heure actuelle, cette question reste en suspens.
• Risque d’acidose lactique – Des cas d’acidose lactique chez des
patients cirrhotiques traités par entécavir, dont l’état de santé était
particulièrement grave (MELD ≥ 22), ont été rapportés. Il est raison-
nable de surveiller ce type de complication avec tout analogue chez les
patients cirrhotiques décompensés.
• EASL Clinical Practice Guidelines: Management of chronic hepatitis B. J Hepatol
2009;50:227-42.
• Lok ASF, McMahon BJ. AASLD Practice Guidelines. Chronic Hepatitis B: Update 2009.
Hepatology 2009;50:1-36.
1
/
5
100%