Rythmologie R Y T H M O L O G I E

RYTHMOLOGIE
La Lettre du Cardiologue - Supplément au n° 341 - janvier 2001
26
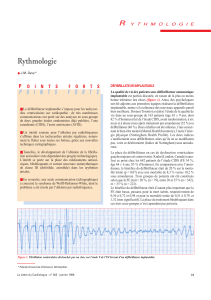
FLUTTER ET FIBRILLATION AURICULAIRES
Le risque embolique du flutter
Le risque thromboembolique du flutter est de plus en plus dis-
cuté. Cent trente-quatre patients (70 ans, de 44 à 91 ans) avec un
flutter de durée médiane 33 jours, sans aucune FA documentée,
ont été analysés par échographie transthoracique et échographie
transœsophagienne pour 94 % d’entre eux. Un thrombus a été
diagnostiqué chez 3 patients (2,5 % ; 2 dans l’auricule et 1 dans
l’oreillette droite), un contraste important chez 16 patients (13 %)
et des débris intra-aortiques chez 10 patients (8 %). Les facteurs
prédictifs d’un contraste important étaient l’âge, le traitement
digitalique et l’existence d’un VG dilaté et/ou hypokinétique. Le
flutter a été réduit par cardioversion chez 93 patients, dont 34
sous antivitamine K, et, après un mois de suivi, 2 accidents embo-
liques ont été relevés : 1 embolie pulmonaire et 1 AVC mortel.
(G. Corrado, Côme, 2996).
Dans une autre étude portant sur 12 patients avec un flutter chro-
nique (187 ± 58 jours de durée moyenne) bénéficiant d’une abla-
tion par radiofréquence et non anticoagulés, les facteurs de la coa-
gulation ont été analysés. Les valeurs étaient anormales dans plus
de la moitié des cas : fragments prothrombiniques 1 et 2 (4/12),
complexe thrombine-antithrombine III (7/12), facteur VIIIc
(7/12), facteur de Willebrand (6/12) et divers (6/12).
De façon similaire à la fibrillation auriculaire, le flutter chro-
nique active les facteurs de la coagulation et semble donc majo-
rer le risque thrombogène. (B. Herweg, New York, 2998).
Le risque embolique de la cardioversion électrique du flutter auri-
culaire a été analysé de façon rétrospective pour 493 patients et
615 cardioversions. Le succès a été obtenu 570 fois (93 %). Des
anticoagulants avaient été prescrits dans 415 cas (67 %). Trois
accidents emboliques devaient survenir dans les 30 jours suivant
le choc électrique (0,5 % des chocs réussis, intervalle de
confiance 0,1 à 1,5 %). Deux des 3 patients n’étaient pas anti-
coagulés, et le troisième avait une anticoagulation insuffisante.
Aucune embolie ne survenait chez les 187 patients bien anticoa-
gulés. Au total, le risque embolique de la cardioversion du flut-
ter n’est pas nul et semble lié au succès de la cardioversion et
à l’absence d’anticoagulant. Il est semblable alors à celui
de la fibrillation auriculaire (3/318, soit 0,9 %). (A. Elhendy,
Rochester, 1920).
Cardioversion de la fibrillation auriculaire
Une étude prospective randomisée en simple aveugle et contrô-
lée contre placebo a été rapportée chez les patients présentant une
fibrillation récente de moins de 48 heures. Deux cent quatre-vingt-
dix-neuf patients (65 ± 11 ans, 34 à 86 ans) ont été traités par voie
veineuse, soit :
– par procaïnamide (n = 65) 1 g sur 30 mn puis 2 mg/mn/24 h ;
– par propafénone (n = 61) 2 mg i.v. sur 15 mn puis 10 mg/kg/
24 h ;
Rythmologie
●
J.M. Davy*
■
L’actualité rythmologique reste “rythmée” par la fibril-
lation et le flutter auriculaires (cardioversion, ablation)
et les arythmies malignes (défibrillateur implantable,
affections génétiques) :
❏le risque embolique du flutter n’est pas négligeable
et semble imposer des précautions identiques à celui de
la fibrillation auriculaire (FA) en cas de cardioversion ;
❏l’ablation des foyers veineux pulmonaires respon-
sables de la FA devient plus rapide, grâce à une sonde
à ballonnet placée à l’orifice des veines pulmonaires,
réalisant une isolation électrique circonférentielle ;
❏l’étude AMIOVIRT, comparant amiodarone et défi-
brillateur (DAI), rappelle que les indications du DAI
dans les cardiomyopathies ne sont probablement pas
celles du post-infarctus ;
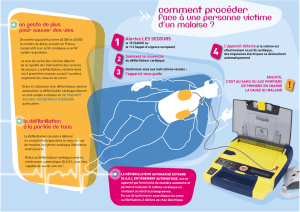
❏l’accès du public au défibrillateur semi-automatique
(DSA) suscite, après l’expérience d’aéroports comme
celui de Chicago, de plus en plus d’intérêt ;
❏affection génétique responsable de mort subite, le syn-
drome de Brugada reste bien mystérieux : comme pour
le QT long congénital, les porteurs sains existent, géné-
tiquement atteints mais cliniquement normaux ; par
ailleurs, un bon pronostic peut être associé aux anoma-
lies ECG si elles sont isolées.
Points forts
* Hôpital Arnaud-de-Villeneuve, Montpellier.

– par amiodarone (n = 87) 300 mg i.v. sur 60 mn puis
20 mg/kg/24 h ;
– par placebo (n = 77).
Tous les patients recevaient la digoxine. La réduction a été obser-
vée respectivement chez 69 %, 82 %, 88 % et 61 % d’entre eux,
l’amiodarone et la propafénone étant plus efficaces que le pla-
cebo ou la procaïnamide (p < 0,05). Cette réduction était obser-
vée respectivement à H2 ± 3, 4 ± 5, 9 ± 8 et 12 ± 10 (p < 0,05)
pour la procaïnamide et la propafénone versus amiodarone et
placebo. Au total, les trois antiarythmiques étaient efficaces, pro-
caïnamide et propafénone étant plus rapides, et propafénone
et amiodarone étant plus actifs. (G.E. Kochiadakis, Hérak-
lion, 3878).
Outre le bénéfice sur le risque embolique, la cardioversion
rapide, échoguidée peut, en raccourcissant la durée de la fibril-
lation auriculaire et donc en diminuant le remodelage auriculaire,
améliorer le succès de la cardioversion et le maintien du rythme
sinusal. Mais l’étude ACUTE ne permet pas de répondre totale-
ment à cette question. Elle compare, chez 1 222 patients, la car-
dioversion échoguidée à la cardioversion conventionnelle. Le
succès immédiat de la cardioversion a été identique : 81 %
(344/427) à J1 (cardioversion échoguidée) versus 80 % (293/367)
à J28
(cardioversion conventionnelle).
De même, à la fin des huit semaines de l’étude, 53 % des patients
(326/619) étaient en rythme sinusal après cardioversion précoce,
contre 50 % (304/603) après cardioversion conventionnelle. Mais
comme le temps moyen de suivi après cardioversion était doublé
(54 jours, versus 28 jours), un bénéfice reste probable, la car-
dioversion précoce pouvant doubler le temps passé en rythme
sinusal.
D’autres études sont sans doute nécessaires. (R.A.M. Grimm,
Cleveland, 2782).
Le bénéfice économique d’une cardioversion précoce, échogui-
dée, raccourcissant le traitement précardioversion mais compor-
tant le coût d’une échographie œsophagienne, n’a jamais été éva-
lué. Les dossiers de 839 des 1 222 patients de l’étude ACUTE
ont pu être analysés. La durée de séjour était la même (5,2 ver-
sus 5,8 jours). Les coûts hospitaliers et les coûts totaux étaient
identiques dans les deux groupes. (A.L. Klein, Cleveland, 2787).
L’amiodarone est largement utilisée dans la cardioversion des
fibrillations auriculaires de survenue récente, mais les données
comparatives avec les autres antiarythmiques de classe I restent
fragmentaires. Deux méta-analyses sont rapportées, portant sur
une fibrillation de moins de 7 jours. La première (595 patients)
regroupait 6 études randomisées portant sur amiodarone versus
placebo ; la deuxième (632 patients) incluait 6 études comparant
amiodarone et antiarythmique de classe Ic. La réduction sponta-
née de la fibrillation récente de moins de 7 jours reste importante
(35 à 64 %). L’amiodarone ne diffère pas du placebo dans les pre-
mières heures. La différence apparaît à la 8eheure (p = 0,058), et
la supériorité est nette après 24 heures (p < 0,001). Les classes Ic
étaient supérieures à l’amiodarone (diminuant la récidive de 26 %,
risque relatif = 0,74) pendant les premières 8 heures, mais deve-
naient identiques à partir de la 24eheure (RR = 0,95, p = 0,49).
Les effets secondaires restaient rares dans les deux groupes, avec
uniquement 4 cas de flutter 1/1 pour les antiarythmiques de classe
Ic (1 %).
L’amiodarone doit donc être utilisée quand les classes Ic ne peu-
vent l’être, son effet est moins rapide dans les premières heures.
(A. Durand-Dubief, Lyon, 2134).
L’effet bénéfique du traitement bêtabloquant chez les patients en
insuffisance cardiaque est maintenant affirmé, mais la place de
ce traitement dans le sous-groupe des patients avec fibrillation
auriculaire est mal connue.
D’un ensemble de 1 094 patients randomisés entre placebo et
carvédilol, un sous-groupe de 136 patients en fibrillation auricu-
laire à l’inclusion a été analysé (84 sous carvédilol et 52 sous pla-
cebo) :
– le carvédilol améliorait la fraction d’éjection de 23 à 33 % ver-
sus 24 à 27 % sous placebo (p = 0,001) ;
– le nombre combiné d’hospitalisations ou de décès était quant à
lui diminué de 35 % (p = 0,055) ;
– une tendance à la diminution de la mortalité était présente :
4,8 % versus 12 % (p = 0,12).
Cet effet était indépendant d’une cardioversion de la FA (19 %
versus 15 %, non significatif), ou d’une bradycardie plus pro-
noncée (baisse de – 13 battements versus – 7 battements, non
significatif).
Chez les patients en fibrillation auriculaire, le traitement par
carvédilol est favorable, et cet effet est indépendant du rythme
cardiaque. (J.A. Joglar, Texas, 3253).
ABLATION DES TACHYCARDIES
L’ablation du flutter commun consiste à créer une ligne de bloc
à travers l’isthme cavotricuspidien et à vérifier le caractère bidi-
mensionnel de ce bloc par des stimulations de part et d’autre de
la ligne ainsi créée. Deux situations de pseudo-conduction sont
rapportées, grâce à des cartographies tridimensionnelles précises
(CARTO), parmi 12 patients sur 63 ablations de flutter commun :
– une conduction contournant l’isthme par la berge postérieure
de l’orifice de la veine cave inférieure (n = 3) ;
– une conduction électrique grâce à un courant bien volté sur du
La Lettre du Cardiologue - Supplément au n° 341 - janvier 2001
27
R
YTHMOLOGIE
Cardioversion Cardioversion
échoguidée conventionnelle
Nombre 619 603
Patients CV 427 367
77 % 61 %
Succès CV 344 293
81 % 80 %
Date CV médiane 1 jour 28 jours
Patients en RS 326 304
53 % 50 %
Durée de suivi 54 jours 28 jours

muscle pectiné épais (n = 9).
Aucune récidive n’était en effet obtenue chez ces 12 patients, quel
que soit l’aspect de pseudo-conduction. (H. Nagakawa, Okla-
homa, 2773).
Une activation à travers la crista terminalis peut entraîner un faux
aspect de bloc incomplet isthmique et amener à réaliser des tirs
de radiofréquence supplémentaires inutiles.
Une stimulation positionnelle, comparant l’activation atriale
basse pendant la stimulation à l’orifice du sinus coronaire à la
partie postérieure du septum interatrial et au bord septal de la
ligne d’ablation, a permis de distinguer un vrai bloc incomplet
(1/6) d’un pseudo-bloc par activation transcristale (5/6).
(F. Anselme, Rouen, 3013).
L’ablation par radiofréquence des TVidiopathiques peut être ren-
due délicate pour les TVseptales proches de la région hisienne.
Ce cas a été rencontré 9 fois sur un total de 90 ablations de TV
idiopathique droite (10 %).
Dans tous les cas, l’électrogramme ventriculaire enregistré au
niveau du His précédait le QRS en tachycardie : V-ECG = – 10
à – 35 ms, avec une topostimulation concordante au niveau du
His. Quatre fois sur 9, l’ablation n’a pu être réalisée, l’électro-
gramme hisien étant le plus précoce de tous les électrogrammes
enregistrés. Les critères ECG de surface montraient une grande
onde R en D1, un aspect QS en V1 et une diminution des ondes
R en inférieur. (Y. Yamauchi, Yokosuka, 3009).
C’est le mérite de Michel Haissaguère d’avoir démontré la pos-
sibilité d’une ablation focale curative de la fibrillation auri-
culaire en se portant sur des foyers extrasystoliques siégeant dans
une ou plusieurs veines pulmonaires. Mais avec les sondes d’abla-
tion actuelles, la technique reste très lourde (plusieurs séances
successives de 4 à 6 heures chacune).
Il est maintenant possible de réaliser une isolation électrique des
veines pulmonaires, par une lésion circonférentielle à l’aide d’un
ballonnet appliqué à l’orifice de la veine pulmonaire. C’est le
système CUVA (Atrionix) utilisant des ultrasons. Il a été évalué
chez 10 patients, âgés de 50 ± 13 ans, avec une fibrillation auri-
culaire paroxystique (8/10) de durée moyenne 8 ± 10 ans, ayant
résisté en moyenne à 3,5 médicaments antiarythmiques, et pour
3 malades à une tentative d’ablation focale. Au total, 2,4 veines
par patient ont été traitées, avec en moyenne 10 ± 9 tirs par veine,
permettant une isolation électrique chez tous les patients au cours
d’une seule séance d’ablation. Aucune récidive de fibrillation
auriculaire n’a été observée chez 5 patients, pourtant sans aucun
traitement antiarythmique. Aucune sténose pulmonaire n’a été
mise en évidence.
Il est donc possible, comme pour le flutter auriculaire commun,
d’envisager une ablation de type anatomique, et non plus élec-
trophysiologique, dirigée vers les orifices des veines pulmonaires,
réalisant une isolation électrique en cas de fibrillation auriculaire
paroxystique et rebelle. (D. Wieber, Chicago, 2153).
Une expérience similaire d’ablation par ballonnet et ultrasons a
été rapportée sur 10 patients avec FAparoxystique rebelle (échec
de 3,6 antiarythmiques). En l’absence d’activité focale, une
approche d’emblée anatomique a été tentée sur une veine (5 fois
sur 10) ou sur 2 veines (5 fois sur 10). L’ablation a été réalisée
avec en moyenne 11 ± 8 tirs par veine, pour une durée totale de
5,7 ± 1,5 heures, en une seule séance. Après un suivi de 6 mois,
seuls trois patients étaient sans aucune récidive. Probablement,
si l’ablation de type anatomique doit être développée, elle devra
être d’emblée aussi large que possible, portant sur 2 voire 4 veines
pulmonaires. (S. Ernst, Hambourg, 2353).
DÉFIBRILLATEURS IMPLANTABLES ET SEMI-AUTOMATIQUES
Indications du défibrillateur implantable
Une revascularisation s’impose quand un arrêt cardiaque par
fibrillation ventriculaire est associé à des lésions coronaires hémo-
dynamiques et accessibles. Par contre, la place du défibrillateur
au décours de la chirurgie est mal connue.
Deux cent quatorze patients ont été étudiés après arrêt cardiaque
et revascularisation coronaire. Chez 29 patients (14 %), l’explo-
ration électrophysiologique était positive et un défibrillateur a été
implanté. L’exploration était négative chez 185 patients (86 %),
qui n’étaient donc pas implantés.
Après un suivi moyen de 21 mois (6 à 36 mois), la mortalité était
de 6 % (10/185) chez les patients non inductibles versus 24 %
(7/29) chez les patients inductibles appareillés avec un DAI ; le
nombre d’événements rythmiques était respectivement de 22 %
(40/185) et de 52 % (15/29).
Les patients revascularisés après un arrêt cardiaque par fibrilla-
tion ventriculaire ne semblent donc pas nécessiter un défibril-
lateur si leurexploration électrophysiologique est négative et
si leur pronostic postopératoire est similaire à celui des patients
avec exploration positive et donc implantés après revascularisa-
tion. (A. Natale, Omaha, 3261).
La place du défibrillateur chez les patients en attente de trans-
plantation est discutée. Un groupe de 854 patients inscrits en
liste d’attente sur une période de 8 ans (janvier 1992-mars 2000)
a été analysé. Cent deux d’entre eux bénéficiaient d’un défibril-
lateur. Leur mortalité totale a été de moitié inférieure, 13,2 %
versus 25,8 % (p = 0,03), et aucune mort subite n’était observée,
contre 72 % de mort subite dans le groupe sans défibrillateur. La
recommandation concernant le défibrillateur en “bridge” pré-
transplantation mérite donc d’être précisée. (S. Sandner, Vienne,
3686).
La valeur prédictive d’une induction de fibrillation ventriculaire
reste mal connue, alors que, dans les recommandations, tout
patient avec syncope et TV ou FV induite à l’exploration néces-
site un défibrillateur.
Cent dix-huit patients consécutifs avec syncope et une cardiopa-
thie ischémique (97 hommes, âge moyen 71 ± 10 ans, FE 37 ± 13 %)
ont été étudiés par stimulation ventriculaire programmée (jusqu’à
3 extrastimulus) : 53 (45 %) ont présenté une tachycardie ven-
triculaire monomorphe et ont été exclus de l’étude, mais, chez
20 patients, une fibrillation ventriculaire (18/20 avec 3 extrasti-
mulus) était obtenue, et 45 patients n’étaient pas inductibles.
Aucun de ces 65 derniers patients n’a reçu de défibrillateur ou de
traitement antiarythmique. Pendant un suivi de 25 ± 20 mois, la
mortalité était de 93 % à 1 an et de 84 % à 2 ans, et restait iden-
tique avec ou sans fibrillation ventriculaire induite. Les deux
groupes étaient similaires au niveau de l’âge, du sexe, de la sévé-
La Lettre du Cardiologue - Supplément au n° 341 - janvier 2001
28
R
YTHMOLOGIE

rité de la cardiopathie et de la fraction d’éjection. En l’absence
de TV monomorphe induite, les patients avec syncope ont une
mortalité faible, l’induction d’une fibrillation n’a pas de valeur
pronostique et l’implantation d’un défibrillateur doit rester dis-
cutée. (S. Hao, New York, 1930).
L’efficacité et le coût du traitement des arythmies ventriculaires
malignes par le défibrillateur ont été analysés sur une cohorte de
plus de 150 000 patients MEDICARE traités pour tachycardie ou
fibrillation ventriculaire entre 1987 et 1995.
Cent cinquante-trois mille soixante patients ont été étudiés,
12 184 ont reçu un défibrillateur et 140 876 n’ont pas été implan-
tés : les patients avec défibrillateur étaient souvent plus jeunes,
de sexe masculin, de race blanche, avec une cardiopathie isché-
mique, une fraction d’éjection abaissée. Ils étaient admis pour
fibrillation plutôt que pour tachycardie ventriculaire. La morta-
lité à 1 an, 2 ans et 3 ans était respectivement de 11 % versus
24 %, 18 % versus 35 % et 22 % versus 42 %. Le risque relatif
était donc divisé par 2, de 0,39, 0,40, et 0,40 et, après ajuste-
ment, 0,43, 0,48 et 0,52. Les coûts MEDICARE (hospitaliers)
restaient plus élevés pendant la durée du suivi : à 1 an, 44 500 $
versus 11 000 $ ; à 2 ans, 49 400 $ versus 14 000 $ ; à 3 ans,
54 400 $
versus 17 000 $. Le bénéfice du défibrillateur est sem-
blable à celui observé dans les études publiées (MADIT, CIDS,
AVID, MUST), mais le surcoût de l’implantation persiste
même après 3 ans. (J. Weiss, Stanford, 1924).
L’étude AMIOVIRT a été présentée en hotline le 15 novembre.
Elle compare amiodarone et défibrillateurimplantable en cas
de TVnon soutenue chez les patients avec une cardiomyopa-
thie dilatée primitive. La place du défibrillateur a été affirmée
en post-infarctus chez des patients asymptomatiques, à haut risque
de mort subite, fraction d’éjection basse et TV non soutenue au
holter (études MADIT et MUST) : indication de classe I quand
la stimulation ventriculaire programmée est positive, mais, en cas
de cardiomyopathie dilatée, la place du défibrillateur n’est pas
connue.
Cent trois patients ont été randomisés, auxquels se sont ajoutés
75 patients d’un registre de suivi : fraction d’éjection < 0,35 %,
tachycardie ventriculaire asymptomatique comportant 3 batte-
ments ou plus et de moins de 30 secondes. L’amiodarone était
prescrite après une dose de charge d’un mois, à la dose de 300 mg
par jour. L’étude a été arrêtée après un suivi de 20 mois en moyenne
pour “futilité” (p = 0,6), car aucune différence significative dans
la mortalité n’apparaissait, avec, à 3 ans, 85 % des patients sous
amiodarone et 79 % avec défibrillateur (8 décès sous amiodarone
et 13 décès sous défibrillateur). Par contre, l’amiodarone suppri-
mait les épisodes de tachycardies symptomatiques (p = 0,002). Il
n’est donc pas possible d’étendre aux cardiomyopathies les recom-
mandations établies pour les infarctus chroniques, mais la stimu-
lation programmée n’était pas réalisée dans cette étude, à la dif-
férence des recommandations pour les patients avec TV non
soutenues asymptomatiques en post-infarctus.
La stimulation ventriculaire (resynchronisation ventriculaire) est
actuellement évaluée dans le traitement de certaines insuffisances
cardiaques congestives, comportant notamment un gros trouble
d’activation ventriculaire. Mais un rôle délétère éventuel sur les
arythmies ventriculaires a pu être évoqué et faire discuter la néces-
sité du défibrillateur triple chambre.
Une étude a porté sur 18 patients implantés d’un défibrillateur
triple chambre (Insynch ICD) et sur un groupe témoin de
29 patients, porteurs d’un simple DAI, et présentant un bloc de
branche gauche (BBG) > avec une largeur de QRS > 130 ms et
une fraction d’éjection < 35 %, groupe apparié selon l’âge, la car-
diopathie, la fraction d’éjection, la classe NYHAet le traitement.
Dans le groupe bénéficiant d’une resynchronisation (QRS dimi-
nuant de 180 ± 28 ms à 160 ±27 ms), une amélioration (p < 0,05)
de la NYHA(2,8 ± 0,5 à 2,1 ± 0,5) et du diamètre diastolique du
ventricule gauche (65 ± 12 mm à 60 ± 11 mm) était notée. Par
contre, aucune différence sur les événements rythmiques (TV,
FV) survenant après l’implantation n’était retrouvée. La mor-
talité n’était pas différente (3 décès sur 29 dans le groupe témoin
et 0 sur 28 dans le groupe resynchronisé). (V. Kuehlkamp, Tue-
bingen, 3675).
Les holters ECG de 24 heures chez 21 patients implantés d’un
stimulateur triple chambre ont été analysés après 3 mois de trai-
tement croisé en 2 périodes : resynchronisation ventriculaire/pas
de resynchronisation.
Le nombre total d’ESV est diminué à 1 051 ± 1 309 ESV par
24 heures versus 2 709 ± 2 560 (p = 0,0001), comme le nombre de
salves ventriculaires (> 3 ESV) : 5 ± 13 versus 55 ±120 (p = 0,007),
avec une tendance à la baisse des TV soutenues (> 30 s) : 1 ver-
sus
3.
Il n’y avait donc pas d’argument pour un rôle rythmique délé-
tère de la resynchronisation. (S. Walker, Londres, 3348).
Le défibrillateur auriculaire implantable permet actuellement
l’autodéfibrillation auriculaire, à l’aide d’un boîtier activateur
déclenché par le patient lui-même, s’il est démontré que la tolé-
rance et le bénéfice du choc le permettent. Un tel boîtier (JEWEL
AF, Medtronic 7250) a été évalué chez 144 patients avec des
tachycardies atriales résistantes, dont 56 ont activé le boîtier d’au-
todéfibrillation : 1 fois pour 18 patients, 2 à 5 fois pour 24 patients,
et plus de 5 fois pour 14 patients, pour un total de 366 épisodes
sur un suivi de 9 mois. Les chocs, en moyenne de 16 ± 8 joules,
ont été efficaces 337 fois (92 %), un seul choc a suffi 313 fois
(86 %), mais une récidive précoce était observée 37 fois (11 %).
La sécurité paraît très bonne (aucune arythmie ventriculaire n’a
été observée et, de toute façon, une sonde de défibrillation ven-
triculaire est associée), la douleur a été acceptable pour la majo-
rité des patients, mais la récidive immédiate est probablement
une limite de la technique (11 % des tentatives). (D. Schwartz-
man, Pittsburgh, 2335).
L’accès du public à la pratique de la défibrillation cardiaque en
urgence, grâce à la généralisation des défibrillateurs semi-auto-
matiques, est un des thèmes de plus en plus d’actualité. L’expé-
rience des deux aéroports de Chicago a été rapportée : O’Hare et
Midway, avec 80 millions et 20 millions de voyageurs par an res-
pectivement. En juin 1999, 51 défibrillateurs externes semi-auto-
matiques ont été installés, bien visibles, très accessibles, et
2 500 employés des aéroports ont été formés à leur utilisation.
En 10 mois, 14 cas de morts subites étaient observés, 12 en rap-
port avec des fibrillations ventriculaires, et 9 ont pu être récupé-
rés, sans aucune séquelle neurologique : survie totale 64 %, dont
survie post-fibrillation ventriculaire 75 %, très supérieure
La Lettre du Cardiologue - Supplément au n° 341 - janvier 2001
29
R
YTHMOLOGIE

aux taux usuels de survie (5 à 10 %).
Sur les 14 épisodes, 5 des employés préalablement formés sont
intervenus, mais également 9 voyageurs qui n’avaient pas béné-
ficié du programme HEARTSAVE. La généralisation de ces
expériences doit rester prudente, mais ces résultats sont très pro-
metteurs. (P. Willoughby, Chicago, 3990).
AFFECTIONS GÉNÉTIQUES RESPONSABLES DE MORT SUBITE
Syndrome du QT long
L’épreuve d’effort est classiquement utilisée dans le diagnostic
du syndrome du QT long, non pour déclencher des arythmies ven-
triculaires et des torsades de pointe, mais simplement pour majo-
rer l’aspect du QT long, car le QT ne se raccourcit pas et ne
s’adapte pas à l’accélération de la fréquence cardiaque résultant
de l’effort.
L’équipe de G. Vincent a montré que cette réponse à l’effort
n’était pas univoque mais dépendait du type de mutation res-
ponsable.
Certes, le SQTL 1 (chromosome 11, canal IKs, gène KVLQT1),
le plus fréquent, montre une augmentation du QTC à l’effort.
Mais en cas de LQT2, le QTC ne se modifie pas franchement
(chromosome 7, canal IKr, gène HERG) et se raccourcit même
dans les rares cas de LQT3 (chromosome 3, canal sodique, gène
SCN5A). (G. Vincent, Salt Lake City, 2830).
Dans les familles de sujets à syncopes en relation avec un syn-
drome du QT long, des sujets asymptomatiques mais présentant
la mutation chromosomique sont fréquemment diagnostiqués. Un
traitement bêtabloquant est actuellement recommandé chez ces
sujets dits à risque, en l’absence de données pronostiques plus
précises : sont-ils des porteurs sains ou vont-ils un jour présen-
ter une syncope, voire une mort subite ?
Dans un groupe de 58 sujets, porteurs asymptomatiques, d’âge
moyen 38 ± 18 ans, avec 40 % d’hommes :
– 18 (31 %) avaient un ECG de repos normal avec un QTC
< 440 ms pour les hommes, < 460 ms pour les femmes ;
– la survenue de syncopes n’a concerné, au cours du suivi, que
22 % (13/58) des sujets ;
– mais les syncopes ont été aussi fréquentes chez les sujets à
ECG normal : 3/18 (18 %) ;
– l’analyse dynamique de l’ECG améliore le dépistage, la sensi-
bilité passant de 69 % avec l’ECG de repos à 76 % avec l’ECG
combiné au holter (QT long lors des fréquences lentes), à 84 %
pour l’ECG de repos associé à l’ECG d’effort (inadaptation à l’ef-
fort) et à 95 % pour l’ECG couplé à un test d’hyperventilation
d’une minute.
G. Lande a étudié, chez ces mêmes sujets porteurs asympto-
matiques, la dynamique de QT (pente QT/RR) sur le holter de
24 heures :
– la pente de nuit est plus abrupte que la pente de jour (0,20 ±
0,04 versus 0,15 ± 0,03) chez 13 des 14 patients, alors que l’in-
verse est observé chez 12 des 14 sujets témoins (0,17 ± 0,03
versus 0,13 ± 0,03) : sensibilité de 93 % ;
– le QTC de nuit est plus long chez les sujets témoins (différence
de 17 ± 11 s) alors que, chez les patients, cette différence est
faible, voire inverse (6 ± 13 ms) ; pour une valeur seuil de 10 ms
(QTC de nuit – QTC jour), la sensibilité n’est que de 64 % ;
– un ECG de repos normal n’élimine donc pas un syndrome du
QT long dans les familles génétiquement atteintes (LQT1, le plus
fréquent) et la normalisation du QT chez l’adulte de sexe mas-
culin a même été observée chez certains sujets par G. Lande.
(G. Lande, Nantes, 2831 et A. Moretti, Pavie, 2832).
Syndrome de Brugada
L’incidence et le pronostic d’un aspect ECG de Brugada chez
les sujets asymptomatiques sont discutés. Trois études de popu-
lations ont été présentées.
Trente-deux mille six cent quarante et un ECG ont été analysés
en aveugle, de façon prospective, sur un an, par 5 électrophysio-
logistes et confirmés par une deuxième lecture indépendante en
cas d’anomalies.
Six ECG avec bloc de branche droit (BBD) et élévation de ST en
V1 V2 ont été mis en évidence, 2 fois dans un contexte aigu : une
hémorragie intracrânienne par rupture d’anévrysme mortelle et
une intoxication volontaire en tricyclique, avec un ECG norma-
lisé en 48 heures. Au contraire, 4 des patients étaient asympto-
matiques, sans antécédents familiaux, avec une échographie car-
diaque normale ; 1 fois sur 4 seulement la stimulation ventriculaire
était positive (TV polymorphe avec 2 extrastimulus ventricu-
laires) et les anomalies ECG étaient majorées par la procaïna-
mide. Les 5 sujets survivants sont restés asymptomatiques sur un
suivi bref de 8 mois ± 5. (G. Michaud, Ann Arbor, 2833).
Les ECG réalisés entre 1996 et 1997 chez 34 520 sujets d’âge
moyen 60 ± 14 ans (12 560 hommes et 21 960 femmes) ont été
analysés et un aspect du syndrome de Brugada a été retrouvé chez
140 d’entre eux, 110 hommes (0,9 %) et 30 femmes (0,14 %) :
– bloc droit incomplet ou complet RSr’71 %,
– aspect ST en dôme 61 %,
– aspect ST en selle 39 %.
Aucun de ces sujets ne présentait de syncope ou d’arrêt circula-
toire dans ses antécédents. (K. Fujimori, Sendai, 3268).
Une étude identique a été rapportée portant sur 13 929 sujets d’âge
moyen 58 ±10 ans, dont 27 % d’hommes. L’aspect ECG de Bru-
gada était retrouvé chez 0,7 % des sujets (dont 86 % d’hommes) :
la prévalence chez les hommes était de 2,1 %.
Après un suivi de 2,6 ans, un décès sur 98 sujets avec ECG posi-
tif était rapporté (1 %), versus 139 décès chez les sujets avec ECG
négatif (1 %) : perdus de vue 2 % en cas d’ECG négatif et 2,7 %
en cas d’ECG positif.
Au Japon, la prévalence de cet aspect ECG est non négligeable
(0,1 % chez les femmes, 1 à 2 % chez les hommes) dans la
population, mais ne semble pas comporter de risque particulier
chez les sujets asymptomatiques. (Y. Miyasaka, Osaka, 3269).
Classiquement, le syndrome ECG de Brugada comporte un haut
risque de mort subite, même chez les sujets asymptomatiques, et
une attitude agressive (DAI) est recommandée.
Un groupe de 60 patients (45 hommes, âge moyen 40 ± 15 ans)
a été évalué sur un suivi moyen de 33 mois. Trente patients étaient
symptomatiques (arrêt cardiaque ou syncope) et 30 asymptoma-
tiques.
La survenue d’une fibrillation ventriculaire n’a concerné que les
La Lettre du Cardiologue - Supplément au n° 341 - janvier 2001
30
R
YTHMOLOGIE
 6
6
1
/
6
100%