Les cancers urologiques à l’ESMO 2012 DOSSIER THÉMATIQUE

La Lettre du Cancérologue • Vol. XXI - n° 9 - novembre 2012 | 461
DOSSIER THÉMATIQUE
Compte-rendu et analyse
de l’ESMO 2012
Les cancers urologiques
à l’ESMO 2012
Urological cancers at the ESMO Congress 2012
P. Beuzeboc*
* Institut Curie, Paris.
Cancers de la prostate
Comment réinventer le traitement
médical du cancer de la prostate
métastatique résistant à la castration ?
◆P.W. Kantoff a fait le point
sur les immunothérapies. Il a notamment
rappelé...
➤Les données de l’essai de phase III IMPACT 3 (1)
montrant un bénéfi ce en survie globale (SG) de
4,1 mois (HR = 0,579) mais également un délai
jusqu’à apparition des douleurs en faveur du sipu-
leucel T. Mais qui pourra en bénéfi cier ? Il n’existe ni
facteurs prédictifs ni critères d’effi cacité. Les patients
pour lesquels ce traitement est le plus approprié
sont-ils ceux qui sont traités très précocement au
stade métastatique asymptomatique, et qui sont
lentement évolutifs ?
➤
Le développement de PROSTVAC
®
-VF/
TRICOM™, avec une étude de phase III (étude
GLOBAL, 1 200 patients prévus) en cours d’activa-
tion après les données de l’étude de phase II rando-
misée (2) retrouvant un bénéfi ce en SG mais pas en
survie sans progression (SSP). Cette étude devrait
commencer en France en 2013.
➤
Les données concernant l’ipilimumab avec
2 études de phase III en cours qui ont la SG comme
critère de jugement.
La prochaine étape pourrait être l’utilisation des anti-
corps immunoconjugués (ciblant PMSA et SLC44A4)
ou de combinaisons thérapeutiques.
◆O. Sartor a essayé de montrer la place
de la chimiothérapie, dans une situation où tout
change très vite. Actuellement, les décisions sont
prises en fonction du docétaxel (avant ou après
docétaxel), mais elles pourraient l’être après
l’acétate d’abiratérone ou après l’enzalutamide
(MDV3100) demain
L’acétate d’abiratérone devant rapidement se posi-
tionner en traitement prédocétaxel, de nouvelles
questions se posent :
➤Quels sont les mécanismes potentiels de résis-
tance ?
➤
Existe-t-il un degré élevé de résistance croisée
pour les traitements ciblant l’axe du récepteur aux
androgènes (RA) ?
➤Quelles sont les activités de la chimiothérapie,
et en particulier des taxanes, après un traitement
par acétate d’abiratérone ?
Les premières données sont assez contradictoires.
Récemment, l’équipe du Royal Marsden (Royaume-
Uni) [3] a rapporté des taux de réponse biologique
plus faibles qu’attendu avec le docétaxel après
acétate d’abiratérone (26 %, avec une médiane de
délai avant progression de 4,6 mois) dans une série
limitée.
En revanche, une expérience multicentrique fran-
çaise (Albiges L et al., abstr. 951) a retrouvé un taux
de réponse de 56 % (18 patients sur 32) avec le
cabazitaxel après docétaxel et acétate d’abiraté-
rone.
Lors de la résistance à l’inhibition de CYP17, plusieurs
mécanismes peuvent s’intriquer : induction de la
stéroïdogenèse et variants d’épissage du RA avec
une activation du RA ligand-indépendante (Mosta-
gher EA et Montgomery B, Clin Cancer Res 2011) ?
Il a été montré que l’expression de ces variants
d’épissage dans les cancers de la prostate résistant
à la castration (CPRCm) était associée à une courte
survie (Hörnberg E, PloS One 2011).

462 | La Lettre du Cancérologue • Vol. XXI - n° 9 - novembre 2012
Résumé
Cette année, le congrès de l’ESMO (European Society for Medical Oncology) a été marqué, en ce qui
concerne l’urologie, non seulement par de très bonnes mises au point et actualisations mais aussi par les
résultats de l’étude de phase III GETUG 15 dans les formes métastatiques hormonosensibles ainsi que par
ceux du docétaxel associé au lénalidomide dans les cancers de la prostate métastatiques et résistants.
Les données des études contrôlées COMPARZ, INTORACT, RECORD-2, INTORSECT et AXIS (survie globale)
ont été rapportées dans les cancers du rein métastatiques. Celles des études de phase II concernant le
sunitinib (SUPAP) et l’évérolimus (RAPTOR) en première ligne des cancers papillaires métastatiques ont
fait l’objet de présentations françaises, de même que l’étude de phase II randomisée évaluant la place du
trastuzumab en association avec une chimiothérapie dans les tumeurs urothéliales métastatiques avancées
ou métastatiques.
Mots-clés
Cancer delaprostate
Cancer durein
métastatique
Cancer papillaire
Cancer delavessie
Cancer du testicule
Summary
In the fi eld of urological tumors,
the ESMO2012 meeting
has been marked by well-
done “states of the art” and
actualizations but also by the
results of phaseIII trials such
as GETUG15 and the doce-
taxel plus lenalidomide study
in metastatic prostate cancer.
For kidney cancer, the results
of the randomized COMPARZ,
INTORACT, RECORD-2,
INTORSECT and AXIS (overall
survival) studies have been
reported. French oral presen-
tations have concerned the
data of phase II trials evalua-
ting the potential benefit of
sunitinib and everolimus in
papillary kidney cancer (SUPAP
and RAPTOR studies) as well as
those of a randomized phaseII
trial evaluating the interest of
trastuzumab combined with
chemotherapy in HER2 posi-
tive advanced bladdder tumors.
Keywords
Prostate cancer
Metastatic kidney cancer
Papillary cancer
Bladder cancer
Testicular cancer
Deux autres questions importantes se posent :
➤
Le cabazitaxel est-il plus effi cace que le docétaxel ?
➤
La dose optimale est-elle de 25 ou de 20 mg/m
2
?
Deux études de phase III (FIRSTANA et PROSELICA),
en cours, permettront d’y répondre.
◆J.S. de Bono, dans un exercice de style
diffi cile, a essayé de voir comment intégrer
les nouvelles molécules : traitements séquentiels
ou concomitants ?
➤
Toutes ont été développées essentiellement en
monothérapie. J.S. de Bono a insisté sur l’importance
de comprendre les mécanismes de résistance entre
docétaxel, acétate d’abiratérone et enzalutamide
ainsi que de développer des biomarqueurs pour guider
les thérapeutiques et des stratégies et des combi-
naisons de traitement pour essayer de prévenir ou
reverser l’émergence d’une résistance. Il faudra maxi-
maliser la durée du contrôle tumoral en minimisant
l’exposition à des traitements ineffi caces et onéreux.
➤
L’association enzalutamide-acétate d’abiraté-
rone présente-t-elle un intérêt ?
Dans un proche avenir vont débuter des essais de
ciblage concomitant du RA et de l’axe PI3K/AKT/
mTOR par l’acétate d’abiratérone et des inhibiteurs
spécifi ques.
➤
De nombreuses molécules sont en développe-
ment (fi gure 1).
Les études précliniques devraient jouer un rôle
important pour défi nir les meilleures combinai-
sons en association ou en traitements séquentiels
à évaluer en clinique.
◆C. Parker s’est concentré sur le ciblage de l’os :
comment allons-nous utiliser
les bisphosphonates, le dénosumab,
le radium 223 ? Dans quel but ?
Est-ce pour améliorer la SG, augmenter la qualité
de vie, retarder les symptômes et les complications
osseuses (Skeletal Related Events [SRE]), retarder les
métastases osseuses ?
L’acide zolédronique et le dénosumab améliorent la
qualité de vie, diminuent et retardent les événements
indésirables sévères mais n’améliorent pas la SG, au
contraire du radium 223.
◆Impact des nouvelles hormonothérapies
sur les douleurs et la qualité de vie :
2 présentations en session orale
➤
L’acétate d’abiratérone a un réel impact sur la
douleur et l’état fonctionnel des patients présen-
tant un CPRCm en préchimiothérapie (Basch E et al.,
abstr. 8950).
➤
De même, l’enzalutamide retarde le temps
jusqu’au premier événement osseux (SRE) et la
survenue des douleurs dans l’essai AFFIRM, comme
l’ont bien montré K. Fizazi et al. (abstr. 8960).
◆Autres présentations orales
➤
Le lénalidomide combiné à l’association docé-
taxel/prednisone classique n’apporte pas de béné-
fi ce par rapport au docétaxel/prednisone selon
une large étude de phase III (Petrylak D et al.,
abstr. LBA24)
Figure 1. Nombreux agents en cours de développement.
• Nouveaux antagonistes du récepteur
aux androgènes : LBD* versus aminoterminal
• Agents régulant négativement les récepteurs aux androgènes :
anti-sens RA (shRNA)
• SARD (dégradant les récepteurs
aux androgènes) : ciblant LBD*
• Inhibiteurs sélectifs non stéroïdiens
de la 17,20-lyase
• Inhibiteurs des Hsp
(Heat shock protein)
:
Hsp90, Hsp27, clustérine
• Inhibiteurs de HDAC : HDAC6/Hsp90 sélectivement
• Inhibiteurs de PI3K/AKT/mTOR :
GDC 0941, etc.
• Inhibiteurs de RAF/MEK
• Inhibiteurs multikinases : cabozantinib
• Inhibiteur de SARC : dasatinib
• Immunoconjugués
• Inhibiteurs de PARP
• Inhibiteurs d’IGF-1R
• Antagonistes des gènes ETS
* LBD : ligand binding domain.

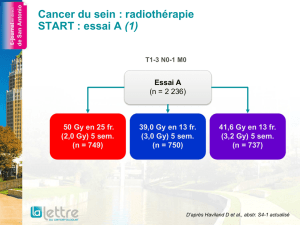
Figure 2. GETUG/AFU 15 : survie globale.
60
20
0
03612 24
Mois après randomisation
Survie globale (%)
48 60 72
80
100
40
Médiane de suivi : 50 mois ; IC95 : 49-54
ADT + docétaxel : médiane 58,87 mois ; IC95 : 50,79-69,09
ADT : médiane 54,24 mois ; IC95 : 42,22-NR
HR = 1,01 ; IC95 : 0,75-1,36 ; p = 0,9549
Patients à risque (n)
193 171 148 102 60 25
192 175 145 97 64 31
Alors que l’association de docétaxel à la privation hormonale (ADT + T) montre une amélioration de la SSP
biologique, avec une médiane de 22,93 mois (19,55-28,39) versus 12,91 mois (11,93-17,71) pour l’hormono-
thérapie seule (HR = 0,72 ; IC95 : 0,57-0,91 ; p = 0,0052), il n’y a pas de diff érence signifi cative en SG.
La Lettre du Cancérologue • Vol. XXI - n° 9 - novembre 2012 | 463
DOSSIER THÉMATIQUE
Il s’agit de la huitième étude de phase III négative
avec le docétaxel (après l’oblimersen, le GVAX,
l’atrasentan, le zibotentan, le bévacizumab, le VEGF
trap, le calcitriol à fortes doses). Décidément, le
principe des associations avec la chimiothérapie est
très décevant. Attendons encore les résultats avec
le dasatinib, l’ipilimumab et l’OGX-010.
➤
Les résultats négatifs de l’essai GETUG/AFU 15
(Gravis G et al., abstr. 893O) [fi gure 2]
Il s’agit de la première étude de phase III compa-
rant une privation androgénique (ADT) avec ou
sans docétaxel chez des patients métastatiques
hormono sensibles.
➤Il faut également relever les données concer-
nant les facteurs prédictifs
–
Association entre la progression selon les
critères du PCWG2 (Prostate Cancer Working
Group 2) et la SG dans les CPRCm (Sonvpade G
et al., abstr. 901PD) et, plus particulièrement, avec
la rPFS (radiographic progression-free survival) selon
ces critères dans l’étude COU-AA-302 évaluant l’acé-
tate d’abiratérone avant traitement par docétaxel
(Ryan C et al., abstr. 894O).
–
Association entre l’utilisation d’un cortico-
stéroïde à l’inclusion dans l’étude AFFIRM et la
survie. Les traitements prolongés par corticoïdes
sont-ils délétères ? C’est ce que laisse penser l’ana-
lyse multivariée des données de l’étude de phase III
AFFIRM (Scher H et al., abstr. 899PD) comparant
enzalutamide et placebo après docétaxel. Pour les
30 % des patients qui étaient sous cortico stéroïde
à l’entrée, la médiane de SG était de 11 mois
(IC
95
: 10-13) ; elle n’était pas atteinte pour les autres.
Cela doit faire réfl échir sur l’utilisation d’une cortico-
thérapie à long terme dans les CPRCm.
➤
Parmi les nouvelles molécules en développement...
–
J.S. de Bono et al. (abstr. 897O) ont présenté les
résultats déjà rapportés au congrès américain en
oncologie clinique du cabozantinib (ciblant à la
fois MET et VEGFR2 [Vascular Endothelial Growth
Factor Receptor 2]) à la dose de 40 mg/j (au lieu
de 100 mg/j).
Dans les 2 études de phase III COMET-1 et COMET-2
qui vont être activées l’année prochaine, la dose
choisie sera de 60 mg/j, avec des possibilités de
diminution à 40 mg/j.
–
Concernant les nouvelles hormono thérapies,
les premiers résultats de l’ODM-201 sont encou-
rageants, dans l’essai de phase I/II ARADES
(Massard C et al., LBA25_PR).
–
Les données de l’étude de phase II randomisée
(Chi K et al., abstr. 900PD) évaluant l’OGX-427
avaient également été rapportées au congrès améri-
cain en oncologie clinique. L’OGX-427 est un anti-
sens phosphorothioate de seconde génération qui
inhibe l’expression d’Hsp27 (Heat shock protein 27).
Les résultats très préliminaires de cette étude rando-
misée (1:1) testant l’OGX-427 (600 mg × 3 en dose
de charge i.v. puis 1 000 mg/sem. i.v. × 36 semaines +
prednisone 5 mg × 2/j versus prednisone aux mêmes
doses avec possibilité de crossover à la progression)
montrent des réponses biologiques (13 patients
sur 22, soit 59 %) et cliniques prometteuses. À suivre.
Cancers du rein métastatiques
Traitement de première ligne
◆Étude COMPARZ, randomisée (1:1), de phase III
et de non-infériorité comparant pazopanib
(800 mg/j ; n = 557) et sunitinib (50 mg/j ;
n = 553) [Motzer R et al., LBA8_PR]
Cette étude présentée en session orale plénière
permet de conclure à une efficacité comparable des

Figure 3. RECORD-2 : survie globale.
60
20
0
091836
Mois
Probabilité d’événement (%)
30 332712 2115 24 36
80
100
40
Évérolimus + bévacizumab (n/N = 74/182)
Interféron α + bévacizumab (n/N = 83/183)
Médianes selon Kaplan-Meier
Évérolimus + bévacizumab : NA
Interféron α + bévacizumab : 25,86 mois
Patients à risque (n)
182 173 158 149 128 108 82 57 40 19 7 1 0
183 170 161 149 135 119 92 67 43 23 11 4 0
464 | La Lettre du Cancérologue • Vol. XXI - n° 9 - novembre 2012
Les cancers urologiques àl’ESMO 2012
DOSSIER THÉMATIQUE
Compte-rendu et analyse
de l’ESMO 2012
2 molécules, avec des taux de réponse (31 versus
25 %) et des médianes de SSP (10,5 versus
10,2 mois) et de SG (28,4 versus 29,3 mois à
l’analyse intermédiaire) comparables. Les pour-
centages de SSP à 48 semaines évaluée par une
revue indépendante sont respectivement de 39,6
et 43,3 % (HR = 1,047 ; IC95 : 0,898-1,220). Il a été
constaté moins de cas de fatigue, de mucites et de
syndromes mains-pieds et une meilleure qualité
de vie avec le pazopanib, mais plus de perturba-
tions hépatiques. Des réductions de doses ont été
nécessaires dans 44 % des cas avec le pazopanib,
et dans 51 % avec le sunitinib.
◆Deux études randomisées négatives évaluant
des combinaisons antiangiogénique + anti-mTOR
ont été présentées en session orale
➤
La première étude, INTORACT, de phase IIIb
(791 patients inclus) compare temsirolimus + béva-
cizumab à interféron α + bévacizumab (Rini B et al.,
LBA21_PR).
➤La deuxième, RECORD-2, de phase II (n = 365),
compare évérolimus + bévacizumab à interféron α +
bévacizumab (Ravaud A et al., abstr. 783O) [fi gure 3].
Après ces essais négatifs, auxquels il faut ajouter
l’essai français TORAVA (4), on peut conclure que
le traitement séquentiel reste la référence et que
les combinaisons demeurent au stade des investi-
gations. Sont à suivre, néanmoins, les associations
avec les inhibiteurs de PD-1 (Programmed cell Death
protein 1).
Traitement de deuxième ligne (tableau I)
◆Présentée en session orale, l’étude
INTORSECT, de phase III, est positive :
elle montre un avantage en SG en faveur
du sorafénib (400 mg × 2/j ; n = 253) comparé
au temsirolimus (25 mg/sem. i.v. ; n = 256)
[Hutson T et al., LBA22_PR]
Alors que le temsirolimus avait montré son effi -
cacité en première ligne dans les formes à mauvais
pronostic, son intérêt en deuxième ligne restait à
évaluer. Le sorafénib, au moment du développement
de l’étude, était un comparateur acceptable. Le but
était une amélioration de la SSP de 33 % : le résultat
a été contraire, une amélioration signifi cative de
la SG avec le sorafénib étant constatée (médiane :
12,27 versus 16,64 mois ; HR = 1,31 ; IC95 : 1,05-1,63 ;
p = 0,014).
◆Données en SG de l’étude de phase III AXIS
comparant axitinib et sorafénib (Motzer R et al.,
abstr. 793PD)
L’axitinib avait montré un avantage en termes de SSP.
Les résultats de SG ne montrent pas de différences
avec, respectivement, des médianes à 20,1 mois
(IC95 :16,7-23,4) pour l’axitinib et à 19,2 mois (IC95 :
17,5-22,3) pour le sorafénib.
Ces résultats posent clairement la question de savoir
si la SSP est un bon “surrogate marker” de la SG en
deuxième ligne.
Lignes ultérieures
D. McDermott et al. (abstr. 784O) ont présenté les
résultats préliminaires d’une cohorte de 34 cas de
cancer du rein inclus dans une étude d’activité et
de tolérance évaluant l’anti-PD-1 BMS-936558,
avec quelques réponses durables aux 2 doses de
1 mg/kg et 10 mg/kg.
Tableau I. Comparatif des essais avec sorafénib comme comparateur en deuxième ligne.
Essai/agent Survie sans progression (mois) Survie globale (mois)
INTORSECT
Temsirolimus versus sorafénib 4,8 versus 3,91 12,27 versus 16,64
AXIS
Axitinib versus sorafénib 4,8 versus 3,4 15,27 versus 16,5

La Lettre du Cancérologue • Vol. XXI - n° 9 - novembre 2012 | 465
DOSSIER THÉMATIQUE
Qualité de vie et tolérance
◆ Dans l’étude PISCES, la qualité de vie, de préfé-
rence en double aveugle avec crossover, paraît meil-
leure avec le pazopanib qu’avec le sunitinib (Cella D
et al., abstr. 792PD).
◆ Comparaison de la tolérance du tivozanib et du
sorafénib dans une étude de phase III ayant inclus
517 patients (Eisen T et al., abstr. 795PD). Les arrêts
de traitement dus à des événements indésirables liés
au traitement ont été de 4,2 % pour le tivozanib et
5,4 % pour le sorafénib ; les réductions de dose ont
été de 11,6 et 42,8 %, respectivement.
Il convient de noter que des toxicités de bas grade
de longue durée sont souvent pires qu’une toxicité
de haut grade courte (tableau II).
Cancers papillaires
◆ A. Ravaud et al. (abstr. 797PD) ont rapporté les
résultats de l’étude de phase II SUPAP du GETUG
(Groupe d'étude des tumeurs urogénitales) et
du GEP (Group of Early Phase trials) évaluant le
sunitinib en première ligne dans les tumeurs papil-
laires de type I et II. L’âge moyen était de 64 ans.
Selon les critères du Memorial Sloan-Kettering
Cancer Center (États-Unis), le pronostic était favo-
rable pour 22 % des patients, intermédiaire pour
61 % et mauvais pour 17 % (et indéterminé pour
7 patients). Le taux de réponse a été de 12 %, la SSP
de 5,6 mois (5,1-7,4), la SG de 12,5 mois (8,2-17,8).
◆ B. Escudier et al. (abstr. 798PD) ont présenté les
résultats de l’étude de phase II RAPTOR évaluant
l’évérolimus en première ligne, montrant une SSP
de 7,3 mois (5-12).
◆ L’essai de phase II randomisé ASPEN va comparer,
en première ligne, dans les cancers papillaires,
sunitinib et évérolimus ; le critère de jugement
principal sera la SSP.
◆ L’avenir se tourne aussi vers de nouvelles molécules
comme le forétinib (anti-MET/VEGFR2). T.K. Choueiri,
en 2011, avait rapporté 70 % de bénéfi ce clinique.
Cancers de la vessie
◆ Les nouvelles technologies génomiques ont
transformé la recherche sur le cancer. Si le cancer
de la vessie constitue une cible attractive pour la
découverte de biomarqueurs et la recherche trans-
lationnelle du fait de l’accès facile à du tissu de
résection, il n’y a malheureusement pas de nouvelles
cibles validées, ni de biomarqueurs prédictifs en
situation métastatique. Aucune altération simple
“druggable” ne caractérise la majorité des tumeurs,
qui le sont, en revanche, par une fréquence faible
d’altérations sur des gènes multiples. Il est donc
diffi cile de conduire des essais pour démontrer une
effi cacité clinique et faire la preuve de concept de
l’intérêt d’un ciblage spécifi que. Néanmoins, parmi
les cibles potentielles, il faut noter HER2, PIK3CA/
mTOR/PTEN/AKT, CDK4/CCND1, FGFR3 et BRAF.
L’incidence de l’amplifi cation de HER2 est de 6 à 11 %.
◆ S. Oudard (abstr. 786O) a présenté les résul-
tats d’une étude française de phase II randomisée,
interrompue prématurément pour des problèmes
de recrutement, comparant en première ligne,
dans les cancers urothéliaux avancés ou méta-
statiques HER2+, une chimiothérapie par gemci-
tabine/sel de platine avec ou sans trastuzumab.
Il aura fallu tester 563 tumeurs pour en trouver
61 HER2+ (FISH+ ou IHC3+) et randomiser 61 patients.
Les SSP ont été de 8,3 mois (4,7-10,6) avec le
trastu zumab versus 10,5 mois (4,3-10,4) sans. Les
médianes de SG ont été respectivement de 15,7 mois
et 14,2 mois. Relevons que le sous-groupe traité par
cisplatine + gemcitabine + trastuzumab présente une
médiane de SG de 33,1 mois (tableau III).
◆ En deuxième ligne, G. Sonpavde et al.
(abstr. 787O) ont validé la SSP à 6 mois comme
facteur prédictif de la SG à 12 mois.
◆ C. Booth et al. (abstr. 788O) ont rapporté des
données canadiennes à partir d’un registre du
cancer de l’Ontario concernant les traitements
adjuvants (ACT) et néo-adjuvants (NACT) réalisés
entre 1994 et 2008 dans une cohorte de 2 738 cas
Tableau II. Comparaison des tolérances du tivozanib et du sorafénib.
Tivozanib (n = 259) Sorafénib (n = 257)
Tout événement indésirable
sévère lié au traitement
68 83
Hypertension (%) 42 31
Dysphonie (%) 18 4
Diarrhée (%) 18 28
Syndrome mains-pieds (%) 13 53
 6
6
1
/
6
100%