Cancers urologiques Urological cancers Cancers de la prostate P. Beuzeboc*

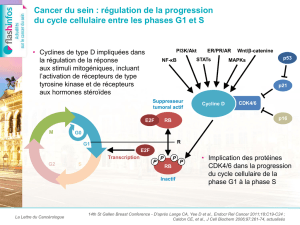
Figure 1. CA184-043 : schéma de l’étude.
Traitement jusqu’à progression ou toxicité intolérableStratifi cation : site investigateur,
phosphatase alkaline, hémoglobine,
ECOG PS • Objectif principal : SG
• Objectifs secondaires : SSP, tolérance
• Objectif exploratoire : taux de réponse PSA
RT
des
métastases
osseuses
par dose
unique
de 8 Gy
(n = 399)
Ipilimumab 10 mg/kg
Semaines 1, 4, 7, 10 Ipilimumab 10 mg/kg
Toutes les 12 semaines
(n = 400)
Placebo
Semaines 1, 4, 7, 10 Placebo
Toutes les 12 semaines
• Post-docétaxel
• CRPC
(n = 799)
1:1
R
454 | La Lettre du Cancérologue • Vol. XXII - n° 11 - décembre 2013
Cancers urologiques
Urological cancers
P. Beuzeboc*
* Institut Curie, Paris.
Cancers de la prostate
Immunothérapie par ipilimumab
Essai de phase IIII CA184-043, randomisé,
multicentrique, en double aveugle comparant la
survie globale des patients présentant un cancer de
la prostate métastatique résistant à la castration
symptomatique après docétaxel et traités par
ipilimumab ou placebo après une radiothérapie
D’après Gerritsen WR et al., abstr. 2850
L’ipilimumab bloque la signalisation négative de
CTLA-4. Une étude de phase I/II avait montré qu’il
existe des signes d’activité à la dose de 10 mg/kg,
que la molécule soit administrée avec ou sans RT.
Cette étude a randomisé 799 patients prétraités
par docétaxel, après une irradiation avec une dose
unique de 8 Gy, en 2 groupes : ipilimumab à la dose
de 10 mg/kg aux semaines 1, 4, 7 et 10 puis toutes
les 12 semaines jusqu’à progression, ou placebo.
Les patients ne devaient pas avoir reçu plus de
2 lignes de CT. Le critère principal était la SG, et
les critères secondaires, la SSP et la tolérance.
Le taux de réponse était un critère exploratoire
(figure 1).
Les médianes de SG ont été respectivement de 11,2
(9,5-12,7) versus 10,0 mois (8,3-11,0) [HR = 0,85 ;
IC95 : 0,72-1,00 ; p = 0,053] (fi gure 2).
Les SSP étaient respectivement de 4 (3,6-4,3) versus
3,1 mois (IC95 : 2,9-3,4) [HR = 0,70 ; IC95 : 0,61-0,82 ;
p < 0,0001). Le taux de réponse PSA était de 13,1 %
(9,5-17,5) [fi gure 3].
Une analyse en sous-groupe a montré que, pour les
patients ayant un meilleur profi l pronostique − taux
de PAL < 1,5 N, taux d’hémoglobine ≥ 11 g/dl et
absence de métastases viscérales −, la médiane de
SG était de 22,7 (17,8-28,3) versus 15,8 mois (13,7-
19,4) [HR = 0,62 ; IC95 :0,45-0,86] (fi gure 4).
Les auteurs ont conclu que l’objectif primaire n’avait
pas été atteint bien que l’ipilimumab ait montré
une certaine activité, avec une augmentation de
la SSP, une augmentation des réponses PSA et un
profi l de tolérance correspondant aux données des
études préliminaires. Ces résultats justifi ent d’autres
investigations chez des patients se présentant à un
stade moins tardif de la maladie.
Actualités
au 38e ESMO

Figure 3. CA184-043 : objectifs secondaires et exploratoires.
Figure 4. CA184-043 : analyse de la survie globale du sous-groupe exploratoire.
Figure 2. CA184-043 : survie globale (population en intention de traiter).
0,8
1,0
0,6
0,4
0,2
0,0
0
399
400
Patients à risque (n)
4
306
332
2
362
376
8
228
222
6
260
281
24
37
26
22
52
36
Ipilimumab (n = 399) Placebo (n = 400)
SG médiane, mois (IC95)11,2 (9,5-12,7) 10,0 (8,3-11,0)
HR = 0,85 ; IC95 : 0,72-1,00 ; log-rank p stratifi é = 0,0530
SG à 1 an (%) 47 40
SG à 2 ans (%) 26 15
Ipilimumab (n = 146) Placebo (n = 142)
SG médiane, mois (IC95)22,7 (17,8-28,3) 15,8 (13,7-19,4)
HR = 0,62 ; IC95 : 0,45-0,86
Ipilimumab
Ipilimumab
Ipilimumab
Analyse post-hoc du sous-groupe de patients
ayant un meilleur profi l pronostique : PAL < 1,5 N,
hémoglobine ≥ 11 g/dl, pas de métastases viscérales
Placebo
Placebo
Placebo
Censuré
Censuré
Censuré
Censuré
Censuré
Censuré
12
155
138
10
195
184
28
15
12
26
24
16
Mois
16
106
77
14
131
106
32
4
2
30
9
6
20
69
47
18
85
65
36
1
0
34
3
1
38
0
0
Proportion de patients vivants
80
100
60
40
20
0
0428624221210 2826
Mois
1614 32302018
SSP (%)
Ip
ilim
u
SG médian
e,
moi
s (
IC
95
)
22,
7
Analyse post-h
ay
ant un meill
e
hémoglobine
≥
80
100
60
40
20
0
0428624221210 2826
Mois
1614 32 34 36 38302018
SG (%)
Ipilimumab (n = 399) Placebo (n = 400)
Objectif secondaire
SSP médiane, mois (IC95) 4,0 (3,6-4,3) 3,1 (2,9-3,4)
HR = 0,70 ; IC95 : 0,61-0,82 ; p < 0,0001
Objectif exploratoire
Taux de réponse PSA,
% (IC95)
13,1 (39/297*)
(9,5-17,5)
5,3 (16/305*)
(3,0-8,4)
* Patients évaluables.
La Lettre du Cancérologue • Vol. XXII - n° 11 - décembre 2013 | 455
Résumé
En ce qui concerne le cancer de la prostate, les résultats globalement négatifs de la première étude
dephaseIII évaluant l’ipilimumab après radiothérapie, à la suite d’un traitement par docétaxel, ainsi que
les actualités concernant les nouvelles hormonothérapies ont représenté les principales informations
decette édition 2013 de l’ESMO. Dans les cancers du rein métastatiques, la déception quant au blocage
de la voie du FGF par le dovitinib est venue des résultats négatifs de l’étude de phaseIII comparant cette
molécule au sorafénib. Enfin, dans les cancers urothéliaux, de nouvelles approches thérapeutiques sont
toujours recherchées.
Mots-clés
Cancer de la prostate
Ipilimumab
Hormonothérapie
Enzalutamide
ODM-201
Cancer du rein métastatique
Cancer papillaire
c-MET
Antiangiogénique
Évérolimus
Cancer urothélial
métastatique
Vinfl unine
Éribuline
Summary
In prostate cancer, negative
results of the first phaseIII
trial which has evaluated ipili-
mumab compared to placebo
after bone radiotherapy in the
post-docetaxel setting and
news concerning hormone
treatments were the highlights
of the ESMO meeting 2013. In
kidney cancer, the blockade
of the FGF pathway is disap-
pointing with the negative data
of a phase III study comparing
dovitinib and sorafenib. In
metastatic transitional cell
carcinomas, new approaches
are always warranted.
Keywords
Prostate cancer
Ipilimumab
Hormone therapy
Enzalutamide
ODM-201
Metastatic kidney cancer
Papillary renal cell carcinoma
c-MET
Antiangiogenic
Everolimus
Metastatic bladder cancer
Vinfl unine
Eribuline

Figure 5. Enzalutamide chez les patients hormononaïfs.
Figure 6. Méta-analyse dégarélix versus agoniste de la LH-RH.
60
80
40
100
20
0
– 20
– 40
– 60
– 80
– 100
1741310 37341916 4340
Mois
2522 49 52 6155 6458 67463128
Pourcentage de baisse du PSA (%)
90
100
Survie sans progression biologique (PSA) : tous les patients
Dégarélix
Agoniste de la LH-RH
80
70
2808456 308280140112 364336
Jours
196168 252224
SSP (%)
456 | La Lettre du Cancérologue • Vol. XXII - n° 11 - décembre 2013
Cancers urologiques
Concernant l’hormonothérapie...
au stade d’hormonosensibilité
Monothérapie par enzalutamide dans les cancers
hormononaïfs : analyse complète de l’étude
de phase II déjà présentée au congrès américain
en oncologie clinique
D’après Smith MR et al., abstr. 2852
Le critère de jugement principal était une diminution
du taux de PSA d’au moins 80 % à la vingt-cinquième
semaine. Les résultats sont impressionnants, comme
le montre la fi gure 5, avec une médiane de pour-
centage maximal de baisse du PSA de 99,6 % par
rapport à l’état basal (IC95 : −100 ; −86,5). Au total,
92,5 % des patients (62 sur 67) ont eu une réponse
PSA à la semaine 25. Cette baisse du PSA était main-
tenue au-delà des 25 semaines chez les patients
poursuivant le traitement, qu’ils aient ou non des
métastases.
Parmi les modifi cations métaboliques en rapport
avec l’inhibition du RA, il faut relever une élévation
de la testostéronémie de 114,3 % et de l’estradiol de
71,7 % ainsi que le maintien de la densité osseuse
à la semaine 25.
Méta-analyse des essais comparant le dégarélix
aux agonistes de la LH-RH
D’après Tombal B et al., abstr. 2855
Le dégarélix est un antagoniste de la LH-RH.
Il entraîne une baisse de la testostéronémie sans
“fl are up” transitoire.
Six essais comparatifs de phase III ont inclus
2 328 patients : 1 491 étaient traités par dégarélix,
et 837 par un agoniste de la LH-RH (458 par gosé-
réline, 379 par leuproréline).
Les données (figure 6) sont en faveur du déga-
rélix, puisqu’il existe une différence signifi cative
en termes de SSP (HR = 0,71 ; IC
95
: 0,54-0,94),
de risque d’événements sur le tractus urinaire
(HR = 0,58 ; IC
95
: 0,39-0,84 ; p = 0,004) et d’évé-
nements musculo-squelettiques (HR = 0,67 ; IC95 :
0,50-0,90 ; p = 0,007).
Le risque d’événements cardiovasculaires ou de décès
liés (tableau I) était moindre avec le dégarélix. Bien
que peu de patients soient décédés de leur cancer
de la prostate lors de l’analyse de l’étude, la SG était
également meilleure (HR = 0,47 ; IC95 : 0,25-0,90 ;
p = 0,022).
Cette méta-analyse regroupant des études très diffé-
rentes, il faudra attendre la publication défi nitive
pour avoir une analyse critique de ces résultats.
Dans les cancers de la prostate
métastatiques résistants à la castration
Étude de phase I/II de tolérance et preuve du
concept de l’ODM-201 dans les cancers de la
prostate métastatiques résistants à la castration
en progression
D’après Fizazi K et al., abstr. 2853
Le profil de l’ODM-201 est différent de ceux du
MDV3100 et de l’ARN-509, avec une inhibition
supérieure de la croissance tumorale dans certains
modèles précliniques.
Cette étude de phase II d’expansion ayant inclus
110 patients avait pour objectif d’établir la dose des
futurs essais (200, 400 ou 1 400 mg/j) ainsi que
Tableau I. Dégarélix versus agoniste de la LH-RH : événements indésirables.
Dégarélix
(n = 1 491)
Agoniste de la LH-RH
(n = 837)
Tout événement cardiovasculaire, n (%) 40 (2,7) 37 (4,4)
Événement cardiovasculaire sérieux
(avec menace vitale ou hospitalisation), n (%) 25 (1,7) 24 (2,9)
Actualités
au 38e ESMO

Figure 7. ODM-201 dans les CPRCm en progression : réponse PSA à 12 semaines.
0
25
– 25
– 50
– 75
– 100
CT et CYP17i-naïf Post-CT et CYP17i-naïf Post-CYP17i
Baisse du PSA ≥ 50 % : 65 % 32 % 9 %
Baisse du PSA ≥ 30 % : 71 % 52 % 20 %
À la dose de 1 400 mg, 6 patients sur 7 ont eu une baisse du PSA ≥ 50 %
* Data truncated at +25 %
***
200 mg 400 mg 1 400 mg
La Lettre du Cancérologue • Vol. XXII - n° 11 - décembre 2013 | 457
d’évaluer son effi cacité et sa tolérance chez des
malades chimionaïfs ou prétraités par docétaxel.
Trois doses ont été sélectionnées pour cette
étude. Chez les patients n’ayant pas reçu de CT ou
d’inhibiteur de CYP17, le taux de réponse biologique
a été de 65 %. Il était de 32 % chez les patients
prétraités par CT mais n’ayant pas reçu d’inhibiteur
de CYP17 et de seulement 9 % après inhibiteur de
CYP17 (fi gure 7).
Pour ces 3 groupes de patients, le taux de réponse
ou de stabilisation de leur maladie sur les CTC à
12 semaines était respectivement de 74, 74 et 47 %.
Les toxicités de grade 3 ont été limitées à la fatigue
(1 %), à des lombalgies (1 %), à des nausées (1 %) et à
des douleurs (1 %). Il n’a pas été observé d’accidents
convulsifs, la tolérance a été très bonne. Il n’est pas
évident qu’il existe un effet dose.
Étude de phase I/II d’un inhibiteur de la bio synthèse
des androgènes, ASP9521, dans les CPRCm
D’après Loriot Y et al., abstr. LBA22
ASP9521, premier inhibiteur oral de 17β-HSD,
avait démontré une activité antitumorale dans des
modèles précliniques. Malgré une escalade de dose
de 30 à 600 mg et une tolérance correcte, il n’a
montré aucune effi cacité.
Le problème des séquences a été abordé par
G. Attard et Y. Loriot
D’après Attard G et al., abstr. 30 ; Loriot Y et al.,
poster discussion
Y a-t-il des séquences optimales dans le contexte
d’un manque de facteurs prédictifs de réponse ?
devons-nous faire des combinaisons ? si oui,
lesquelles ?
J. Mezynski et al. (1) ont rapporté, dans une série
anglaise très limitée, des taux de réponse faibles
avec le docétaxel après abiratérone. Cela n’a pas
été retrouvé avec le cabazitaxel dans une étude
franco-anglaise.
Y. Loriot et al. ont récemment publié, dans Annals of
Oncology (2), des taux de réponse très limités (8 % ;
temps jusqu’à progression : 2,5 mois) avec l’abiraté-
rone après MDV3100 chez des patients traités dans
le protocole AFFIRM.
A.J. Schrader et al. (3) ont retrouvé d’aussi piètres
résultats avec la séquence inverse, ce qui laisse
supposer qu’il existe une résistance croisée entre
les 2 traitements.
Existe-t-il une association entre la réponse au docé-
taxel et la durée de la CT et une hormonothérapie
préalable à l’enzalutamide dans l’essai AFFIRM
(De Bono J et al., abstr. 2862) ?
Après analyse de 3 groupes basés sur des durées
d’expo sition différentes, le bénéfi ce de l’enzaluta-
mide en termes de SG, de SSP radiographique et
de réponse PSA est apparu maintenu indépendam-
ment de la durée… Des résultats similaires ont été
rapportés avec l’abiratérone dans l’étude COU-AA-
301, avec un bénéfi ce en survie maintenu indépen-
damment de la durée du docétaxel.
Combinaison concomitante d’enzalutamide et
d’abiratérone dans les cancers de la prostate
résistants à la castration avec métastases osseuses
D’après Efstathiou E et al., abstr. 2854
Le but était de co-cibler le RA et la biosynthèse
des androgènes en réalisant des analyses ancil-
laires moléculaires et biologiques de la biosynthèse
des stéroïdes dans le sang et la moelle. Chez les
Actualités
au 38e ESMO

Figure 8. Abiratérone + enzalutamide.
75
25
12 %
0
100
50
49 patients évaluables
Baisse ≥ 30 % : 83,6 % (41/49)
Baisse ≥ 50 % : 75,5 % (37/49)
Baisse ≥ 90 % : 44,9 % (22/49)
– 30
– 50
– 75
– 100
– 90
Modifi cation du PSA (%)
458 | La Lettre du Cancérologue • Vol. XXII - n° 11 - décembre 2013
Cancers urologiques
60 patients inclus, aucune toxicité majeure n’a été
mise en évidence ; le temps médian d’exposition
était de 164 jours (18-409). Une baisse du PSA
d’au moins 50 % a été constatée chez 75,5 % des
49 patients évaluables (fi gure 8). Cette étude non
comparative de 2 molécules très actives ne permet
pas de conclure quant à l’augmentation potentielle
de l’activité par leur association…
Cancers du rein métastatiques
Résultats négatifs d’une étude de phase III
comparant le dovitinib au sorafénib après une
première ligne par antiangiogénique et une
première ligne par inhibiteur de mTOR
D’après Motzer R et al., abstr. LBA 34
L’activation de la voie du FGF a été proposée dans les
mécanismes d’échappement des antiangiogéniques.
Le dovitinib est un ITK qui cible FGFR, VEGFR, PDGFR
et d’autres kinases. Une étude de phase II avait
rapporté une médiane de SSP de 5,5 mois ; celle de
SG était de 11,8 mois.
Cette étude de phase III a randomisé (1:1)
570 patients entre dovitinib (n = 284 ; 500 mg/j,
5 jours “on” et 2 jours “off”) et sorafénib (n = 286 ;
400 mg × 2/j). Les médianes de SSP ont été
respectivement de 3,7 et 3,6 mois (HR = 0,86 ;
IC95 : 0,72-1,04) et les médianes de SG de 11,1 et
11 mois (HR = 0,96 ; IC
95
: 0,75-1,22). Dans le groupe
dovitinib, la tolérance a été correcte.
Le problème de l’hétérogénéité tumorale pour
apprécier la réponse aux antiangiogéniques
D’après Crusz SM et al., abstr. 2700
L’hétérogénéité des réponses et des modes de
progression des métastases chez les patients ont fait
l’objet de cette analyse radiologique longitudinale
du suivi de lésions métastatiques dans le cadre de
2 essais de phase II prospectifs testant le pazopanib
(800 mg/j) et le sunitinib (50 mg, 4 semaines “on”
suivies de 2 semaines “off”). Réalisée sur 30 patients
(14 dans le groupe pazopanib, 16 dans le groupe
sunitinib), elle a porté sur 147 lésions métastatiques.
Des réponses hétérogènes étaient observées chez
67 % des patients.
À la progression, 42 % des métastases restaient
contrôlées, la majorité des patients (90 %) progres-
sant sous forme de nouvelles lésions. Pour un même
individu, l’hétérogénéité des réponses et des résis-
tances refl ète l’hétérogénéité intratumorale ainsi
que les limites d’une simple biopsie…
Implications pronostiques de la néphrectomie chez
les patients présentant des métastases synchrones
D’après Bamias A et al., abstr. 2701
En attendant les données des études contrôlées pros-
pectives CARMENA (comparant néphrectomie puis
sunitinib versus sunitinib seul) et EORTC (néphrec-
tomie puis sunitinib versus sunitinib puis néphrec-
tomie), cette étude rétrospective européenne de
patients traités par sunitinib présentée par A. Bamias
a regroupé 458 patients (traités entre octobre 2005
et janvier 2012), dont 170 vivaient en Grèce, 186 en
France et 102 en Belgique.
Il y avait 186 métastases synchrones : 57 en Grèce,
75 en France et 54 en Belgique.
Avec une médiane de 34 mois, la survie était signi-
fi cativement meilleure chez les patients néphrecto-
misés, mais les caractéristiques à l’inclusion étaient
très différentes.
En analyse multivariée, la néphrectomie était
un facteur pronostique significatif (HR = 0,54 ;
IC95 : 0,30-0,97). À revoir…
Les résultats en fonction de la classifi cation pronos-
tique sont exposés dans le tableau II.
Tableau II. Néphrectomie chez les patients avec métastases synchrones.
HR (IC95) p HR (IC95)p
Néphrectomie
Oui
Non
1
0,42 (0,26-0,68) < 0,001 1
0,43 (0,28-0,68)
MSKCC
Favorable
Intermédiaire
Mauvais
1
1,87 (1,18-2,97)
3,60 (1,44-9,02)
0,008
0,006
IMDC
Favorable
Intermédiaire
Mauvais
1
1,19 (0,70-2,05)
2 ,41 (1,27-4,58) 0,519
0,007
Actualités
au 38e ESMO
 6
6
 7
7
1
/
7
100%