n°33 - Institut de Biosciences et Biotechnologies de Grenoble (BIG)

LETTRE SCIENTIFIQUE
Physiologie Cellulaire & Végétale!1
Système biomimétique
Jean-Louis Martiel
Page 1
!Lettre n° 33 - Février 2013
iRTSV
Résultats scientifiques
Institut de Recherches en Technologies et Sciences pour le Vivant
Fonctions intégrées des protéines - Du vivant aux nanotechnologies
Biofilms in vivo
Marie-Odile Fauvarque
Page 3
Nano-machine moléculaire
Maria-Guillermina Casabona
Page 2
Direction des Sciences du Vivant
Pour comprendre cette dynamique, les chercheurs
de l’équipe Physique du cytosquelette et de la morpho-
genèse du laboratoire Physiologie Cellulaire &
Végétale, en collaboration avec Cécile Sykes de
l’Institut Curie (Paris) utilisent un système biomi-
métique permettant de reconstituer in vitro un tel
réseau d'actine. Ce système est composé de mo-
nomères d’actine, d’un complexe qui initie et réti-
cule des filaments d'actine (Arp2/3), d’un activa-
teur de ce complexe qui recouvre la surface de
billes de polystyrène, et d’une protéine qui inter-
rompt l’élongation de ces polymères d’actine (la
protéine de coiffe CP). Dans ce système biomimé-
tique, le réseau d’actine qui se développe à la sur-
face des billes est capable de les propulser.
Cette nouvelle étude vise à caractériser la produc-
tion de forces générées par les réseaux de filaments
d’actine afin de mieux en comprendre la complexi-
té en combinant la reconstitution du mouvement
de ces billes et des modèles biophysiques. Tout
d’abord, ces chercheurs ont modélisé la cinétique
de croissance de réseaux de filaments à partir de
filaments d’actine isolés positionnés à la surface
d’une bille (Figure A). Chaque filament isolé est à
l’origine d’un réseau réticulé qui
se développe grâce i) à l’élonga-
tion des filaments par polyméri-
sation des monomères d’actine et
ii) par leur branchement donnant
lieu à une structure arborescente.
Ceci est rendu possible par le
complexe Arp2/3 qui initie et
réticule des filaments d'actine et
par l’activateur de ce complexe
fixé à la surface des billes (Figure
B). Néanmoins l'élongation de ces
filaments est limitée par l’action
de la protéine de coiffe condui-
sant à la densification des ré-
seaux. Pour une combinaison
favorable des concentrations de
Arp2/3 et de CP, il a formation
d’un gel d’actine. Ces étapes (ini-
tiation, réticulation et élongation)
sont simples à simuler par un
modèle peu coûteux en temps de
calcul et ceci pour un nombre
réaliste d’environ 10!000 filaments
par bille.
Système biomimétique
Les cellules se déplacent et se déforment en utilisant la force développée par leur cytosquelette d’actine. Ce cytos-
quelette est fait d’un grand nombre de filaments, formant un réseau dont la composition et la dynamique sont très
complexes et en perpétuel réarrangement.
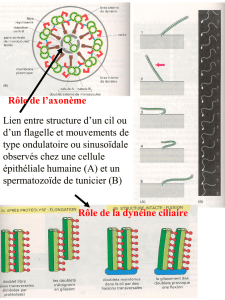
Figure. Différentes étapes de la croissance du réseau d’actine à la surface d’une bille fonctionnalisée.
A. Génération de sous-réseaux en différents points sur la bille.
B. Extension, branchement et enchevêtrement des sous-réseaux.
C. Lorsque l’enchevêtrement est complet, les interactions entre sous-réseaux sont modélisées par des ressorts.
D. La force due à la polymérisation de monomères dans le réseau parvient à rompre l’un des ressorts.
A Contact de filaments d’actine isolés et activation B Branchement par Arp2/3 et extension des sous-réseaux
C Enchevêtrement des sous-réseaux D Brisure de symétrie et rupture du réseau
temps temps
temps
Suite en dernière page

LETTRE SCIENTIFIQUE
2!Biologie du Cancer et de l'Infection
L’équipe Pathogenèse Bactérienne et Réponses Cellu-
laires du laboratoire Biologie du Cancer et de l’In-
fection cherche à élucider les mécanismes molécu-
laires de la pathogénicité bactérienne et à décryp-
ter les réponses cellulaires de l'hôte à l'infection.
Une nouvelle nano-machinerie moléculaire capa-
ble de pourvoir «!la bonne santé!» de bactéries en
leur permettant de mener une guerre intra- et in-
ter- espèces a été récemment identifiée dans l'enve-
loppe bactérienne (Figure 1). Cette structure res-
semble au bactériophage ; appelée système de
sécrétion de type VI (SST6), elle se présente sous la
forme d’un appendice retrouvé à la surface de la
bactérie et composé de plus de 15 protéines qui
agissent en tant que dispositifs d'injection de toxi-
nes ou d’autres effecteurs. Dans une étude bio-in-
formatique précédente [1], SST6 avait été caractérisé
comme étant un complexe de 13 protéines retrou-
vées à la fois chez les bactéries pathogènes et les
non pathogènes. De plus, cette étude avait mis en
évidence que certaines bactéries, tel le pathogène
opportuniste humain Pseudomonas aeruginosa, pré-
sentaient un certain nombre de gènes accessoires
spécifiques localisés dans le même opéron que
celui qui code pour des protéines connues comme
étant impliquées dans la régulation de l’activation
de SST6.
Une nouvelle étude a été réalisée en collaboration
avec le groupe du Dr Joseph Mougous de l'Univer-
sité de Washington [2] dans le but de caractériser les
produits de ces gènes accessoires, souvent associés
aux besoins spécifiques de la bactérie, afin de
mieux comprendre le rôle de SST6 dans les interac-
tions intra- et inter- bactériennes. Dans ce but, les
chercheurs ont construit des mutants de P. aerugi-
nosa délétés des gènes accessoires tagS, tagT, tagR
et tagQ (Figure 2). Les systèmes de sécrétion dans
ces bactéries mutantes se sont avérés être correc-
tement assemblés mais incapables de sécréter leur
toxines, suggérant que ces protéines ont un rôle
dans la régulation de l’activation du SST6. Avec
l’aide de la plate-forme protéomique de l’iRTSV, il
a été montré que TagQ est une lipoprotéine qui est
localisée sur la membrane externe de P. aeruginosa
et qui est indispensable pour l'ancrage de TagR, un
acteur clef dans l’activation du SST6, sur cette
même membrane. Enfin des approches biochimi-
ques ont permis de montrer que TagT et TagS for-
ment un nouveau transporteur ABC intra-mem-
branaire, lui aussi indispensable à l'activation du
SST6.
Ces études ont permis de proposer un modèle
rendant compte du fait que les protéines considé-
rées comme accessoires pour le système de sécré-
tion SST6 participent très probablement à une
voie de signalisation trans-membranaire qui
favorise la mise au point du dispositif d'injection
dans des conditions environnementales appro-
priées.
Contacts : Maria-Guillermina Casabona
Ina Attrée
BCI
Laboratoire Biologie du Cancer et de l'Infection
UMR_S 1036 - CEA - Inserm - UJF
Références
[1] Boyer F, Fichant G, Berthod J, Vandenbrouck
Y and Attree I. Dissecting the bacterial type VI
secretion system by a genome wide in silico
analysis: What can be learned from available
microbial genomic resources? BMC Genomics,
2009, 10: 104
[2] Casabona MG, Silverman JM, Sall KM,
Boyer F, Coute Y, Poirel J, Grunwald D,
Mougous JD, Elsen S and Attree I. An ABC
transporter and an outer membrane lipoprotein
participate in posttranslational activation of
type VI secretion in Pseudomonas aeruginosa.
Environmental Microbiology, 2013, 15(2): 471-486
Les microbes vivent dans presque tous les environnements, formant des communautés poly-microbiennes appe-
lées biofilms. Pendant la colonisation et l'infection des tissus, les agents pathogènes et commensaux cohabitent,
interagissent, communiquent et combattent pour les éléments nutritifs. Dans la plupart des cas, un contact di-
rect de cellule à cellule est nécessaire pour ce phénomène.
Guerre civile bactérienne
Un opéron est un groupement de gènes qui sont transcrits ensemble en ARN messager.
Les transporteurs ABC forment un vaste ensemble de protéines transmembranaires dont le rôle est le transport
unidirectionnel de part et d'autre de la membrane cytoplasmique de diverses substances (ions, stérols, macromolé-
cules...) en utilisant l'énergie fournie par l'hydrolyse de l'ATP.
E. coli P. aeruginosa + E. coli
P. aeruginosa ΔtagQ +
E. coli
Figure 2. Tests de compétition entre P. aeruginosa et Escherichia coli, une autre bactérie à Gram négatif.
A - Mono-culture de Escherichia coli (colonies colorées).
B - Test de compétition entre E. coli et une souche sauvage de P. aeruginosa. Toutes les colonies de E. coli sont tuées.
C - Dans ces tests de compétition, les quatre mutants de délétion de P. aeruginosa ΔtagQ, ΔtagR, ΔtagS et ΔtagT, sont mis en
culture en présence de E. coli. Leur capacité à injecter une toxine dépendante du SST6 est évaluée au travers de ce test visuel.
A B
C
P. aeruginosa ΔtagR +
E. coli
P. aeruginosa ΔtagS +
E. coli
P. aeruginosa ΔtagT +
E. coli
toxines
T6SS
Pseudomonas aeruginosa
Cellule cible
(Gram-)
Figure 1. L’injection des
toxines via SST6 est dé-
pendante d’un contact
entre deux cellules.

LETTRE SCIENTIFIQUE
Biologie à Grande Échelle!3
La formation de biofilms bactériens résulte de l’intégration de signaux émanant de l’environnement par les bacté-
ries qui acquièrent la capacité de s’agglomérer pour former une communauté sessile, protégée de l’extérieur par
la sécrétion de macromolécules biologiques, typiquement!: des exopolysaccharides, des protéines d’adhésion et de
l’ADN extracellulaire. Ces biofilms posent des problèmes de santé publique dès lors qu’on les retrouve sur des
instruments médicaux (implants, cathéters, sondes,…) ou qu’ils permettent à la bactérie d’échapper aux défenses
immunitaires de l’hôte et aux traitements antibiotiques. Ils constituent également un réservoir de bactéries favori-
sant l’apparition de mutants plus virulents ou résistants aux antibiotiques.
La bactérie Pseudomonas aeruginosa présente une
capacité singulière de transition entre un mode de
vie «!planctonique !» (mobile et virulent) et un
mode «!biofilm!» (sessile et moins virulent). Très
sensible à la phagocytose des polynucléaires neu-
trophiles, elle n’est pas pathogène pour les indivi-
dus sains, mais peut causer des infections mortel-
les chez les patients présentant un déficit de l’im-
munité cellulaire (personnes traitées par une chi-
mio-thérapie, en réanimation ou greffées,…). P.
aeruginosa est également une des premières causes
d’infections broncho-pulmonaires chez les patients
atteints de mucoviscidose.
La compréhension des mécanismes de régulation
bactériens contrôlant la formation de biofilms peut
ouvrir la voie vers de nouvelles approches théra-
peutiques. À l’heure actuelle, l’essentiel de la re-
cherche sur les biofilms bactériens se fait in vitro et
fait donc abstraction de la réponse immunitaire de
l’hôte. L’équipe Génétique & Chemogénomique du
laboratoire Biologie à Grande Échelle a utilisé la
mouche du vinaigre, Drosophila melanogaster, qui
possède une immunité cellulaire efficace, pour
mimer des infections chroniques à P. aeruginosa.
Dans ce modèle, les mouches sont infectées par
voie orale avec de la nourriture contaminée. La
virulence des bactéries est mesurée par leur capaci-
té à tuer les mouches infectées tandis que leur
capacité à coloniser le tractus intestinal est obser-
vée par microscopie confocale (Figure). La souche
de laboratoire Pseudomonas PAO1 est ainsi capable
de tuer les drosophiles en moins d’une semaine!;
elle est retrouvée sous forme de micro-colonies
extrêmement denses, caractéristiques de biofilms,
dans les zones antérieures du tractus intestinal!:
gésier, et proventricule (Figure). Ce système a été
utilisé dans le cadre d’une étude extensive d’une
souche Pseudomonas PAO1::PprBK menée par
l’équipe du Dr Sophie de Bentzmann de l’Univer-
sité Aix-Marseille. In vitro, cette souche forme très
facilement des biofilms. En cohérence avec les
observations faites in vitro, cette souche présente
une capacité accrue à former des biofilms chez la
mouche !; ainsi se maintient-elle non seulement
dans la zone antérieure du tractus intestinal, mais
également dans l’intestin moyen où la formation
de biofilms est mise en évidence par la détection
d’ADN extracellulaire autour des micro-colonies
(Figure). Chez la mouche, Pseudomonas
PAO1::PprBK se révèle moins virulente que la sou-
che parentale!: un phénotype lié d’une part à une
capacité réduite de traverser la barrière épithéliale
intestinale, et donc de disséminer dans l’hémo-
lymphe, et d’autre part, à l’absence de sécrétion de
toxines de système de sécrétion de type III (résul-
tats obtenus par l’équipe Pathogenèse Bactérienne et
Réponses Cellulaires du laboratoire Biologie du
Cancer et de l’Infection).
Ces résultats serviront de fondement pour lancer
de nouvelles recherches visant à identifier les
facteurs microbiens contrôlant les infections
chroniques ou aiguës dues à P. aeruginosa ainsi
que les facteurs génétiques ou physiologiques
qui, chez l’hôte, interfèrent avec la formation de
biofilms ou la dissémination des bactéries.
Des biofilms in vivo
Contact : Marie-Odile Fauvarque
BGE
Laboratoire Biologie à Grande Échelle
UMR_S 1038 - CEA - Inserm - UJF
Référence
de Bentzmann S, Giraud C, Bernard CS,
Calderon V, Ewald F, Plesiat P, Nguyen C,
Grunwald D, Attree I, Jeannot K, Fauvarque
MO and Bordi C. Unique biofilm signature,
drug susceptibility and decreased virulence in
Drosophila through the Pseudomonas aeruginosa
two-component system PprAB. PLoS Pathogens,
2012, 8(11): e1003052
PAO1::PprBK PAO1::PprBKPAO1
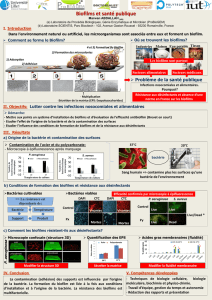
Figure. Le tractus intestinal des mouches est disséqué,
fixé et marqué après 1 jour d’infection par voie orale.
En rouge!: le marquage de l’actine permet de visualiser
les tissus de la mouche.
En bleu!: le marquage DAPI colore l’ADN et permet
de repérer les noyaux des cellules de l’épithélium intes-
tinal ou l’ADN bactérien extracellulaire.
En vert!: on observe les bactéries qui expriment une
protéine fluorescente (GFP).
Les deux souches PAO1 et PAO1::PprBK colonisent
très fortement le proventricule (indiqué PV), une
structure complexe située à l’extrémité antérieure de
l’intestin. La souche PAO1::PprBK est également
capable de s’ancrer fréquemment dans les parties
médianes de l’intestin (midgut indiqué MG) et de
sécréter massivement de l’ADN extracellulaire (Poin-
tes de flèches blanches, images de droite).
Les images du bas correspondent au grossissement de
la zone indiquée par un carré blanc, images du haut.
Images confocales : plate-forme d’imagerie de l’iRTSV.
Toxines de type III : certaines bactéries fabriquent des
toxines qu’elles injectent directement dans le cytoplasme
d’une cellule cible par le biais d'une nano-machinerie en
forme d'aiguille (système de sécrétion de type III). Pseu-
domonas aeruginosa est l’une de ces bactéries. Cf Lettres
scientifiques de l’iRTSV n° 16 et 29.

4!Contacts : [email protected]
Les laboratoires de l’iRTSV
Directeur de la publication
Dr. Jérôme Garin
Éditeur et format électronique
Pascal Martinez — [email protected]
Comité de rédaction
Ina Attrée, Maria-Guillermina Casabona, Marie-Odile
Fauvarque, Jean-Louis Martiel.
Institut de Recherches en Technologies et
Sciences pour le Vivant
http://www-dsv.cea.fr/irtsv
http://www-dsv.cea.fr/irtsv/lettres
CEA Grenoble
17 rue des Martyrs
38 054 Grenoble cedex 09
Responsable : Jérôme Garin
Tel. : 04 38 78 45 01
Fax : 04 38 78 51 55
© CEA [2013]. Tous droits réservés. Toute reproduction totale ou partielle sur quelque support que ce soit ou utili-
sation du contenu de ce document est interdite sans l’autorisation écrite préalable du CEA
"
BCI
Biologie du Cancer
et de l'Infection
UMR_S 1036
CEA/Inserm/UJF
BGE
Biologie à Grande
Échelle
UMR_S 1038
CEA/Inserm/UJF
CBM
Chimie et Biologie
des Métaux
UMR 5249
CEA/CNRS/UJF
PCV
Physiologie Cellu-
laire & Végétale
UMR 5168
CEA/CNRS/UJF/Inra
GPC
Groupe Physiopa-
thologie du Cytos-
quelette
iRTSV et UMR_S 836
UJF/Inserm/CEA/CHU
Lorsque la bille est entièrement recouverte par
l’enchevêtrement des différents réseaux réticulés, il
devient nécessaire d’intégrer au modèle cinétique,
un autre modèle rendant compte de la mécanique
des filaments. Les chercheurs adoptent une des-
cription ‘coarse grained’ dans laquelle les réseaux
arborescents sont représentés par des points, et les
interactions à l’interface entre deux réseaux par
des ressorts (Figure C). On peut ainsi "oublier" les
détails (filaments) pour se concentrer sur la dyna-
mique globale des réseaux. Les forces dues à l’al-
longement des filaments (calculées par le modèle
cinétique) sont appliquées aux ressorts (modèle
‘coarse grained’) et les mettent sous tension (Figures
C et D). Lorsque l’extension d’un des ressorts dé-
passe un certain seuil, une fissure apparaît. En se
propageant, cette fissure conduit à une brisure de
symétrie (ou ouverture) du réseau global entou-
rant la bille et in fine, à la propulsion de la particule
(Figures D).
Cette synergie expérience-modèle a permis
d’identifier et de formuler les principes gouver-
nant la dynamique et l’organisation du cytosque-
lette. Ces recherches permettent de mieux com-
prendre le rôle de cette dynamique dans les cel-
lules (conditions normales et pathologiques). Par
exemple ces études mettent en évidence les con-
séquences des dysfonctionnements mécaniques
intracellulaires pour des pathologies aussi graves
que le cancer.
Référence
Kawska A, Carvalho K, Manzi J,
Boujemaa-Paterski R, Blanchoin L, Martiel JL
and Sykes C. How actin network dynamics
control the onset of actin-based motility.
Proceedings of the National Academy of Sciences,
2012, 109(36): 14440-14445
Contact : Jean-Louis Martiel
LPCV
Laboratoire Physiologie Cellulaire & Végétale
UMR 5168 - CEA - CNRS - UJF - Inra
1
/
4
100%