Mimer le vivant pour étudier les mécanismes de contraction

ComUE
> > > Accueil Présentation Actualités Actus recherche
Mimer le vivant pour étudier les mécanismes de contraction cellulaire
Recherche, Sciences de la Vie et Santé
Mieux comprendre l'origine des dysfonctionnements mécaniques intracellulaires
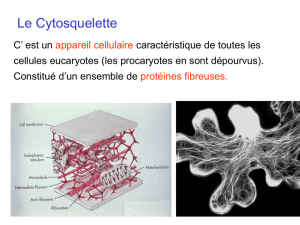
Grâce à la conception d'un dispositif imitant un squelette
cellulaire, des chercheurs du Laboratoire de Physiologie
Cellulaire & Végétale (CEA / CNRS / INRA / Université Joseph Fourier Grenoble) ont pu décrypter pour la
première fois une partie des lois d'organisation qui définissent l'architecture des cellules. Ces chercheurs ont
montré que des molécules motrices, les myosines, étaient responsables de la contraction sélective de
certaines structures intracellulaires formées par l'actine, protéine abondamment présente dans les cellules. Le
mécanisme mis en lumière permet de comprendre comment la génération de forces à l'intérieur des cellules
peut être modulée localement et de façon très précise. De tels résultats ouvrent de nouvelles perspectives, en
particulier pour la compréhension de dysfonctionnements observés dans certaines pathologies graves comme
le cancer.
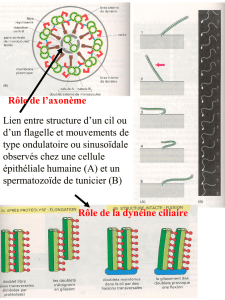
Un filament d'actine est un polymère orienté pouvant s'organiser en différentes architectures : soit parallèles (tous les
filaments sont dans le même sens), soit anti-parallèles (en sens opposés) ou en réseaux denses (entrecroisés). A
l'image de ce qui se passe pour les muscles de l'organisme, il existe, au niveau du cytosquelette de chaque cellule, des
contractions très localisées. A l'origine de ces contractions, les myosines : des protéines motrices qui déplacent et
déforment les filaments d'actine. Au sein d'une cellule, les différentes architectures d'actine sont agencées de telle sorte
qu'il s'avère extrêmement complexe de les étudier séparément. C'est pour cette raison que, jusqu'à présent, il n'était
pas possible d'étudier l'impact qu'a l'agencement des filaments d'actine sur la force exercée par les myosines.
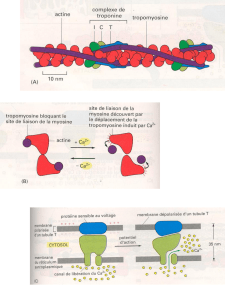
Dans le cadre de cette étude, les chercheurs ont créé un dispositif imitant un squelette cellulaire dans lequel les
différentes architectures de filaments d'actine sont géométriquement séparées les unes des autres, devenant ainsi
aisément identifiables. Les analyses réalisées grâce à ce dispositif ont montré que les molécules de myosine agissent
de façon spécifique et sélective sur le cytosquelette au cours de la contraction. Ainsi, sous l'action des myosines, les
filaments antiparallèles d'actine se contractent rapidement, tandis que les filaments agencés en réseaux se contractent
plus lentement ; quant aux filaments parallèles, ils ne se contractent pas du tout. Ces phénomènes sélectifs suggèrent
que, dans l'espace intracellulaire, l'action des myosines n'induit la contraction que de certaines structures ciblées. Les
résultats obtenus indiquent également que, dans la cellule, la vitesse de contraction et la déformabilité de chaque
filament d'actine sont déterminées par son agencement.
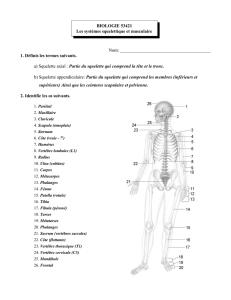
Superposition d'images prises au cours du temps illustrant la déformation d'un anneau de filaments d'actine (en rouge)
sous l'action des myosines (en vert) dans une structure biomimétique. A partir de l'analyse de la vitesse de constriction
de l'anneau, il est possible de déterminer la propriété contractile de ce type de structure. Echelle : 5 micromètres. ©
Anne-Cécile Reymann
Outre l'importance de ces résultats pour la connaissance fondamentale des mécanismes qui régissent certaines
propriétés essentielles des cellules, cette étude constitue une première étape dans le cadre de travaux qui permettraient
de déterminer l'origine des dysfonctionnements mécaniques intracellulaires retrouvés dans des pathologies aussi
graves que le cancer.
Référence :
Reymann AC, Boujemaa-Paterski R, Martiel JL, Guérin C, Cao W, Chin HF, De La Cruz EM, Théry M and Blanchoin B
(2012). , Science AAAS.Actin network architecture can determine myosin motor activity
Mise à jour le 18 septembre 2014
Page 1
1
/
1
100%