niveau de pr

24 | La Lettre de l’Hépato-Gastroentérologue • Vol. XV - n° 1 - janvier-février 2012
EVIDENCE-BASED MEDICINE MICI
Les 5-aminosalicylés protègent-ils
contre le cancer colorectal ?
V. Abitbol (Paris)
Question
non résolue
» Quel est le traitement
le plus efficace entre
la ciclosporine
et l’infliximab à proposer
après échec des corti-
coïdes en intraveineux
lors d’une poussée sévère
de rectocolite hémorra-
gique ?
niveau
de preuve
2
à l’AZA, auquel cas la seule possibilité est l’IFX en
induction puis en entretien, car un traitement en
bridge par la CsA ne sera pas possible, soit il s’agit
d’un malade naïf pour l’AZA et le choix reste ouvert.
C’est dans cette dernière situation que le GETAID
a mené un essai contrôlé randomisé comparant en
ouvert la CsA administrée par voie intraveineuse
(2 mg/kg/j) relayée ensuite par l’IFX administré par
voie orale (5 mg/kg aux semaines 0, 2 et 6) sur une
durée de 3 mois (2). Chez les malades qui avaient
répondu dans les 7 jours, un traitement de fond par
l’AZA était commencé. L’hypothèse de cette étude
était que la CsA était supérieure à l’IFX. Le critère
de jugement principal était l’échec du traitement
défini par l’absence de réponse clinique à 7 jours,
l’absence de rémission clinique et endoscopique à
98 jours, la survenue d’une rechute clinique entre
ces 2 dates, la colectomie, un effet indésirable grave
imposant l’arrêt du traitement et le décès.
Parmi les 111 malades analysés, l’échec du traitement
était observé chez 60 % des 55 malades traités par
CsA et chez 54 % de ceux ayant reçu IFX (différence
absolue de 6 % ; IC
95
: −12 à 25 % ; p = 0,49). Les
taux de réponse obtenus dès la première semaine
de traitement étaient de 85 % avec CsA et de 86 %
avec IFX (p = 0,66). La proportion de malades colec-
tomisés dans les 3 premiers mois était de 18 % sous
CsA et de 21 % sous IFX (p = 0,66). Enfin, les effets
indésirables graves observés dans les 2 groupes de
traitement étaient comparables et correspondaient
aux profils de tolérance attendus : infections, aggra-
vation de la maladie, cytolyse à l’introduction de
l’AZA... Cet essai clinique n’a donc pas démontré que
la CsA était plus efficace que l’IFX dans le traitement
de la poussée sévère et corticorésistante de RCH.
Références bibliographiques
1. Travis SP, Stange EF, Lemann M et al. European evidence-based
consensus on the management of ulcerative colitis: current mana-
gement. J Crohn Colitis 2008;2:24-62.
2. Laharie D, Bourreille A, Branche J et al. Ciclosporine versus
infliximab in acute severe colitis refractory to intravenous steroids:
a randomized study. J Crohns Colitis 2011;5:S8.
Conflit d’intérêts. Interventions ponctuelles auprès de MSD.
Un effet protecteur antitumoral du 5-ASA est probable, mais des preuves
solides manquent. Seules des études cas-témoins ont été publiées. L’asso-
ciation entre la réduction du risque de cancer colorectal et la prise de
salicylés n’est pas nécessairement causale et peut être le résultat de biais.
Ce qu’il faut retenir
niveau
de preuve
4L
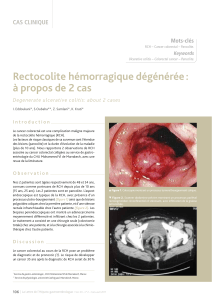
es patients souffrant de rectocolite hémor-
ragique (RCH) ont un risque augmenté de
cancer colorectal (CCR). Le rôle protecteur
des 5-aminosalicylés (5-ASA) dans le cancer a été
avancé et leur utilisation a été recommandée dans
la RCH (1, 2). Néanmoins, les résultats des études
publiées restent contradictoires.
En 2005, une méta-analyse a regroupé 9 études
et a inclus au total 1 932 patients chez lesquels
334 cancers et 140 dysplasies ont été diagnostiqués.
La prise de 5-ASA était associée à une diminution du
risque de CCR (odds-ratio [OR] = 0,51 ; IC95 : 0,37-
0,69) et du risque de cancer et de dysplasie (OR =
0,51 ; IC95 : 0,38-0,69). Le bénéfice était observé
pour une prise régulière ou pour une dose supérieure
à 1,2 g/j. La salazopyrine paraissait avoir un effet
moins protecteur que la mésalazine. Cette méta-
analyse n’avait inclus que des études de cohorte et
de cas-contrôles de méthodologies disparates (3).
Une des premières études négatives a été publiée
par C.N. Bernstein et al. en 2003. Utilisant la base
de données des MICI du Manitoba au Canada,
25 patients ayant eu un CCR entre 1995 et 2000
avaient été comparés à 348 sujets contrôles ; il n’y
n’avait pas d’effet bénéfique du 5-ASA sur le risque
de CCR (4). Cette étude avait été critiquée en raison
de la durée limitée des traitements par 5-ASA. Cette
cohorte a été suivie jusqu’en 2008 et l’absence de

La Lettre de l’Hépato-Gastroentérologue • Vol. XV - n° 1 - janvier-février 2012 | 25
EVIDENCE-BASED MEDICINE
MICI
rôle protecteur du 5-ASA a été confirmée dans une
nouvelle étude (5). Ce travail associait, d’une part,
une étude rétrospective qui évaluait l’incidence
du CCR parmi 8 744 patients ayant une MICI − en
comparant les usagers de 5-ASA (≥ 1 fois, ≥ 1 an,
≥ 5 ans, ≥ 7,5 ans cumulés) à des non-usagers −,
d’autre part, une étude cas-témoins évaluant l’expo-
sition aux 5-ASA chez 101 patients ayant eu un CCR
par comparaison avec 303 contrôles. Ces 2 nouvelles
évaluations ne montrent pas d’effet protecteur des
5-ASA, même en excluant les patients sous sala-
zopyrine. L’étude de C.N. Bernstein et al. a le mérite
d’évaluer une large population de patients souffrant
de MICI avec un long suivi prospectif et des préci-
sions sur les doses et les durées de traitement par
5-ASA. La sévérité de la RCH et l’extension de la
maladie qui sont des facteurs de risque reconnus du
CCR n’ont pas été prises en compte dans ce travail.
En conclusion, les données disponibles évaluant le
rôle protecteur des 5-ASA dans le CCR sont contra-
dictoires. Ce sont des études de cohorte et de cas-
témoins qui comportent des biais. La relation causale
n’est pas démontrée. Les malades qui prennent des
salicylés sont peut-être ceux qui ont le suivi le plus
régulier et qui sont les plus attentifs à leurs symp-
tômes et au dépistage par coloscopie.
Références bibliographiques
1. Biancone L, Michetti P, Travis S et al. European evidence-based
consensus on the management of ulcerative colitis: special situa-
tions. J Crohns Colitis 2008;2:63-92.
2. AGA Medical Position Statement on the Diagnosis and mana-
gement of Colorectal Neoplasia in Inflammatory Bowel Disease.
Gastroenterology 2010;138:738-45.
3. Velayos FST, Jonathan P, Walsh JM et al. Effect of 5-aminosa-
licylate use on colorectal cancer and dysplasia risk: a systematic
review and metaanalysis of observational studies. Am J Gastroen-
terol 2005;100:1345-53.
4. Bernstein CN, Metge C, Blanchard JF, Yogendran M. Does
the use of 5-aminosalicylates in infl ammatory bowel disease
prevent the development of colorectal cancer? Am J Gastroenterol
2003;98:2784-8.
5. Bernstein CN, Nugent Z, Blanchard JF. A population-based
study of 5-aminosalicylate use and colorectal cancer in IBD. Am
J Gastroenterol 2011;106:731-6.
Les anti-TNFα diminuent-ils
le recours à la chirurgie dans la RCH ?
J. Filippi (Nice)
U
ne mise au point récemment publiée dans la
revue Current Drug Targets (1) apportera au
lecteur des données exhaustives sur ce sujet
d’actualité. Pour la question qui nous est posée dans
ce numéro spécial, il convient de réduire notre champ
d’exploration aux essais contrôlés randomisés, seuls
essais pouvant satisfaire aux exigences de l’Evidence-
Based Medicine (EBM).
➤
Avant l’ère des biothérapies : les données
concernent uniquement le sous-groupe de patients
présentant une rectocolite hémorragique (RCH)
sévère. En effet, aucune étude n’a évalué le risque de
colectomie à long terme chez les patients atteints
de RCH sans critère de sévérité et traités par dérivés
des 5-aminosalicylés (5-ASA) ou par traitement
immunosuppresseur “classique” (azathioprine,
méthotrexate). L’on dispose donc de données pour
les corticoïdes et la ciclosporine.
Dans une revue récente ayant compilé les résultats
de 32 essais (2 000 patients traités par corticoïdes
pour colite aiguë grave, entre 1974 et 2006), le taux
moyen de colectomie à court terme était de 27 % sans
modification notable sur une période de 30 ans (2).
En situation de corticorésistance, la ciclosporine
a largement été utilisée comme traitement de
secours avant le recours à la chirurgie. Dans l’étude
la plus vaste concernant cette molécule, 73 patients
étaient randomisés pour en recevoir 2 ou 4 mg/kg
par voie intraveineuse. Les taux de réponse à 8 jours
étaient similaires dans les 2 groupes (respective-
ment 82 et 83 %) et les taux de colectomie à court
Les anti-TNF diminuent significativement le recours à la chirurgie dans
la rectocolite hémorragique (RCH) à 1 an, dans les essais randomisés
contrôlés contre placebo.
Dans la vraie vie, environ 1 patient sur 5 atteint de RCH devra bénéficier
d’une colectomie à long terme sous anti-TNF.
En l’état actuel des connaissances, on ne peut recommander la prescrip-
tion d’anti-TNF chez tous les sujets avec RCH afin de modifier l’histoire
naturelle de la maladie.
Ce qu’il faut retenir
niveau
de preuve
1
1
/
2
100%