Place de l’anatomopathologie dans l’évaluation

La Lettre du Sénologue - n ° 39 - janvier-février-mars 2008
Dossier
Dossier
25
Place de l’anatomopathologie dans l’évaluation
de la réponse à la chimiothérapie néoadjuvante
du cancer du sein : marqueurs pronostiques et prédictifs
Place of pathology in evaluation of response after neoadjuvant chemotherapy
in breast cancer: prognostic and predictive markers
IP C. Abrial (1, 2), F. Bouchet-Mishellany (3, 4), I. Raoells (3, 4), A. Cayre (4), H. Curé (5), P. Chollet (1, 2, 3), F. Penault-Llorca (3, 4)
La chimiothérapie néoadjuvante représente une possibili-
té thérapeutique pour les patientes atteintes de tumeurs
mammaires de plus de 3 cm, et donc inaccessibles à un
geste chirurgical conservateur. Cependant, aucune étude n’a
démontré que cette modalité thérapeutique prolongeait la
survie des patientes par rapport à celle des patientes traitées
par chimiothérapie adjuvante (1).
Les objectifs principaux de la chimiothérapie préopératoire
sont la diminution de la taille tumorale pour permettre une
chirurgie conservatrice plus fréquente, l’obtention d’une
meilleure éradication de la maladie micrométastatique par
un traitement précoce avant le développement de clones ré-
sistants alors que le facteur anti-angiogénique (l’angiostatine)
potentiel, sécrété par la tumeur primitive, est toujours pré-
sent, et l’évaluation de la sensibilité des cellules tumorales aux
cytotoxiques administrés.
Le pathologiste joue un rôle majeur dans la prise en charge
optimale des patientes traitées par chimiothérapie néoadju-
vante pour un cancer du sein. En effet, la détermination histo-
pathologique de la réponse au traitement est plus précise que
les méthodes cliniques ou que l’imagerie. De plus, l’histopa-
thologie évaluée après chimiothérapie néoadjuvante peut être
complémentaire des résultats obtenus sur les biopsies initia-
les. Enfin, le pathologiste intervient dans la détermination de
paramètres prédictifs de réponse, dans l’évaluation de la ré-
ponse au traitement, et dans la détermination de paramètres
pronostiques sur le résidu tumoral.
ÉVALUATION HISTOPATHOLOGIQUE DE LA
RÉPONSE À LA CHIMIOTHÉRAPIE NÉOADJUVANTE
Évaluation de la réponse
Lorsque le reliquat est macroscopiquement identifiable, la
taille de la tumeur résiduelle macroscopique est mesurée ainsi
que la distance minimale aux berges en millimètres. La taille
1. Unité de recherche clinique, Centre Jean-Perrin, 58, rue Montalembert, BP 392, 63011
Clermont-Ferrand Cedex 1.
2. INSERM U 484, rue Montalembert, 63005 Clermont-Ferrand Cedex.
3. Université d’Auvergne, faculté de médecine, 28, place Henri-Dunant, 63001 Clermont-
Ferrand.
4. Laboratoire d’anatomopathologie, Centre Jean-Perrin, 58, rue Montalembert, BP 392,
63011 Clermont-Ferrand Cedex 1.
5. Institut Jean-Godinot, 1, rue du Général-Koenig, 51056 Reims.
de ce reliquat tumoral pourra ainsi être comparée à la taille
clinique et/ou échographique initiale.
En cas de reliquat non identifiable macroscopiquement, des
prélèvements en grille systématique de la pièce opératoire se-
ront réalisés pour échantillonner le plus exhaustivement pos-
sible la pièce opératoire. Deux cas de figures sont ensuite pos-
sible : soit un reliquat carcinomateux est identifié et sa taille
sera précisée, soit il n’y pas de reliquat identifiable. Il faudra
rechercher des signes histopathologiques d’altération tissu-
laire témoignant de l’existence, préalable au traitement, d’une
tumeur qui a été stérilisée.
Concernant les ganglions axillaires, ils sont étudiés individuel-
lement et la présence d’un envahissement métastatique ou de
modifications thérapeutiques sont enregistrées.
L’évaluation histopathologique est importante, puisqu’elle
peut permettre aux cliniciens de modifier le schéma théra-
peutique.
Classications histopathologiques de la réponse
à la chimiothérapie
Plusieurs équipes de pathologistes ont proposé des classifi-
cations histopathologiques de la réponse à la chimiothérapie
néoadjuvante. Il faut cependant souligner qu’il n’existe pas, à
l’heure actuelle, de consensus permettant de privilégier une
classification plutôt qu’une autre. Cela complique notable-
ment les comparaisons des taux de réponses complètes his-
topathologiques (RCH) obtenues dans différentes études. Le
tableau résume les différentes classifications qui ont été dé-
crites dans la littérature.
La classification de Feldman (2) est valable seulement sur la piè-
ce d’exérèse mammaire et non sur les ganglions lymphatiques.
Les patientes du groupe A ont une survie sans récidive significa-
tivement plus longue que celles du groupe B. De plus, l’absence
de toute tumeur résiduelle dans la pièce d’exérèse après chimio-
thérapie première est un excellent facteur pronostique.
La classification de Chevallier (3) étudie la réponse sur le sein
et les ganglions lymphatiques. Elle est classique en France et
reste une référence (figures 1a et b ; 2a et b ; 3a et b). Cepen-
dant, la classe 3 englobe une population très hétérogène de pa-
tientes comprenant de très bons répondeurs (pour lesquels le
reliquat est minime et très altéré) et des répondeuses partielles
(qui présentent une régression tumorale de moins de 50 %). Le
grade 2 est considéré comme une rémission complète.

La Lettre du Sénologue - n ° 39 - janvier-février-mars 2008
Dossier
Dossier
26
La classification de Sataloff (4) évalue la réponse sur le tissu
mammaire et sur les ganglions lymphatiques. Cette classifi-
cation est plus proche de la réalité, car elle tient compte de la
viabilité cellulaire. En effet, elle isole un groupe de très bons
répondeurs en prenant en compte les reliquats tumoraux très
nécrosés, non mesurables macroscopiquement, dont la signi-
fication clinique est très proche des répondeurs complets. De
plus, elle stratifie les répondeurs partiels en “bons répondeurs”
(effet thérapeutique supérieur à 50 %) et “mauvais répondeurs”.
Les auteurs ont pu mettre en évidence une survie prolongée
pour les patientes qui présentaient une RCH.
La classification de Viens (5) tient également
compte de la viabilité cellulaire. Elle a été validée
en clinique sur des carcinomes inflammatoires et
ne tient pas compte de la réponse ganglionnaire.
La classification de Honkoop (6) différencie le
groupe de la maladie résiduelle minime du groupe
de la maladie résiduelle macroscopique, qui est
plus hétérogène puisqu’il englobe des répondeurs
et des non-répondeurs. L’évaluation du statut gan-
glionnaire tient compte du nombre de ganglions
envahis (probablement excellent indicateur pro-
nostique en postchimiothérapie), mais ne tient pas compte
d’une éventuelle stérilisation des ganglions.
La classification d’Aberdeen (7) est surprenante, car elle est
indexée à l’opposé des autres classifications. Cependant, elle
est intéressante, car elle isole à la fois les très bons répondeurs
et stratifie les répondeurs partiels.
Les classifications les plus utilisées en France sont celles de
Chevallier (3) et de Sataloff (4). Au Centre Jean-Perrin, nous uti-
lisons également ces deux classifications. En effet, il nous paraît
fondamental de détailler la réponse ganglionnaire, cette derniè-
re est souvent plus faible que la réponse au site initial (8).
Tableau.
Évaluation anatomopathologique de la réponse à la chimiothérapie néo-
adjuvante dans les cancers du sein.
Classication de
Feldman (1986)
Groupe A : absence de tumeur résiduelle macroscopique.
Groupe B : tumeur résiduelle.
Classication de
Chevallier (1993b)
Classe 1 : rémission complète = disparition tumorale complète macroscopique
et microscopique dans le sein et l’aisselle.
Classe 2 : carcinome in situ, pas d’atteinte ganglionnaire.
Classe 3 : carcinome invasif avec altération stromale.
Classe 4 : rares altérations ou absence d’altérations des cellules tumorales.
Classication de
Satalo (1995)
Réponse sur le sein
TA : eet thérapeutique total ou pratiquement total.
TB : eet thérapeutique supérieur subjectivement à 50 %.
TC : moins de 50 % d’eet thérapeutique mais eet évident.
TD : pas d’eet thérapeutique
Réponse ganglionnaire
NA : eet thérapeutique évident, pas de métastases.
NB : pas d’eet thérapeutique, pas de métastases.
NC : aspects d’eet thérapeutique, mais présence de métastases.
ND : pas d’eet thérapeutique, métastases viables.
Classication de Viens
(1998)
Grade I : réponse complète = absence de tumeur résiduelle.
Grade II : bon répondeur = reliquat de carcinome in situ ou tumeur invasive
résiduelle minime de moins de 5 mm ou embole résiduel nécrotique.
Grade III : répondeur partiel = carcinome invasif avec altérations cellulaires
tumorales et/ou stromales.
Grade IV : non répondeur = plus de 75 % de tumeur résiduelle sans altération.
Classication de
Honkoop (1998)
Maladie résiduelle minime
pCR (pathologic Complete Response) : réponse complète.
mPR (microscopic Pathologic Response) : macroscopie normale, rares cellules
néoplasiques dispersées (sein ou ganglions).
Maladie résiduelle macroscopique
Macroscopique
Diuse
Stratication de la réponse ganglionnaire
Pas de métastases
1 à 3 ganglions envahis (N+)
4 à 10 N+
plus de 10 N+
Classication
d’Aberdeen (COSTA
1999)
Grade 1 : aucun changement.
Grade 2 : persistance de foyers tumoraux.
Grade 3 : réduction majeure du nombre de cellules tumorales.
Grade 4 : quelques cellules tumorales résiduelles.
Grade 5 : aucune cellule tumorale identiable
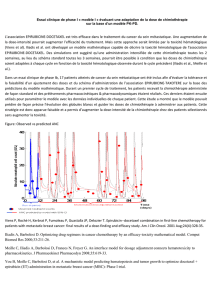
Figures 1a et b.
Biopsie préchimiothérapie
néoadjuvante d’un carcinome canalaire invasif
et pièce chirurgicale postchimiothérapie
néoadjuvante (classe 1 de Chevallier).
a
b

La Lettre du Sénologue - n ° 39 - janvier-février-mars 2008
Dossier
Dossier
27
Discordance entre les taux de réponses cliniques et
histopathologiques
La réponse à la chimiothérapie néoadjuvante est évaluée par
des examens cliniques, mammographiques, échographiques
et anatomopathologiques. Les taux de réponses pathologiques
rapportés s’échelonnent de 3 à 30 % selon les études. Plusieurs
de ces études ont montré qu’il existait un lien entre une ré-
ponse pathologique complète et une survie prolongée et entre
la présence d’un envahissement ganglionnaire axillaire et une
survie plus courte (1).
Les taux rapportés de réponse clinique et de réponse mammo-
graphique sont généralement plus élevés que ceux de réponse
histopathologique. Dans une étude récente, parmi un groupe
de 89 patientes traitées par anthracyclines en préopératoire,
15 (17 %) présentaient une réponse clinique complète dont
seulement 3 avec une réponse histopathologique complète (9).
D’autres travaux aboutissent à des écarts similaires (10-12).
Cependant, quelques études rapportent des taux de réponses
cliniques et pathologiques complètes proches (13, 14). À l’in-
verse, le taux de réponse échographique est souvent corrélé
à celui de la réponse histologique complète (15-17). Il paraît
donc évident que les évaluations échographique et surtout
anatomopathologique sont plus précises.
ÉVALUATION DES FACTEURS PRÉDICTIFS DE LA
RÉPONSE À LA CHIMIOTHÉRAPIE NÉOADJUVANTE
L’évaluation histopathologique des biopsies préthérapeuti-
ques permet de démontrer l’existence de facteurs prédictifs.
Les facteurs évalués sont soit morphologiques (type histopa-
thologique, grade SBR, envahissement ganglionnaire…), soit
immunohistochimiques (récepteurs hormonaux, Her-2, p53,
Cox-2, Ki-67…).
Ces paramètres devraient nous permettre de sélectionner les
patientes qui vont bénéficier de la chimiothérapie néoadju-
vante, et ainsi de ne pas proposer cette approche thérapeuti-
que aux patientes potentiellement non répondeuses.
L’évaluation de la valeur prédictive de nombreux paramètres
établis sur la tumeur mammaire primaire a fait l’objet de nom-
breuses études. Les paramètres morphologiques sont souvent
significatifs. C’est le cas notamment de la taille tumorale. De
meilleurs taux de réponses histopathologiques et/ou cliniques
sont observés pour les tumeurs de petite taille (18, 19). C’est le
cas également du grade histopronostique, du grade nucléaire
et du type histopathologique. C’est ainsi que les tumeurs de
haut grade histopronostique et à fort taux de mitoses sont as-
sociées à de meilleurs taux de réponse (20, 21). Il en est de
Figures 2a et b.
Biopsie préchimiothérapie néoadjuvante
d’un carcinome canalaire invasif et pièce chirurgicale
postchimiothérapie néoadjuvante (classe 3 de Chevallier).
a
b
Figures 3a et b.
Biopsie préchimiothérapie néoadjuvante
d’un carcinome canalaire invasif et pièce chirurgicale
postchimiothérapie néoadjuvante (classe 4 de Chevallier).
a
b

La Lettre du Sénologue - n ° 39 - janvier-février-mars 2008
Dossier
Dossier
28
même pour les tumeurs présentant un grade nucléaire élevé (22).
Concernant le type histopathologique, les carcinomes de type lo-
bulaire présentent des taux de réponse à la chimiothérapie néoa-
djuvante inférieurs aux carcinomes de type canalaire (23, 24).
Ces paramètres présentent, en outre, l’avantage d’être réalisés
systématiquement puisqu’il s’agit des paramètres histopatho-
logiques classiques évalués sur la biopsie initiale.
Les paramètres immunohistochimiques possèdent une valeur
prédictive plus variable. C’est ainsi que la présence de récep-
teurs aux estrogènes est liée à une moins bonne réponse à la
chimiothérapie et, inversement, la négativité des récepteurs
aux estrogènes paraît liée à une meilleure réponse (9, 21). Les
autres facteurs prédictifs, comme les marqueurs de prolifé-
ration, la surexpression d’Her-2, mais aussi les marqueurs de
l’apoptose, semblent moins déterminés.
Les marqueurs de prolifération peuvent être évalués par la
mesure du pourcentage de cellules en phase S ou de cellules
marquées par le Ki-67. D’après certains auteurs, une tumeur
présentant un taux élevé de cellules en phase S n’est pas plus
sensible à une chimiothérapie néoadjuvante qu’une tumeur
ayant un taux plus faible (25, 26). À l’inverse, d’autres équi-
pes montrent qu’il existerait une tendance entre un pourcen-
tage élevé de cellules en phase S et une meilleure réponse à
la chimiothérapie néoadjuvante (27, 28). Concernant le Ki-67,
des taux élevés pourraient prédire une meilleure réponse à la
chimiothérapie néoadjuvante (28, 29). D’autres travaux rap-
portent des résultats contradictoires (26).
Concernant la surexpression d’Her-2, les résultats sont contra-
dictoires. Ainsi, MacGrogan et al. (30) ne retrouvent pas de
valeur prédictive, alors que Rozan et al. (31) concluent à une
tendance prédictive. De plus, dans une étude rétrospective de
Penault-Llorca et al. (32), les tumeurs Her-2+ présentent qua-
tre fois plus de chance de répondre à la chimiothérapie néo-
adjuvante que les autres.
Enfin, concernant les marqueurs de l’apoptose, la plupart des étu-
des ne retrouvent pas de corrélation entre la p53 et la réponse à
la chimiothérapie (26, 31, 33). Seules quelques études rapportent
une résistance des tumeurs p53 aux chimiothérapies à base d’an-
thracyclines (34). L’étude de Makris et al. (26) montre une ten-
dance entre la surexpression de Bcl-2 et la réponse au traitement.
À l’inverse, d’autres ne retrouvent pas cette tendance (34).
Ainsi, les paramètres à déterminer sur la biopsie diagnostique
initiale avant le traitement sont : le type histopathologique,
le grade histopronostique avec le compte des mitoses sur 10
champs au fort grandissement, le statut des récepteurs hor-
monaux, éventuellement le taux de cellules exprimant Ki-67
(selon les équipes) et le statut Her-2 si des protocoles néoad-
juvants avec de l’Herceptin
®
sont envisagés.
ÉVALUATION DES FACTEURS PRONOSTIQUES
L’évaluation de la valeur pronostique de nombreux paramè-
tres a été établie sur la tumeur mammaire primaire, mais éga-
lement sur la pièce opératoire.
En situation néoadjuvante et parmi les paramètres morpholo-
giques, plusieurs études rapportent que la taille clinique ini-
tiale, le statut ganglionnaire initial et le stade tumoral initial
sont prédictifs d’une meilleure survie globale et sans rechute
(11, 35). En revanche, une étude menée dans notre institution
rapporte que le grade SBR, mesuré initialement avant l’admi-
nistration de la chimiothérapie néoadjuvante, ne se révèle pas
pronostique (8).
La chimiothérapie néoadjuvante est souvent proposée à des
tumeurs mammaires de grande taille et de fort grade SBR. Il
s’agit donc, en général, de tumeurs agressives de haut stade, a
priori de mauvais pronostic. Après traitement, si la tumeur a
été sensible à la chimiothérapie, la taille tumorale et le nom-
bre de ganglions envahis vont diminuer. Ainsi, par rapport à
la tumeur initiale, il va exister une sous-stadification clinique
et pathologique du TNM. Malgré cela, la taille histologique
mesurée à la chirurgie et l’envahissement ganglionnaire res-
tent de puissants paramètres pronostiques (8, 11, 15, 36, 37).
Par ailleurs, nous avons montré dans notre institution que la
persistance d’un grade SBR élevé ou son développement sous
traitement est un facteur de mauvais pronostic (20).
De plus, de nombreuses études ont montré l’intérêt pronos-
tique de la réponse complète histologique, à la fois sur le
contrôle local et sur la survie globale.
Sur le contrôle local
Plusieurs études relient la réponse anatomopathologique ob-
tenue en fin de chimiothérapie néoadjuvante et les rechutes
locales : les patientes en RCH présentent moins de rechutes
locales que les autres (38, 39). Dans une étude menée sur des
patientes atteintes de cancer du sein localement avancé, Kue-
rer et al. (18) concluent qu’une RCH prédit une excellente sur-
vie sans rechute, tandis que l’absence de réponse, voire une
progression, induirait une survie sans rechute médiocre. Une
autre étude, réalisée au Centre Jean-Perrin (13), montre que le
taux de survie sans rechute à 15 ans est significativement plus
élevé chez les patientes en RCH que chez les autres.
Sur la survie
L’étude citée précédemment (13) conclut également à une survie
globale significativement meilleure à 15 ans chez les patientes en
RCH par rapport aux autres. La valeur pronostique de la RCH se
retrouve dans d’autres études telles que celle d’Eltahir et al. (40) et
de Bonadonna et al. (11). De plus, dans l’étude de Bonadonna et
al. (11), l’envahissement ganglionnaire résiduel après chimiothé-
rapie est également un indicateur de mauvais pronostic.
Enfin, parmi les paramètres immunohistochimiques, la pré-
sence de cellules fortement prolifératives (pourcentage élevé
de cellules en phase S et surexpression de Ki-67) est un mar-
queur de mauvais pronostic (27, 32). Quelques études réalisées
chez des patientes traitées par chimiothérapie néoadjuvante
sur l’impact pronostique de la surexpression d’Her-2 aboutis-
sent à des résultats controversés : l’équipe de MacGrogan et al.
(30) rapporte une corrélation entre la surexpression d’Her-2 et
la survie, tandis que Rozan et al. (31) n’en retrouvent pas.

La Lettre du Sénologue - n ° 39 - janvier-février-mars 2008
Dossier
Dossier
29
CONCLUSION
Les taux des réponses clinique et histopathologique sont sou-
vent discordants. Les patientes en réponse clinique majeure
présentent, dans la majorité des cas, une tumeur histopatho-
logiquement non stérilisée. Une modification des méthodes
d’évaluation de la réponse histopathologique et le développe-
ment de l’imagerie mammaire fonctionnelle et de l’IRM de-
vraient permettre de réduire cette discordance.
La détermination de la réponse histopathologique à la chimiothé-
rapie est essentielle, car très précise. Le pathologiste a donc un rôle
clé dans l’évaluation du traitement, dont l’objectif primaire est la
réponse pathologique complète. En effet, de nombreuses études
ont montré qu’une RCH était de bon pronostic (11, 13, 40).
De plus, la détermination de paramètres prédictifs sur les
biopsies avant traitement devrait permettre d’améliorer les
taux de réponses observés et donc la survie des patientes.
Enfin, les facteurs évalués après chimiothérapie néoadjuvante
pourront être comparés avec ceux mesurés avant la prise du
traitement et permettront également au pathologiste de gui-
der le clinicien dans la prise en charge thérapeutique optimale
des patientes, pour le choix des cytotoxiques utilisés après le
geste chirurgical et pour la détermination du pronostic de la
tumeur. n
RéféRences bibliogRaphiques
1. Chollet P, Amat S, Mouret-Reynier MA, Curé H. Les bénéfices de la
chimiothérapie néoadjuvante dans le cancer du sein opérable. Oncologie
2002;4:34-7.
2. Feldman LD, Hortobagyi GN, Buzdar AU, Ames FC, Blumenschein GR.
Pathological assessment of response to induction chemotherapy in breast
cancer. Cancer Res 1986;46(5):2578-81.
3. Chevallier B, Roche H, Olivier JP, Chollet P, Hurteloup P. Inflammatory
breast cancer. Pilot study of intensive induction chemotherapy (FEC-HD)
results in a high histologic response rate. Am J Clin Oncol 1993;16:223-8.
4. Sataloff DM, Mason BA, Prestipino AJ, Seinige UL, Lieber CP, Baloch
Z. Pathologic response to induction chemotherapy in locally advanced
carcinoma of the breast: a determinant of outcome. J Am Coll Surg 1995;
180:297-306.
5. Viens P, Penault-Llorca F, Jacquemier J et al. High-dose chemotherapy
and haematopoietic stem cell transplantation for inflammatory breast
cancer: pathologic response and outcome. Bone Marrow Transplant
1998;21:249-54.
6. Honkoop AH, van Diest PJ, de Jong JS et al. Prognostic role of clinical,
pathological and biological characteristics in patients with locally advan-
ced breast cancer. Br J Cancer 1998;77:621-6.
7. Costa SD, von Minckwitz G, Raab G et al. e role of docetaxel
(Taxotere) in neoadjuvant chemotherapy of breast cancer. Semin Oncol
1999;26(3)Suppl.9:24-31.
8. Cure H, Amat S, Penault-Llorca F, le Bouedec G et al. Prognostic va-
lue of residual node involvement in operable breast cancer after induction
chemotherapy. Breast Cancer Res Treat 2002;76:37-45.
9. Faneyte IF, Schrama JG, Peterse JL, Remijnse PL, Rodenhuis S, van de
Vijver MJ. Breast cancer response to neoadjuvant chemotherapy: predic-
tive markers and relation with outcome. Br J Cancer 2003;88:406-12.
10. Belembaogo E, Feillel V, Chollet P et al. Neoadjuvant chemotherapy in
126 operable breast cancers. Eur J Cancer 1992;28A(4-5):896-900.
11. Bonadonna G, Valagussa P, Brambilla C et al. Primary chemotherapy
in operable breast cancer: eight-year experience at the Milan Cancer Insti-
tute. J Clin Oncol 1998;16:93-100.
12. Gradishar WJ. Docetaxel as neoadjuvant chemotherapy in patients
with stage III breast cancer. Oncology (Huntingt) 1997;11(8)Suppl.8:15-8.
13. Chollet P, Amat S, Cure H et al. Prognostic significance of a complete
pathological response after induction chemotherapy in operable breast
cancer. Br J Cancer 2002;86:1041-6.
14. Amat S, Bougnoux P, Penault-Llorca F et al. Neoadjuvant docetaxel
for operable breast cancer induces a high pathological response and
breast-conservation rate. Br J Cancer 2003;88:1339-45.
15. Chollet P, Charrier S, Brain E et al. Clinical and pathological res-
ponse to primary chemotherapy in operable breast cancer. Eur J Cancer
1997;33(6):862-6.
16. Cure H, Charrier S, Ferriere JP et al. First-line chemotherapy in opera-
ble breast neoplasms: results of 3 protocols. Bull Cancer 1997;84(1):31-4.
17. Amat S, Bougnoux P, Penault-Llorca F et al. Neoadjuvant docetaxel
for operable breast cancer induces a high pathological response and
breast-conservation rate. Br J Cancer 2003;88(9):1339-45.
18. Kuerer HM, Newman LA, Buzdar AU et al. Pathologic tumor res-
ponse in the breast following neoadjuvant chemotherapy predicts axillary
lymph node status. Cancer J Sci Am 1998;4:230-6.
19. Pierga JY, Mouret E, Laurence V et al. Prognostic factors for survival
after neoadjuvant chemotherapy in operable breast cancer. e role of cli-
nical response.Eur J Cancer 2003;39:1089-96.
20. Amat S, Penault-Llorca F, Cure H et al. Scarff-Bloom-Richardson
(SBR) grading: a pleiotropic marker of chemosensitivity in invasive duc-
tal breast carcinomas treated by neoadjuvant chemotherapy. Int J Oncol
2002;20:791-6.
L’ensemble des références sera disponible sur le site Internet d’Edimark : http://www.edimark.fr
Vendredi 25 avril 2008 (1 journée) – Des ateliers pratiques de radiologie interventionnelle en sénologie ont été organisés
par le département d’imagerie médicale de l’hôpital Lapeyronie à Montpellier (Pr Patrice Taourel).
Démonstration pratique en petits groupes des techniques de micro- et macrobiopsie sous mammographie, échographie et IRM.
Discussion de stratégie diagnostique à partir de dossiers.
Corrélations radiopathologiques.
Renseignements et inscriptions : Département d’imagerie médicale, hôpital Lapeyronie, 371, avenue du Doyen-Gaston-Giraud,
34295 Montpellier Cedex 5. Tél. : 04 67 33 86 02 – Fax : 04 67 33 89 49. E-mail : p-taourel@chu-montpellier.fr
Droits d’inscription : 200 euros.
 6
6
1
/
6
100%