17/10/2014 SCOTTO DI CARLO Kristel L3 CR: MARIE

SNP – Bases neurophysiologiques des sens chimiques
17/10/2014
SCOTTO DI CARLO Kristel L3
CR: MARIE Claire
SNP
Dr BARTOLOMEI F.
6 pages
Bases neurophysiologiques des sens chimiques
Parmi les différents sens (vision, audition, tact, olfaction et gustation), on en regroupe deux aux propriétés
voisines: l'olfaction et la gustation, aussi appelés sens chimiques.
Les points communs de l'olfaction et de la gustation :
-Stimuli chimiques (odeurs, saveurs) qui vont être à l'origine de la transformation d'un message chimique en
un message nerveux perçu par le cerveau.
-Perception mêlée (ingestion d'aliments puis rétro-olfaction) de ces deux sens.
-Tout deux sont des sens d'alerte mais soumis à un apprentissage important chez l'homme.
Ils possèdent des structures cérébrales communes en particulier au niveau de la perception hédonique1.
Cependant, ils possèdent des systèmes perceptifs différents.
A. Sens du goût
Présent et important dès la naissance (reconnaissance des odeurs et du goût de leur mère).
Le goût évolue avec l'âge, notamment par rapport aux saveurs amères.
Il y a un apprentissage qui se fait tout au long de nos expériences (caractère hédonique des aliments) soumis
aux cultures, époques et moeurs.
La perception gustative est liée à la discrimination de 5 saveurs de base: salé, sucré, acide, amer et Umami
(acide glutamique).
Il existe des récepteurs spécifiques à ces 5 saveurs.
1 Appréciation ou non d'une saveur ou d'un goût perçu.
1/6
Plan
A. Sens du goût
I. Correspondance saveur-chimie
II. Organisation générale
III. Détection des saveurs de base
IV.Transfert vers le SNC
B. Olfaction
I. Organisation générale
II. Épithélium olfactif
III.Transduction des odeurs
IV.Amygdale, olfaction et mémoire émotionnelle
V. Anomalies de la perception olfactive

SNP – Bases neurophysiologiques des sens chimiques
I. Correspondance entre saveur et structure chimique
Salé: NaCl ou autres sels (KCl par exemple)
Acide: Acides
Sucré: sucres (saccharose) mais aussi d'autres molécules n'ayant pourtant pas un structure de sucre (sucres
artificiels tels que l'aspartam)
Amer: ions (K+, Mg2+), quinine, café (800 composants)
⇨ Pas de correspondance chimique particulière
Umami: identifié depuis le XVIIIème siècle, présent dans les viandes, les fromages, les champignons et plus
généralement dans la cuisine asiatique. L'Umami correspond à l'acide glutamique (un des grands
neurotransmetteurs excitateurs).
Ces 5 saveurs de base sont donc capables d'envoyer des stimuli au SNC pour la perception gustative.
II. Organisation générale
La langue, organe du goût
Les papilles gustatives sont chacune composées de 1 à 500 bourgeons gustatifs eux-mêmes formés de 50 à 100
cellules gustatives.
L'information est envoyée depuis ces cellules gustatives jusqu'au système nerveux central.
Les papilles gustatives sont des tubérosités présentes au niveau de la langue. On en distingue 3 types:
–les papilles caliciformes, sur le fond de la langue. Elles sont formées de milliers de bourgeons gustatifs.
–les papilles foliées : 10-300 bourgeons gustatifs
–les papilles fungiformes, plus nombreuses, au devant de la langue et moins sensibles au goût (1-10
bougeons gustatifs)
Aujourd'hui, on considère que toutes les papilles sont capables de percevoir toutes les saveurs.
Les bourgeons gustatifs présentent une structure en oignon qui se finit par un pore faisant émergence au niveau
de la langue. Ils contiennent les cellules réceptrices du goût (50-100): les TRC.
Les TRC (Taste Receptor Cells) sont des cellules allongées d'origine épithéliale (donc différentes des neurones)
associées à des cellules basales moins différenciées qui participent à leur renouvellement tous les 15 jours. Les
TRC sont également en contact avec des terminaisons nerveuses efférentes.
Mécanisme général de la transduction du goût
Une saveur stimule les récepteurs canaux des TRC, ce qui entraîne leur dépolarisation par modification du
potentiel, puis la libération des neurotransmetteurs (sérotonine ou ATP) au contact des fibres nerveuses. Le
potentiel d'action ainsi créé est transporté vers le SNC.
Les cellules TRC possèdent des récepteurs spécifiques aux 5 saveurs de base.
NB: Chaque cellule TRC présente une spécificité de saveur à la différence d'un bourgeon qui possède
plusieurs spécificités.
III. Détection des saveurs de base
2/6

SNP – Bases neurophysiologiques des sens chimiques
a. Détection du salé
Canaux Na+ spécifiques et sensibles à l'amiloride, exprimés dans des cellules TRC spécifiques.
Les cellules TRC sont à peu près toutes capables de répondre à des fortes quantités de sodium, en revanche
certaines cellules spécifiques sont capables de réagir à de faibles quantité de sodium.
Pour les autres saveurs, ce sont des récepteurs transmembranaires couplés à des protéines G activés qui
vont secondairement stimuler les canaux ioniques.
b. Détection de l'acide
Longtemps peu connue, elle fut identifiée par des travaux récents (années 2000). La perception de l'acide est
liée aux protéines transmembranaires PKD 1L3 et 2L1 associées sous forme de dimère.
c. Détection de l'amer
Les substances amères sont détectées par une trentaine de récepteurs T2R différents.
Cette détection est liée aux protéines T2R à 7 domaines transmembranaires dont on connaît une trentaine de
gènes chez l'homme et les souris. Elles peuvent être exprimées dans les mêmes cellules et sont extrêmement
nombreuses dans les cellules détectant l'amer.
Ceci permet une détection puissante, même à très faible concentration, et « non spécifique » de l'amer
(détection poison ++).
d. Détection des saveur sucrée et Umami
Également détectées par des récepteurs assez similaires de la famille T2R, il s'agit de la famille de récepteurs
T1R: T1R1, T1R2, T1R3.
La saveur sucrée est due à des hétérodimères T1R2-T1R3 tandis que la saveur Umami l'est à des dimères T1R1-
T1R3.
IV.Transfert vers le SNC
Une fois que les cellules nerveuses sont dépolarisées, un potentiel d'action est émis et se transfère via 3 nerfs
(VII, IX et X). L'information converge vers le tronc cérébral au niveau du noyau du tractus solitaire, puis dans
le thalamus et enfin dans le cortex gustatif (plusieurs relais sont effectués, notamment dans l'hypothalamus pour
le salé).
Le cortex cérébral est à l'origine de la perception consciente du goût dans l'insula antérieure (5ème lobe du
cerveau enfoui au fond de la vallée sylvienne).
Expérience d'IRM fonctionnel
Absorption un liquide avec un goût → Analyse des zones du cerveau activées pendant des séquences d'IRM
fonctionnel.
Contraste fait entre liquide salé et liquide physiologique par exemple.
Puis observation de l'effet du jugement hédonique → activation de la connexion avec le cortex fronto-orbitaire
en plus de l'activation insulaire (perception primaire du goût).
Le cortex orbitaire est considéré comme un cortex gustatif secondaire.
3/6

SNP – Bases neurophysiologiques des sens chimiques
B. Olfaction
Peut être aussi un système d'alarme (odeurs de fumée, etc.).
Il existe plus de 5 millions de substances odorantes dont 80% seraient perçues comme désagréables.
L'apprentissage est comme pour le goût important. Il s'agit chez l'homme d'un système à 2 neurones ne passant
pas par le thalamus et atteignant directement le SNC (pas de filtre / relais thalamique).
Les molécules odorantes (odeurs) sont des corps chimiques suffisamment volatiles et de petite taille (< 300
Da) pour atteindre le neuro-épithélium olfactif.
Elles possèdent une bonne solubilité dans l'eau pour traverser le mucus et stimuler le cortex nasal.
Structure chimique = Molécules aromatiques et aliphatiques ++
Un grand nombre de molécules peuvent réunir ces conditions; de 10 000 à 20 000 substances sont actuellement
qualifiées d'odorantes.
I. Organisation générale
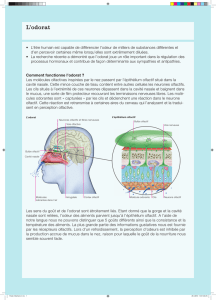
Les molécules rentrent dans les fosses nasales et se fixent au niveau de l'épithélium olfactif sur des récepteurs
spécifiques. La transformation du signal chimique en signal électrique s'effectue et on peut observer l'émission
d'un message nerveux (PA). Celui-ci fait relais au niveau du bulbe olfactif (seul relais) puis est transféré vers le
SNC (cortex olfactifs).
II. Épithélium olfactif
Organe de perception de l'olfaction, il se situe au fond des fosses nasales, dans la partie supérieure. Il est de
l'ordre de 10cm² chez l'homme (soit 10 fois plus petit que chez le chien).
L'épithélium olfactif est fait de 3 types cellulaires : les cellules olfactives réceptrices (COR = neurones), les
cellules basales et les cellules de soutien.
Les COR sont de véritables neurones bipolaires de forme allongée possédant une dendrite au contact du
mucus, un corps cellulaire arrondi et des axones se regroupant avec les autres pour former des filets nerveux
olfactifs qui traversent la lame criblée de l'ethmoïde pour se projeter sur le bulbe olfactif. Les COR meurent et
sont renouvelées toutes les 3 semaines environ par les cellules basales (exception parmi les neurones).
Trauma crânien → fracture ethmoïde → rupture filets nerveux olfactifs → anosmie.
III. Transduction des odeurs
Fixation des odeurs sur leurs récepteurs à 7 domaines transmembranaires au
niveau dendritique (cils).
Nombreuses formes de COR (1 000 gènes connus chez le rat, 350 chez
l'homme).
Chaque COR présente un seul type de récepteur.
L'activation des récepteurs provoque une dépolarisation des cellules (protéines
G) et l'émission de potentiels d'action.
Même si chaque neurone olfactif ne possède qu'un sous-type de récepteur
spécifique, il n'est pas forcément sensible qu'à une seule molécule
odorante.
Chaque cellule olfactive possède son propre récepteur mais une molécule
odorante peut avoir des épitopes en communs avec d'autres odorants et ainsi
activer plusieurs récepteurs. La gamme de réponse peut donc être très variée.
La discrimination des odeurs par le cerveau s'effectue par un décryptage
prenant en compte l'activation d'un type de réponse ou le codage fréquentiel
(entre autres) qui diffèrent selon les odeurs.
4/6

SNP – Bases neurophysiologiques des sens chimiques
Une fois les messages émis par la COR, ils passent par les axones des nerfs olfactifs. Les cellules bipolaires
envoient leurs axones à travers la lame criblée de l'ethmoïde vers le bulbe olfactif pour y faire relais.
Elles y font synapse. La convergence des fibres avec un deuxième neurone relais (cellule mitrale) forme les
glomérules olfactifs. La cellule mitrale va envoyer ses axones à travers le tractus olfactif pour gagner les cortex
olfactifs dans le SNC.
L'information olfactive est ensuite transmise aux cortex olfactifs primaires (lobe temporal interne, amygdale)
relais vers le cortex orbito-frontal (cortex olfactif secondaire).
Projections centrales
Le premier grand relais (cortex olfactif primaire) est la région temporale interne, et en particulier le noyau
cortical de l'amygdale qui reçoit des projections olfactives. Le cortex temporal interne, lui, fait relais vers
l'hippocampe. Une odeur peut donc être à l'origine d'une réactivation de la mémoire.
Cortex temporal interne → projections vers hypothalamus, hippocampe, cortex orbito-frontal.
De même qu'avec la gustation, on peut faire des expériences d'IRM fonctionnels par inhalation d'odeurs.
IV.Amygdale, olfaction et mémoire émotionnelle
L'amygdale peut moduler la consolidation de la mémoire via les connexions avec les cortex impliqués dans la
mémoire: hippocampus, rhinal cortices.
Chez l'Homme: l'atteinte bilatérale des amygdales altère l'apprentissage olfactif et la reconnaissance des odeurs
Les cortex olfactifs secondaires (zones orbito-frontales) sont impliqués dans le jugement hédonique d'une
odeur.
V. Anomalies de la perception olfactive
Dysosmie quantitative:
–l'hypo(o)smie ou anosmie: le patient a une perte partielle ou totale de l'odorat
–l'hyperosmie: perception d'un odorat trop développé
Dysosmie qualitative:
–la cacosmie est la perception d'une mauvaise odeur qui existe réellement à l'intérieur du corps du sujet
(rhume).
–la parosmie est la perception d'une mauvaise odeur déclenchée par la perception d'une molécule
odorante provoquant usuellement une sensation plutôt agréable (déformation de la perception).
–l'hallucination olfactive est la perception erronée d'une odeur (souvent due à l'épilepsie).
Exemples de causes de troubles olfactifs :
Odorat et pathologie rhino-sinusienne (rhinites, …)
Odorat et traumatisme crânien: jusqu'à 25% des TC sévères (globalement 7%) sont source d'anosmie (le plus
souvent irréversibles) ou d'hyposmie sévère
Odorat et vieillissement diminution physiologique de l'odorat
Odorat et toxiques (tabac, cocaïne, radiothérapie, médicaments, …)
Tumeurs cérébrales (base du lobe frontal)
Épilepsie: aura olfactive dans les crises de l'amygdale ou du système orbito-frontal. Cortex olfactif touché →
hallucination olfactive. Parfois associée à une réminiscence de souvenir olfactif (voyage agréable dans le temps
vécu par le sujet).
5/6
 6
6
1
/
6
100%