4ème DM de chimie : Les équations de réaction

4ème DM de chimie : Les équations de réaction NOM : … ………Date :……..
p 1
/25 S’informer Info
/10 Raisonner Rai
/4 Réaliser Réa
/6 Orthographe/phrases complètes
- ……
Modèle particulaire de la matière :
Jusqu’à présent nous nous étions dit que toute matière était constituée de molécules microscopiques
indéformables, insécables, dont la masse ne changeait pas et que dans un corps pur (matière
pure) elles étaient toutes identiques.
Q 1 : Explique pourquoi on ne peut pas expliquer ce qui se passe lors de la combustion
carbone avec le modèle particulaire que l’on connait pour l’instant.
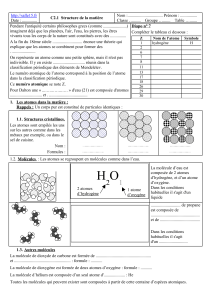
1. Représentation des molécules
Une molécule est en fait constituée de particules plus petites liées entre elles : ce sont les atomes
a "Modèlescompacts"desmolécules
Q 2 : Recopier le tableau de l’ Activité 1 p 60 de votre manuel qui donne le nom, le
symbole et la représentation (« modèle ») des trois atomes dont nous avons besoin
pour expliquer les combustions vues en classe.
Q 3 : Répondre à la question 1. de l’ Activité 1 p 60 .
Q 4 : Dessiner les "modèles compacts" des quatre molécules : Eau, Dioxygène, Dioxyde de carbone,
Méthane.
Respecter les formes et les couleurs des "modèles" des atomes.
b Formuleschimiquesdesmolécules
Pour représenter rapidement une molécule on utilise sa formule chimique.
Lire le "coup de pouce" de la p 60.
La formule chimique de la molécule d’eau est H2O car la molécule d’eau contient 2 atomes d’hydrogène
(notés : H) et 1 atome d’oxygène (noté : O).
Q 5 : Expliquer pourquoi la formule chimique du dioxyde de carbone est CO2 .
Expliquer pourquoi la formule chimique du dioxygène est O2.
Q 6 : Donner la formule chimique du méthane. Justifier votre réponse.
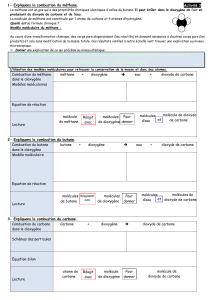
2. Bilan et équation de réaction de la combustion du carbone
En chimie, le bilan littéral d’une transformation chimique est un « résumé ».
Q 7 : Recopier le bilan littéral de la combustion du carbone donné dans l’ Activité 2 p 61.
A gauche de la flèche, des espèces chimiques sont écrites et séparées par un « + ».
Sont-ce les espèces chimiques qui apparaissent ou celles qui disparaissent qui sont
écrites à gauche de la flèche?
A droite de la flèche, est-ce l’espèce chimique qui disparaît ou qui apparaît ?
Le bilan littéral de la combustion du carbone se lit : « Le carbone réagit avec le dioxygène pour former
du dioxyde de carbone. »
Q 8 : Dessiner le "bilan avec les modèles" de l’ Activité 2 p 61.
Q 9 : Répondre aux questions 1 et 2 de l’ Activité 2 p 61.
Q 10 : Que font les atomes des réactifs lors de cette transformation chimique ?
Q 11 : Ecrire l’équation de réaction de la combustion du carbone.
Lire le "coup de pouce" p 61. (Il suffit de remplacer, dans le bilan littéral, les noms des
espèces chimiques par leur formule chimique)
3. Bilan et équation de réaction de la combustion du méthane
Répondre aux 5 questions de l’ Activité 3 p 62.
Orthographe/phrases complètes :
• Plus de 10 erreurs d’orthographe : -0,25 point par erreur supplémentaire.
• Majuscules en début de phrase, sujet, verbe, « phrase commençant par « car » : - 0,25 point.
/1
/1
/3
/4
/2
/1
/2
/2
/1
/2
/1
/5
Rai
Info
Info
Réa
Rai
Rai
Info
Réa
Info
Info
Info
1
/
1
100%