Expériences portant sur les réactions d`estérification, d`hydrolyse

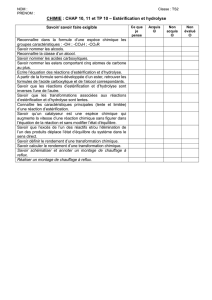
1
Montage n°6
Expériences portant sur les réactions d'estérification,
d'hydrolyse ainsi que sur la saponification des esters
A - Plan du montage
I - Estérification et hydrolyse
[] 1/ L’estérifivcation peut être totale
Synthèse de l’acétate d’isoamyle
[*] 2/ L’équilibre estérification-hydrolyse
Dosages de l’acide acétique après réaction
II - La saponification
[**] Avec la végétaline.
*Cette expérience est issue du fascicule de TP de P. Lalanne
**Cette expérience est issue du Durupty, Term. S

Montage de chimie n°6
2
B - Commentaires
Introduction
Les esters sont des molécules organiques (i.e. contenant du carbone) de formule générale:
R C
O
R'O
Ces molécules sont très présentes dans la nature (arômes, huiles,...). Dans les manipulations qui vont
suivre on va s’intéresser à la synthèse (“estérification”) des esters, à la réaction inverse qui peut être
conduite de deux manières différentes.
I - Estérification et hydrolyse
On va tout d’abord synthétiser un ester que nous connaissons tous: l’acétate d’isoamyle, qui
est un arôme de la banane; on pourra d’ailleurs effectuer la caractérisation “au nez”.
Expérimentalement on utilise du chlorure d’éthanoyle et de l’alcool isoamylique.On ajoute
goutte-à-goutte l’alcool au chlorure d’éthanoyle (qui est dans un erlenmeyer plongé dans un bain
eau-glace). L’alcool doit être en excès. On décante.
On peut aussi synthétiser l’aspirine.
On s’intéresse ensuite à la réaction d’estérification classique avec un alcool et un acide: elle
est lente, athermique et limitée. On va s’intéresser ici à l’aspect “limitée”.
Pour cela on fait deux expériences: dans l’une on part de 1 mol d’acide acétique et 1 mol
d’éthanol; dans la seconde on part de 1 mol d’ester et 1 mol d’eau. On catalyse par 2 gouttes d’acide
sulfurique concentré et on chauffe à 70°C. On monte des réfrigérants à eau pour éviter la vaporisation
de produits et le déplacement d’équilibre. On dose ensuite après trempe l’acide acétique.
Si tout va bien les quantités sont égales.
II - La saponification
On a vu une manière de détruire les esters, par hydrolyse acide. On va maintenant s’intéresser
à une réaction totale, très importante historiquement, puisq’il s’agit de la préparation du savon.
On utilise pour cela une huile naturelle, l’huile de végétaline, qui est un corps gras, un
triglycéride. La saponification de cette huile (hydrolyse en milieu basique) doit donner un savon.
Expérimentalement, on utilise un mélange d’éthanol, de soude décamolaire et d’huile qu’on
chauffe dans un ballon surmonté d’un réfrigérant à eau. Après 15 minutes on relargue dans une solution
saturée de NaCl, on filtre sur büchner et on fait mousser. Attention, le savon synthétisé n’est pas
neutralisé, il ne faut donc pas l’utiliser.
C - Bibliographie
Fiches de TP de P. Lalanne.
Manuel de Term.S, Collection Durupty, Hachette
1
/
2
100%