Revue Cartographie et traitement curatif des fibrillations ventriculaires

Revue
Cartographie
et traitement curatif
des fibrillations
ventriculaires
Mélèze Hocini , Pierre Jais, Frédéric Sacher, Stéphane Garrigue,
Jacques Clémenty, Michel Haissaguerre
Hôpital Cardiologique du Haut Lévêque, avenue de Magellan, 33604 Pessac Cedex
Résumé. La fibrillation ventriculaire (FV) sur cœur apparemment normal représente5à10%
des causes de morts subites. Nous présentons une série de patients avec FV récidivante
idiopathique ou associée à plusieurs substrats dont nous avons pu cartographier les extrasys-
toles ventriculaires déclenchantes et en effectuer l’ablation par radiofréquence. Le nombre
moyen par patient de FV documentée et traitée par un défibrillateur implantable avant
l’exploration est de 10 épisodes ± 14. L’exploration endocavitaire révèle que l’origine des ESV
est dans le muscle ventriculaire « ordinaire » dans seulement 9 cas (infundibulum pulmonaire)
tandis que la majorité des ESV sont initiées par le réseau de Purkinje, soit sur la face antérieure
du ventricule droit, soit dans le ventricule gauche. Le potentiel local de Purkinje précède
l’activation ventriculaire avec un temps parfois considérable atteignant 150 ms. Sept applica-
tions de radiofréquence ont été délivrées en moyenne par patient sur le tissu de Purkinje le plus
distal entraînant l’ablation de l’activité spécifique. Les résultats sur l’état clinique du patient
sont spectaculaires : 88% des patients n’ont plus présenté de FV dont peut témoigner l’analyse
du défibrillateur, avec un recul moyen actuel de plus de 34 mois.
Mots clés : ablation, radiofréquence, défibrillateur automatique implantable, fibrillation
ventriculaire, Purkinje
La meilleure compréhension des
mécanismes d’arythmies a eu pour
conséquence l’émergence de nouvel-
les techniques permettant de cartogra-
phier et guérir par ablation la plupart
des arythmies cardiaques. L’interac-
tion de la « gâchette » initiatrice avec
les facteurs qui perpétuent l’arythmie
(le substrat) est particulièrement im-
portante pour les fibrillations cardia-
ques. Dans les oreillettes, le résultat
est la fibrillation auriculaire (FA),
arythmie soutenue la plus fréquente
chez l’homme, alors que dans les ven-
tricules, la fibrillation ventriculaire
(FV) est le mécanisme le plus commun
lié à la mort subite cardiaque.
La mort subite cardiaque est res-
ponsable approximativement de
50 000 décès par an en France et de
300 000 aux États-Unis [1]. La FV est
le mode le plus fréquent de décès
chez des patients porteurs d’une car-
diopathie mais elle a également été
décrite chez des patients avec des
cœurs structurellement normaux. Jus-
que récemment, la prise en charge des
patients ayant présenté une mort su-
bite cardiaque ressuscitée repose sur
l’implantation d’un défibrillateur
automatique implantable (DAI). En
outre, de larges études cliniques ran-
domisées ont mis en évidence l’avan-
tage de l’implantation prophylactique
de tels dispositifs chez des patients à
haut risque (infarctus du myocarde).
Cependant, cette approche thérapeu-
tique est limitée dans beaucoup de
pays en raison du coût prohibitif. Cela
peut être une cause de morbidité
m
t
c
Tirés à part : M. Hocini
mt cardio, vol. 1, n° 1, janvier-février 2005 47
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 25/05/2017.

importante chez les patients présentant des épisodes fré-
quents ou lors des orages rythmiques.
Mécanismes
de la fibrillation ventriculaire
L’élément initiateur le plus communément observé
dans le déclenchement de la FA est représenté par les
battements ectopiques des veines thoraciques. Analogue
aux mécanismes de la FA, ceux de la FV peuvent être
classés par le mode de déclenchement suite à une gâ-
chette initiatrice et perpétuée par un substrat.
Initiation des fibrillations ventriculaires
Actuellement, ilyadifférentes hypothèses dans le
déclenchement des FV, [2]. La FV peut être déclenchée
par des extrasystoles pendant la période vulnérable du
ventricule, classiquement appelée phénomène « R sur T »
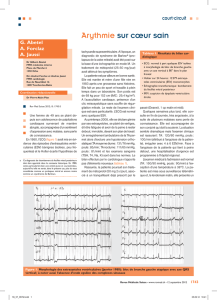
(figure 1). Cela peut correspondre à des post-
dépolarisations tardives ou à des activités déclenchées.
L’importance de cette période vulnérable est certaine
puisqu’elle est utilisée pour l’induction des FV lors des
tests de seuil des défibrillateurs. Cependant, d’autres mé-
canismes ont été proposés car la FV peut se produire sans
phénomène de « R sur T ». Une deuxième hypothèse est
que la FV peut être initiée par une réentrée spontanée
rapide provoquée par l’interaction d’une simple vague-
lette avec un obstacle anatomique fixe qui la brise et
donne ainsi naissance à de multiples vaguelettes qui
s’auto-entretiennent et qui génèrent des activités électri-
ques de haute fréquence [2]. Troisièmement, les phéno-
mènes d’automaticité ou de réentrée ont été décrits dans
les différentes structures qui constituent le ventricule, à
savoir les fibres musculaires elles-mêmes et le tissu de
conduction de Purkinje.
L’implication du système de Purkinje dans le déclen-
chement des FV a été mise en évidence grâce à de nom-
breuses études sur l’animal. Dans le modèle du QT long
(LQT) et de torsade de pointes induits par l’anthropleurine,
El Sherif et al. [3] ont mis en évidence le rôle du réseau de
Purkinje dans le déclenchement de l’arythmie. Janse et al.
[4] ont également souligné le rôle prépondérant du réseau
de Purkinje distal dans le déclenchement des FV ischémi-
ques. Ces études ont mis en évidence la survie de l’arbo-
risation du système de Purkinje même après un infarctus
transmural. Elle est probablement liée au passage passif de
sang oxygéné dans la cavité cardiaque où le réseau de
conduction se situe juste sous l’endocarde [5]. Cependant,
en raison de l’ischémie partielle ou de l’accumulation
loco-régionale des métabolites ischémiques, ces fibres
peuvent développer des propriétés électrophysiologiques
anormales, générant ainsi un potentiel arythmique (phé-
nomène de réentrée, d’automaticité ou d’activité déclen-
chée).
Perpétuation des fibrillations ventriculaires
Basé sur l’hypothèse des réentrées multiples (vaguelet-
tes errantes) proposée par Moe, il est maintenant accepté
que le maintien de la FV soit lié à différentes formes de
réentrée ou de « rotors ». Le rôle des vaguelettes de réen-
trée, unique ou multiple, a été mis en évidence au cours de
simulations informatiques [6], tandis que le « rotor », dé-
fini comme une activité électrique soutenue tournant
autour d’un obstacle fonctionnel, a été démontré par des
études in vitro indépendantes [2, 7].
Figure 1.Télémétrie d’un patient sans cardiopathie avec syncope récidivante montrant des épisodes de TV et de FV polymorphes, déclenchés
par des ESV monomorphes à couplage court (dans la phase descendante de l’onde T).
Revue
mt cardio, vol. 1, n° 1, janvier-février 2005
48
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 25/05/2017.

Traitement curatif
de la fibrillation ventriculaire
L’élimination des éléments déclencheurs et/ou la mo-
dification du substrat perpétuateur est efficace dans le
traitement à long terme des FA. De même, alors que les
déclenchements et/ou le substrat pourraient théorique-
ment être la cible de l’ablation dans les FV, les études
jusqu’à présent ont exclusivement rapporté l’ablation de
l’élément déclencheur. Ceci peut-être le reflet de notre
connaissance limitée du substrat impliqué dans la FV et le
rôle d’une masse plus importante de myocarde [8-16].
Fibrillation ventriculaire idiopathique
La FV sur cœur apparemment normal représente 5 à
10 % des causes de morts subites. Elle est définie d’une
part par l’absence de cardiopathie organique, d’autre part,
par l’absence d’anomalie électrique décelable actuelle-
ment : syndrome du QT long, syndrome de Brugada ou TV
polymorphe catécholergique. La FV idiopathique a
d’autres éponymes dans la littérature : FV récurrente, TV
polymorphe idiopathique, torsade de pointe à couplage
court. Récemment, nous avons présenté une série de
patients avec FV récidivante dont nous avons pu cartogra-
phier les extrasystoles ventriculaires (ESV) déclenchantes
et en effectuer l’ablation par radiofréquence (RF) [11, 12].
Caractéristiques cliniques
Trente-deux patients âgés de 41 ± 14 ans, avec des
épisodes récidivants de FV ont été étudiés. Six d’entre eux
décrivent une histoire familiale de mort subite. Des syn-
copes inexpliquées sont retrouvées chez 17 patients avant
la mise en évidence des FV. La cartographie endocavitaire
a eu lieu dans les2à3jours après les FV. Le nombre de FV
documentée et traitée par un défibrillateur implantable
avant l’exploration est de 9 ± 13 épisodes (5 à 50). Une
moyenne de 3 ± 2 antiarythmiques (classe I, bêtabloqueurs,
amiodarone et vérapamil) a été essayée sans succès.
Les épisodes de FV surviennent durant l’activité jour-
nalière chez la majorité des patients, durant le sommeil
chez certains, mais aucun ne se produit pendant l’effort. Il
s’agit de FV primaire, non précédée de TV monomorphe
initiatrice. L’absence de cardiopathie organique [17] a été
définie par l’examen clinique, l’électrocardiogramme,
l’échocardiogramme, un bilan hémodynamique et coro-
narographique voire par biopsie endomyocardique
(n = 6). Ont été aussi éliminées une dysplasie du ventri-
cule droit, la possibilité de spasme coronarien (test à
l’ergonovine, n = 5) et une TV polymorphe catécholergi-
que par épreuve d’effort ou test à l’isopropyl moradréna-
line (Isuprel
®
). Une administration de classe IC permet
d’exclure un syndrome de Brugada chez 12 patients alors
qu’une recherche génétique sur le SCN5A/HERG est effec-
tuée chez 12 d’entre eux.
Morphologie des extrasystoles ventriculaires
Alors que cette série représente des patients consécu-
tifs, chez tous sauf deux, l’arythmie survient par période
de quelques jours (orage rythmique) au cours desquels
peuvent être documentées ESV, TV polymorphe et FV ; les
arythmies disparaissent ensuite pendant des mois ou an-
nées pour réapparaître soudainement. Dans deux cas, les
extrasystoles ventriculaires sont constamment présentes
sur les enregistrements Holter.
L’examen attentif des ESV sur ECG 12 dérivations
montre qu’elles sont polymorphes (2 ± 1 morphologies
variant de1à5)dans la majorité des cas (66 %), qu’elles
ont un couplage très variable en moyenne de
297 ± 42 ms, et que les couplages les plus courts indui-
sent les TV polymorphes ou FV. Un phénomène R sur T est
observé chez 11 patients tandis que des couplages plus
longs (survenant dans le segment descendant de l’onde T)
sont notés dans les autres cas. Il est enfin noté fréquem-
ment des ESV interpolées.
Trois classes morphologiques d’ESV peuvent être dis-
tinguées :
–des extrasystoles à type de bloc gauche, axe droit
(morphologie infundibulaire provenant du myocarde
commun) chez 5 patients ;
–des ESV provenant de la face antérieure du ventri-
cule droit : aspect de bloc gauche et axe gauche chez 10
patients (provenant du système de conduction distal
droit) ;
–des ESV provenant du ventricule gauche (provenant
du système de conduction distal gauche) puisque positives
dans la dérivation V1 (figure 2) mais avec la caractéristi-
que d’être très fines (durée moyenne 128 ± 18 ms des
complexes QRS contre 145 ± 13 ms dans l’infundibulum
pulmonaire) chez 13 patients ; 4 patients ont à la fois des
morphologies ventriculaires droites et gauches.
Cartographie endocavitaire des ESV initiant
les FV et ablation par radiofréquence (RF)
La cartographie est réalisée au moment où les ESV sont
fréquentes et en phase d’orage rythmique. Deux à 4 cathé-
ters multipolaires introduits via une voie d’abord fémorale
sont utilisés. L’ESV naît du muscle ventriculaire « ordi-
naire » dans seulement 5 cas (infundibulum pulmonaire)
alors que la majorité des autres ESV naissent du réseau de
Purkinje, soit sur la face antérieure du ventricule droit, soit
dans le ventricule gauche (face septale).
Le potentiel distal de Purkinje est défini par la présence
en rythme sinusal d’un potentiel rapide qui précède de
quelques msec (moins de 15 ms) un potentiel plus lent qui
représente l’activation ventriculaire locale. Des temps de
plus de 15 ms reflètent l’enregistrement d’un système de
conduction plus proximal, proche de la branche de
conduction (figure 3). Un potentiel de Purkinje précédant
l’activation ventriculaire locale en rythme sinusal et lors
mt cardio, vol. 1, n° 1, janvier-février 2005 49
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 25/05/2017.

d’une ESV indique son origine du système de Purkinje,
alors que son absence indique une origine musculaire
ventriculaire. La cartographie endocavitaire des ESV re-
trouve un potentiel de Purkinje qui précède l’activation
ventriculaire avec des temps de conduction parfois consi-
dérables atteignant 150 ms. On peut observer des temps
de conduction variables à partir de la même fibre de
Purkinje associés à des morphologies d’ESV différentes,
témoignant de voie de sortie différente. L’observation de
formes répétitives montre que les 3 premières décharges
des TV polymorphes ou FV proviennent aussi du tissu de
Purkinje. Enfin, il peut être observé des impulsions « iso-
lées » du tissu de Purkinje non conduites aux ventricules
(figure 4).
Au site d’ablation, l’activité endocardique précède le
début du QRS sur l’ECG de 130 ± 19 ms. L’ablation peut
provoquer une exacerbation provisoire des ESV qui, dans
certains cas, initie le déclenchement d’une FV en cours
d’examen. Progressivement, en utilisant des applications
d’énergie de RF en moyenne de 13 ± 7 minutes, les ESV
de morphologie différentes sont éliminées. Les électro-
grammes locaux après l’ablation sur le tissu de Purkinje le
plus distal montrent l’abolition de ce potentiel, retardant
légèrement le ventriculaire local. Deux patients ont réci-
divé de leur ESV pendant leur séjour et ont dû subir une
deuxième procédure d’ablation.
Résultats
Après l’ablation, les patients sont suivis sur le plan
clinique et par l’interrogation des mémoires de leur défi-
brillateur. Un patient a présenté une récidive de FV avec
des chocs appropriés documentés, alors qu’un second
patient a présenté une présyncope due à un épisode non
soutenu (6 secondes) de TV polymorphe sans décharge du
défibrillateur. Ces deux patients n’ont pas souhaité béné-
ficier d’une seconde procédure d’ablation. Chez les autres
patients, les enregistrements Holter ne montrent aucune
ou peu d’ESV isolées sur 24 h (28 ± 49 ; variant de 0 à
145). Sur un suivi sans équivoque (attesté par l’interroga-
tion du défibrillateur) de 34 ± 28 mois sans antiarythmi-
que, il n’y a eu aucune mort subite, syncope ou récidive de
FV chez 28 patients (88 %).
Fibrillation ventriculaire :
QT long et syndromes de Brugada
Le syndrome de Brugada et du QT long (LQT) est une
cause connue de mort subite cardiaque. Ces syndromes
sont tous deux associés à des troubles de la repolarisation
ventriculaire [17-19]. Les études récentes suggèrent un
rôle important des ESV naissant du ventricule droit dans le
syndrome de Brugada. Chinushi et al. ont rapporté chez
V1
V2
V3
V4
V5
V6
Figure 2.Tracé de gauche, enregistrement Holter montrant le déclenchement d’une FV idiopathique par une ESV. Notez la fréquence des ESV
juste avant l’épisode de FV. Tracé de droite, enregistrement ECG (dérivations précordiales) du même patient 2 jours plus tard, montrant les
mêmes ESV (morphologie semblable en V5 sur l’ECG et l’enregistrement Holter).
Revue
mt cardio, vol. 1, n° 1, janvier-février 2005
50
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 25/05/2017.

un patient porteur d’un syndrome de Brugada, des épiso-
des récidivants de FV initiés par des ESV monomorphes
(aspect de bloc gauche) [20]. Ceci est corroboré par
Morita et al. [21], qui a observé des ESV chez 9 patients sur
45. Onze morphologies d’ESV sont retrouvées dont 10
d’origine ventriculaire (7 infundibulaires, 2 septales et 1
de l’apex du ventricule droit).
Alors que la prise en charge de ces patients repose sur
l’implantation d’un défibrillateur, ces études et notre ré-
cent succès dans l’ablation des FV idiopathiques [11, 12]
nous a conduit à évaluer le rôle des ESV initiatrices chez
des patients présentant des anomalies de la repolarisation
ventriculaire [15].
Caractéristiques cliniques
Quatre patients avec un syndrome du LQT (2 hommes,
37 ± 8 ans) et 4 patients avec un syndrome de Brugada (3
hommes ; 36 ± 8 ans) ont été explorés. Ces patients ont
présenté des épisodes documentés de TV polymorphe ou
FV (1-21 épisodes). Trois rapportent des antécédents fami-
liaux de mort subite. Les patients porteurs d’un syndrome
de Brugada ont en moyenne 12 ± 9 épisodes de FV, alors
que ceux avec un LQT ont moins d’épisodes (6 ± 4) de FV
ou de syncope.
Un traitement antiarythmique est tenté chez les pa-
tients avec un LQT, notamment les bêtabloqueurs seuls ou
en association avec les classes IC (n = 3), le vérapamil
(n = 2) et l’amiodarone (n = 1). Aucun antiarythmique
n’est essayé chez 3 patients porteurs d’un syndrome de
Brugada alors que la quinidine a échoué chez 1 patient.
Le syndrome du LQT est diagnostiqué chez 4 patients
(intervalle QT corrigé > 460 msec). Aucune anomalie gé-
nétique (KCNQ1, SCN5A et HERG) n’est décelée. Le
diagnostic du syndrome de Brugada repose sur une suré-
lévation en dos de chameau du segment ST en V1 et V2.
Aucune anomalie organique (examen clinique, électro-
cardiogramme, échocardiogramme et coronarographie)
n’est retrouvée chez les patients porteurs du syndrome de
Brugada. Le syndrome du LQT est diagnostiqué au mo-
ment de la FV alors que le syndrome de Brugada est
I
II
III
aVR
aVL
aVF
V1
V2
V3
V4
V5
V6
I
II
III
V1
Purkinje
Branche
proximale
His
Figure 3.Exemple d’une ESV naissant du système de Purkinje ventriculaire droit. Tracé de gauche : ESV typique à type de retard gauche, axe
gauche. Tracé de droite : enregistrement endocavitaire du même patient, montrant le potentiel de Purkinje (flèche) précédant l’activation
ventriculaire locale sur l’électrode distale en rythme sinusal. L’électrode proximale montre un potentiel de branche. Lors de l’ESV, le potentiel
de Purkinje précède toujours mais de façon plus précoce l’activation ventriculaire.
mt cardio, vol. 1, n° 1, janvier-février 2005 51
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 25/05/2017.
 6
6
 7
7
 8
8
 9
9
 10
10
1
/
10
100%