Bulletin du cancer

Bull
<
a:uel
201S:
1C2
:
lSH!9
en
h;"'.t
sur
1
on
I~
on
:.~\·:
.
~f'I"·(?H".~
:
,-
C"''f'
.
·.;,k:
L.J,..'f'
...
.,
...
•.
uc:.c~
r~:
c
~i"
®
Cross
Mark lnhibiteu
rs
de
ALK
de
2e
generation dans le
cancer bronchique non a
peiiies
le;;u;es •
revue de Ia litterature
Ma
ri
e Vi
al
a 1•2,
Solen
n
Bro
sse
au
u,
D
avid
Planchard
4,
Benjamin
Besse
4, je
an-
Ch
ar
le
s
So
ri
a 1•4•5
Re~u
le
24
novembre
2014
Accep
te le 8
h?vrier
201
s
Oisponib
le s
ur
i
nternet
le :
25
mars
20
1S
Mots
cles
can
cer
bronchiq
ue
non
a
pe
tit
es
cellules
AL
K
Crizot
in
ib
Me
c
an
i
smes
de
res
i
stance
ln
hib
iteurs
de
ALK
Ke
y
words
NSCLC
ALK
Cri
zo
tin
ib
AL
K inhibitors
Re
si
st
ance
m
ec
hanis
ms
to
me
102
> n 4 >avril
2015
1. ln
stitu
t G
ustave-Roussy,
departement
d'inno
va
tion
lherapeuti
que
et
d'e
ssais
pr
ecoces,
9480S
Villejui
f,
France
2.
CHU
de
Cl
er
mon
t
-Ferrand,
oncologie
medicale,
6301 1 Cl
ermon
t-
Ferrand
,
Fr
ance
3. CHU
de
Caen,
pneumologie,
14033
Cae
n,
France
4.
ln
stit
ut
Gus
t
ave-Roussy,
depar
te
ment
de
medec
i
ne
oncologique,
9480S
Villejuif,
F
rance
5.
Un
ive
r
site
Paris-Sud,
75011
Par
is,
France
Correspondan
ce
:
j
ea
n
-Cha
rl
es
So
ri
a,
lnstilut
Gustave
-
Roussy,
departement
d'inn
ova
ti
on
the
rap
eutique
et
d'essais
precoces,
11
4,
ru
e
~
dou
a
rd
-Va
illan
t
,
9
480
S
Villeju
if,
Fra
n
ce.
jean-charle
s.so
ria
@
gustave
rou
ssy
.fr
•
Resume
L'i
dentification
du
reman
iem
en
t
EML4-ALK
dans
5 % d
es
ca
n
ce
rs
bronch
i
ques
non
a
pet
it
es
cellu
les
a
permis
le
developpement
ra
pide d'inhibite
ur
s de
ALK
de
1
'e
gene
r
ation
(c
ri
zo
tin
ib)
et a modifie a
Ia
fois
Ia p
rise
en c
harge
et le
pronost
ic de
ces
pati
en
ts
. D
eux
et
ude
s
de
ph
ase
Ill
avec
le
crizotinib
ont
demont
re
so
n effi
cacite
en
2e
li
gne
me
tast
atiq
ue
(PROFIL
E 1007)
et
plus
rec
emment
en
1
'e
lign
e metastati
qu
e
(PROF
IL
E
101
4)
a Ia
foi
s en
term
es
de
surv
ie
sans
progres
-
sion mais au
ss
i
de
r
eponse
obje
ct
ive.
Ce
pendant
,
in
elu
ctab
le
me
nt
dans
l
es
12 a
16
mois
qu
i
su
ivent
so
n intr
oduct
ion, il
est
co
nstat
e un
ec
happ
em
ent
th
e
rap
eut
i
que
du
fait de !
'emerge
n
ce
de
mecanism
es de r
es
ist
ance
su
rvena
nt soit par muta
tion
(L
11
96M)
ou
amp
lifi
cat
i
on
au niv
eau
du
gene
ALK
,
activ
at
ion
d'une
voi
e de si
gnali
s
ation
alterne
(EG
FR
,
KRAS
...
).
De
nouv
ea
ux inhibite
ur
s
d'ALK
de
2e
gene
rati
on
ont ete
deve
l
oppes
do
nt le
ceritinib,
l
'a
l
ectin
ib, et I
'AP
2
6113
.
Ce
tte r
ev
ue
de Ia litt
erature
a
done
p
our
o
bj
ec
tif
de
pr
esen
t
er
ces
no
u
ve
ll
es
mo
l
ec
ul
es
et
leur
niv
ea
u de
developpeme
nt
clinique,
et
de
di
scuter
de
Ia
meilleure
strategie
th
erapeutique
pour
Ia
pri
se
en
charge
du
AL
K+
.
•
Summary
Second
generation
ALK
inhibitors in non-small cell lung c
an
c
er:
Syst
em
ic
r
ev
iew
Th
e
iden
tif
ica
ti
on
of
the
EML4
-AL
K rearrangement in 5% of
NSCLC
e
nhanced
th
e development
of
7
st
generation A
LK
inhibitors
such
as
cri
zotinib.
Two
pho
se
111
tri
als
demons
trated
crizotinib
efficacy
in
second
lin
e
me
t
astatic
(PROFILE
1 007) and
more
recently first line metastatic
(PROFILE
701
4}
NSCLC
in
te
rm
s of progression-f
ree
survival and al
so
obj
ec
t
ive
response
.
How
ever,
wit
hin
Bu
ll
eti
nd
u--
-
CANCER
http./ f
dx
.
doi.org
j
l0
.
10
1
6/j
.
bulcan
.
20
15.
02
.
016
.
<!:>
20
15
societe
fra
n1aise
cfu
cance
r.
Pub
li
e p
ar
Elsevie
r
Masson
SAS.
Ta
us
df
Oits
r
es
erves
.
•
,....
00
IV"\

•
N
00
M
M.
Viala,
S.
Brosseau,
0.
Planchard,
B.
Besse
, J·C
Soria
12
to
16
months,
patients will progre
ss
due
to
th
e
emergence
of
acquired
resistance
mechanisms
such
as
mutation
(L
1796M)
or amplification
of
th
e
ALK
gene,
as well as
ac
tivation of alternative
signaling pathways (
EG
FR
,
KRAS).
Second
generation
ALK
inhibit
ors
hove
been
devel
oped
suc
h
as
ce
ritinib,
olectinib,
and
AP26113.
This
review will
present
th
os
e new
drugs,
summari
ze
the
results
of their
ongoing
trial
s,
and
discus
s
the
bes
t
way
to tr
ea
t
ALK+
NSCLC
patients.
lntrodudion
et
place
du
uizotinib
II
est
des
ormai
s
acquis
qu'
il
exis
te
des
an
oma
li
es
moh~culai
r
es
qu
i
agissent
comme
d
es
acteurs
cles
de
Ia
cr
o
issa
n
ce
tumorale
( « drive
rs
onco
ge
nique
s »)au
se
in
des
cancers
bronch
iqu
es
non
a
petites
cell
ul
es
(CBNPC),
au
premie
r
rang
d
esq
uels Ia
mut
ati
on
du
ge
ne
de
I
'EGFR
et Ia
transl
oca
tion
EML4-ALK.
En
2007,
Soda
et
al.
[1] ont
ra
ppo
rte
!'identification
du
rearra
n-
ge
ment
du
gene
ALK,
Ia partie S'
du
ge
ne
EML4
est
fusionn
ee
a
Ia
partie
3' de
ALK.
La
proteine
de
fusi
on
re
sultant
de
cette
trans
l
oca
ti
on
(EML4-ALK)
a
un
e
ac
ti
vite
kinas
e
en
train
ant
une
cas
ca
de
d'activation impliqu
ee
da
ns
Ia
pr
olife
ration
cellu
l
ai
re
et
Ia
can
ce
rogen
ese
de
ce
s tume
ur
s.
Ce
tt
e
tr
a
nslo
ca
tion
est
retrouvee
dans
env
iron
5 %
de
s
ade
n
o-
carc
in
omes
bron
c
hiqu
es
def
in
issant
un
sous
-
groupe
mo
le
culair
e
p
re
cis (2].
Ce
r
earra
ng
emen
t
ALK
es
t
associ
e a
des
ca
r
ac
te
ri
stiq
u
es
cl
i
nico-
pathol
og
iqu
es
(3].
Pa
rmi
l
es
plus
importantes,
il ta
ut
not
er
:
Ia
faib
le
intoxication t
abagique
(<
10
paque
ts-
annees,
en
gene-
ral
),
l'a
ge
jeune au di
agnos
ti
c,
le type
hi
sto
logiqu
e « ade
no-
carcinome
», Ia pr
ese
n
ce
de
ce
llul
es
en
bague
a cha
ton
, et
l'abs
ence
d
'a
ut
res
moteu
rs
oncogeniques
(4
].
La
determination
du
stat
ut
ALK
se
fait
cl
assiq
uement
pa
r
une
te
chniqu
e d'hybri
dat
i
on
in
situ
(FIS
H)
[5],
elle
es
t int
er
pr
et
ee
pos
itive
si
plus
de
15
% d
es
ce
llu
l
es
pr
esenten
t
le
r
ea
rr
a
ng
e-
ment [6
].
En
pa
ra
llele de Ia
decouverte
de
cette
tr
ans
l
ocation
re
pr
esen
t
an
t
une
verita
ble addiction
oncogeniq
ue [1 ], une petite
mol
e
cule
ora
le
, le crizotinib
eta
it t
este
en
phase
1 en t
ant
qu
'inhibite
ur
de
ty
rosine
k
in
ase
ciblant AL
K,
Met
et
ROS1
(7,8].
L'activ
ite et
Ia
tol
erance
du
cri
zotinib
ont
ete
demontrees
par
Cam
idg
e et a
l.
[9],
chez
l
es
patients
avec
un
carc
in
ome
bronchiq
ue
metasta-
tiq
ue
trans
lo
que
A
LK.
S
haw
et
a
l.
(10], a
tr
avers
l
'etu
de P
RO
FILE
100
7,
etude
de
phase
Ill
rand
om
isee
, ont
compare
le
c
ri
zot
in
ib
, traitem
en
t
ora
l
a Ia
dose
de
250
mg
de
ux
foi
s
par
jo
ur
a
une
chimiothe
rap
ie
sta
ndard
(p
emet
rexe
d
ou
docetaxel)
en
2e
li
gne
chez
d
es
pat
ients
avec
un
cance
r du
poumon
non
a petites
cellu
l
es
l
ocalement
avance
ou
metastatique
porteu
rs
de
Ia t
ransloca
ti
on
EML4-ALK.
Tr
ois
cent
qu
aran
t
e-sep
t patients
ont
e
te
ran
dom
i
ses.
La
su
r
vie
sa
ns
progression
(S
SP)
etait significa
tiv
em
ent
p
lu
s
elevee
d
ans
le
groupe
cr
i
zot
in
ib
par
rapport
au
gro
up
e
chimio-
therapie
(7,7
mois
cont
re 3
mois
respec
tivement). Le ta
ux
de
reponse
o
bj
ec
tive (
RO)
et
ai
t
de
6S
%
dans
le
groupe
cr
i
zo
t
ini
b
contre
seulemen
t
20
%
dans
le
groupe
chimiotherapie.
11
n'a
cependant
pa
s
pu
etre mis
en
evide
nc
e
de
bene
fi
ce
sign
ifi
ca
tif
en
survi
e globa
le
dans
le
groupe
c
ri
zotinib,
ceci
eta
nt lie a
Ia
possibilite
de
cross-over
(p
r
es
de
90
%
des
patien
ts
dans
le
groupe
ch
imio
the
rapi
e ont
re~u
un
traitement
par
cr
izotinib a Ia
progressio
n
).
O'
un
po
int
de
vue
de
Ia
to
ler
an
ce,
le
s
ef
fets
in
desirables
les
plu
s f
requem
m
en
t ret
rouves
eta
ien
t d
es
t
ro
u-
bl
es
de
Ia
vision
(di
ffi
culte
d
'ac
commodat
i
on
, vi
sion
tr
ouble
pe
r
iph
erique,
fl
as
h lumineux), diarr
hee
s,
nause
es,
vomisse
-
ment
s,
constipation,
cedemes,
in
f
ectio
ns
respiratoires
h
autes,
dysgueusie,
vertiges.
Ce
pe
ndant
,
ce
la
co
n
ce
rnait
mains
de
10
%
des
patients de l'
et
ude
et
il
s'
agissa
it
le
plus
souvent
d'
un
g
rade
~
2.
En
revanch
e,
!'el
eva
ti
on
d
es
tr
ansaminases
es
t
un
effet
seco
nd
aire a suivre de
pres
et
pe
ut et
re
de
grad
e 3
ou
4
pour
15
%
des
ma
l
ades.
L
es
r
es
ultats
de
cette
et
ude
ont pe
rmi
s au
crizo
ti
nib
d'obte
nir
so
n A
MM
en
France
en
2013
en
2e
li
gne
ap
r
es
e
ch
ec
d'u
ne
chimioth
era
p
ie
standard
chez
les
pat
ien
ts t
ransloques
ALK
po
ur
un
cance
r du po
um
on
n
on
a petites
ce
llul
es
ava
n
ce
.
P
ar
Ia
sui
t
e,
Mok
et a
l.
[11] ont
compare
le c
ri
zo
tinib a
un
doublet
de
c
hi
miothe
ra
pie sta
ndard
(association
pla
t
ine
et
pemet
r
exed)
en
1'e li
gne
met
astatique
(etude
PRO
FI
LE
10
1
4)
po
ur
des
patien
ts
avec
un
carc
inome
bronch
i
que
sta
de
IV
tr
ans
-
loqu
e
ALK.
L
es
r
es
ultats
ont
ete
presente
s a
I'AS
CO
en
20
14
.
Troi
s
cent
quarante-sept
pa
ti
e
nts
ont
ete
rand
o
mises
dans
l
es
2
bras
.
La
SSP
eta
it
de
1
0,9
mois
dans
le g
roup
e
cr
izotinib
contre
7 m
ois
dans
ce
lu
i chimiotherapie
(p
<
0,0
0
01)
. La r
eponse
o
bj
ec
ti
ve
eta
it r
espec
t
iveme
nt de
74
%
dan
s le
bras
crizotinib
versus
45
% da
ns
le
bras
chimiother
apie
(p
<
0,000
1).
Les
donnees
en s
ur
vie
gl
ob
ale
ne
sont
pa
s
encore
matur
es
me
me
s'
il
es
t
peu
probab
le qu
'e
ll
es
s
oi
ent
sign
ifi
catives
;
en
effet,
un
cross-ove
r
vers
le
crizotinib
etait
poss
ibl
e a Ia
progr
ess
ion
(t
ab
l
eau
1)
.
Cette
e
tu
de
pourrai
t permettre !'obtention
de
I'AMM
pour le
crizotinib
en
1'e
ligne met
asta
tique
dans
ce
tt
e
categori
e
de
pat
ie
nts
.
Ce
pe
nd
ant,
cet
inhibit
eur
de
ty
rosine
ki
nase
es
t
con
fr
onte a
Ia
pr
obl
ema
t
iqu
e
des
met
astases
cerebra
l
es.
Chez
l
es
pa
tients
so
us
cr
izotini
b,
!'app
arit
ion
de met
astases
cerebra
l
es
es
t
fr
e-
quemment
cons
tat
ee
alors
qu
'il
ex
i
ste
un
cont
role de Ia ma
la
-
die,
pa
r
ai
ll
e
ur
s. Dans
un
e e
tud
e re
trosp
ec
ti
ve
in
c
lu
an
t
888
patients,
Cos
ta et a
l.
[12
]
ont
mis
en
ev
id
ence
!'
appa
riti
on
de
met
astases
ce
r
eb
ral
es
chez
20
%des
patien
ts
sous
crizotinib.
La
pe
ne
trat
ion
ce
r
eb
rale
de
Ia m
olecu
le
(13]
et Ia
detection
de
t
aux
faibles
de
c
riz
otinib
dans
le
LCR
[14]
necessiten
t
des
B
ull
eti
n
du--
-
CANCER
lome 1
02
>
n
~
4
> avr
oi
2C
15

lnhibiteurs
de
JI
LK
de 2 • gen
eration
dans le cancer bronchique non a
petites
cellules
:revue
de
I<J
litterature
hBifJIU I
Etudes
de phase
Ill
etudia
nt
le crizotinib versus une chimiotherapie standard
E
tud
es
Lign
e therapeutique
Traitement
Nombre
de
patients
RO
SSP
SG
PROF
I
LE
1
007
[10) 2.
Crizotinib
347
65
%
7,7
mois
·
20,3
mois
vs
docetaxel
ou
pemetrexed
20
o
,u
3
mois
22,8
m
ois
PROFI
LE 1014 [11] 1'.
Crizotin
ib
347
74
0/o
.
10,9
mois
vs
platine
+
pemetrexed
45
O,b 7
mois
RO
:
r~pon~e
ob
j
ec
t
ive
;
SSP
:
surv
ie
sans
progression
;
SG
:
survie
globale
; • : p < 0,05.
investiga
tions
complementaires.
Le
m
eca
n
isme
pri
nc
ipal
res·
ponsable
de
cette
prog
r
ession
cereb
r
ale
reste
inconnu.
Malg
re
de
tre
s
bons
resultats
a
Ia
fo
is
en
s
urvi
e
sa
ns pr
og
r
ession
(SSP
)
et
en
r
ep
on
se
objective
avec
le
crizo
tin
ib,
de
fa~on
in
e·
luctable,
l
es
p
atien
ts
von
t d
ans
Ia
pr
emiere
an
ne
e
echapper
au
traitement.
Ceci
est
dG
au
de
veloppement
de
mecanismes
de
r
esis
tan
ce
connus
[1
5].
Ces
mecanismes
de
r
esistances
p
euvent
etre
div
i
ses
en
2
grou·
pes
: !'apparition d'
une
muta
tion
ou
!'amp
li
fication
du
nombr
e
de
co
pi
e
du
gene
A
LK
,
al
terant
ainsi
Ia
cib
le ; et !'
act
i
va
tion
de
voi
es
de
s
ig
na
li
sations
a
lt
ernes,
l
es
cellules
tum
ora
l
es
pe
rd
an
t
ains
i le
ur
dependance
a Ia
voie
A
LK
(tableau
II
).
A l'heure
ac
tu
e
ll
e,
ces
mutations
acqu
i
ses
on
t
un
e
valeu
r
predict
i
ve
de
resistance
au c
rizot
inib,
mais au
cune
valeur
pronostique
int
rin
seque.
Les
mutations
da
ns
le
domaine
kinase
representent
30
% d
es
mu
tat
ions
seco
nd
aires
[16]. La
mu
tati
on
majeure
es
t
du
e a
Ia
substit
uti
on
d'une l
euc
in
e
par
un
e
me
thi
on
i
ne
en
p
osition
11
96
(L
11
96M)
du
domaine
k
inase
de
ALK,
in
terf
e
rant
avec
Ia
li
aison
du
cr
i
zot
i
nib
s
ur
le
r
ecepte
ur [17].
Cette
mutation
est le pe
ndant
de
Ia
T790M
ch
ez
les
pa
ti
e
nt
s
EGFR
mut
es.
D'autres
mutations
de
res
i
stance
on
t ete identifiees,
elles
aussi
situ
ees
au
niveau
du
doma
i
ne
kinase
du
gene
ALK
tel
que
G
1202R
,
S1206Y,
G
1269A,
T
ABL
EAU
II
M
ecan
ism
es
de resista
nce
se
condaire
au
crizotinib
(NSCLC
ALK
+)
A
LK
d
omi
n
ant
Mutation
secondaire
au
n
ivea
u
du
dom
aine kin
ase
(l11
96M,
C1
1S6Y)
Amplif
ica
tion
du
nombre
de
copie
du
gene
de
f
usion
ALK
(CNG)
A
LK
non
dominant
(voies
al
te
rn
es)
Ac
ti
va
tion
de Ia
voie
EGFR
KRAS
mutations
Amp
li
fi
cation
c-K
IT
tom
e
10
2 ,
n
'
~
,
avr
il 2
01
5
115
1Tin
s,
F11
7
4l
,
L1152R
et
C1156Y.La
preval
e
nc
e et l'impli
ca·
t
ion
cli
nique
de
ces
mutati
ons
do
iv
ent
et
re
plus
amp
le
me
nt
ana
ly
see
s.
L'
autre
mecanisme
concerne
!'ac
ti
vation
de
voies
de
si
gna
lisa-
t
io
ns
altern
es.
L
es
nou
ve
ll
es
voies
de
si
gnalisat
i
on
qui
peuvent
e
tre
impli
quees
dans
Ia r
es
i
stance
au
crizotinib
sont
Ia
vo
ie
de
I'EGFR
,
de
KRAS
ou
enco
re
de
c·K
I
T.
Ces
voies
so
nt
act
i
vees
p
ar
d
es
cell
ules
tumorales
r
esista
nt
es
en
tr
al
nant
un
e proliferation
tumorale
independan
te
malgre
une
inh
ib
iti
on
de
Ia
vo
ie
ALK
.
II
es
t
po
ss
ible de diviser
ainsi
l
es
patients
mut
es
A
LK
resistants
au
crizot
inib en 2
catego
r
ies
:
le
groupe
des
« A
LK
dominan
t »,
rep
resentant
approxima
tiv
ement
46
%
des
cas
et
i
ncl
u
ant
l
es
m
ut
ations
du
domaine
kinase
A
LK
(28
0/o)
et
les
ga
in
s
du
nom-
bre
de
co
p
ies
du
gene
de
fu
sio
n
ALK
(18
%),
et l
es
«
ALK
non
dominant
»,
qui
en
reg
r
oupe
nt
36
%,
i
nc
lu
ant
!'
eme
rg
en
ce
de
voies
alte
rn
es
par
ac
tiv
ation
de Ia
voie
de
I
'EG
FR
, mutation de
KRAS
ou en
core
amplifi
ca
tio
n
du
ge
ne c·KIT[1
8,
1
9].
Ces
facteurs
conferan
t
une
resistance
au
cr
i
zot
inib
peuvent
exis
ter
de
fa~on
independante
ou
pa
rt
ie
ll
ement
dep
e
nda
n
te
du
gene
ALK.
L
es
18
0/o
restant
conce
rn
ent
des
mec
a
nismes
n
on
encore
co
nnus
[
20
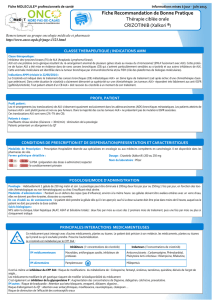
) (figure
1).
Afin
de
de
jouer
ces
mecanismes
de
resistance
ALK
dom
i
nan
t,
de
nouvelles
molecules
dites « inhibit
eurs
de
A
LK
de
2e
gene
r
a-
ti
on » ont ete
deve
l
oppees
a l'
in
star
du
ceritinib
ou
encore
de
l'al
ectinib.
Ces
mol
ec
u
les
sont
en
cours
d'inve
st
ig
at
i
on
a t
rave
rs
des
etu
d
es
clini
que
s.
L'objec
tif
de
ce
tte
revu
e
est
de
presenter
l
es
inhibit
eurs
de
A
LK
de
2e
ge
ne
r
at
io
n a tr
avers
les
differentes e
tu
des
cliniques
r
ea
l
isees
ou
en
co
ur
s,
et
ains
i
de
di
sc
u
ter
par
Ia
su
ite
de
Ia
me
ille
ure
stra
t
egie
th
erapeutique
ch
ez
nos
pati
en
ts
porteurs
d'u
n
adenoca
rc
in
ome
bron
ch
ique
meta
sta
ti
que
tr
ansloque
AL
K.
lnhibiteurs
d'ALK
de
2e generation
Ceritinib
(LDK
378)
Le
cer
itinib
es
t
un
inhibi
teu
r
de
ty
ro
sine
ki
nase
puissan
t et
se
l
ecti
f
cib
l
an
t A
LK
.
Shaw
et
al.
[2
1)
ont
mis
en
evide
n
ce,
a
travers
une
etude
de
ph
ase
1/
11
d'escalade
de
dose
(50
a
750
mg/j), Ia
dose
maxima
le tol
eree
(MTD)
du
ceritinib
a
750
mg
par
jour a
pa
rtir
d'une
co
h
or
te
de
59
patients
.
Soixante
Bull
e
tindu
---
-
CANCER
•
M
00
M

•
M.
Viala,
S.
Bro
sseau,
D.
Pl
anchard,
B.
Besse
,
J·C
So
ri
a
Mutations
in
connues
18%
ALK-/c-KIT+
9%
FI
GU
RE
1
ALK+IKRAS
+9%
ALK mutations
19%
ALKM+
/CNG
9%
Proportion
des
m
ec
anisme
s de resistance au crizotinib
o·apres
Doebele
et
al.
(18
].
et
onz
e
patients
de
plus
ant
ete
indus
dans
Ia ph
ase
d'expan-
sio
n,
soi
t
une
co
horte t
otale
de
130
pat
i
ents.
Cent
quatorze
d
'e
ntre
eux
etaient e
valuables
,
c'est
-
a-dire
avaient
re~u
au
mains
400
mg
de
ceriti
ni
b
par
jour
(79
crizotin
ib-
resistan
ts et
35
na
"if
s)
. La
reponse
objective
de
Ia
cohorte
etait
de
58,5
Ofo,
do
nt
66,3
%chez
l
es
pa
tients
na"ifs
de
crizo
tinib et
54
oro
pour
l
es
pat
ients
resistants.
Ces
reponses
e
tai
en
t vis
ibl
es,
notamment c
hez
les
pa
t
ients
por
te
ur
s
de
Ia
mu
tati
on
de
res
i
stance
l1196M,
mais
ega
lement
ch
ez
des
pa
t
ients
sa
ns
mutation
detectable
. La
SSP
moyenne
e
tai
t
de
8,2
1
mois
, dont 7
mois
ch
ez
l
es
pat
i
ents
pretraites.
Le
p
ro
fil de toxicite
eta
it
marqu
e
par
d
es
diarrh
ees
(8
%Grade
3
ou
4
[G
3 ou 4]},
des
vomissements,
deshydratat
i
on,
cytolyse
hep
a
tique
(1 0 a 19 % G 3
ou
4)
et
hypopho
sp
hor
emie.
La
ges
ti
on
de
ce
tte
hepatotox
icite
(G
3
ou
4)
f
ai
t !'
obj
et
aujour-
d'
hu
i
de
r
ecomma
ndations
prec
i
ses.
En
e
ff
et,
le
tr
aitemen
t p
ar
ce
riti
nib
do
it et
re
inte
rr
ompu
jusqu'a
un
e
resolut
io
n
co
mpl
e
te
ou
G
~
2
de
Ia
cyto
l
yse,
et
reintrodu
it a
un
e d
ose
red
uite
(di
minution
de
150
mg
par
jour).
Pa
r
contre,
si
cette
eleva
tion
des
transaminases
(G
3
ou
4)
s'accompag
ne
d
'u
ne hyperbiliru·
binemie
(> 2
N)
,
le
ceritinib
doi
t e
tre
definitivement
arre
te (22].
L
es
r
esu
l
ta
ts
de
cette
etu
de
de
phase
I
on
t
perm
is
une
appro
b
a-
tion
pa
r Ia
FDA
en
2e
lig
ne
apres
echec
ou
into
l
erance
au
cr
izotin
ib
pour
l
es
patients
ALK
trans
l
oques
.
En
F
rance,
Ia
mole-
cu
le
es
t
di
spon
ible en au
to
ri
sa
tion
tempor
aire
d'utilisation
(ATU)
chez
les
patients
ayant
de
ja
r
e~ u
un
traitement par
crizo
t
inib
.
De
pl
us,
Shaw
et
a
l.
ont
sou
li
gne
a
I'ESMO
2014
[23],
dans
ce
tte
meme
e
tu
de,
l
'e
ffet
du
cerit
inib
sur
les
metastases
ce
r
ebrales
incluan
t
246
pati
ents,
dont
122
eta
i
ent
i
nd
em
nes
de
metasta
·
ses
cerebrales
au
baseline,
et
124
porteurs
de
meta
sta
ses
ce
re
·
b
rales
(2
6
na
"if
s
et
98
aya
nt
re~u
precedemment
un inhibiteur
de
ALK).
La
reponse
objective
eta
it
de
54
%
su
r l
es
lesions
cere
bral
es,
don
t
69,2
%
dans
le
groupe
naH
co
ntre
so
%
dans
le
groupe
pretraite.
La
SSP
et
ai
t
de
6,9
mois;
cec
i dem
ontran
t
une
ac
ti
vite
an
ti-
tum
o
ral
e
cerebrale
du
ce
ri
tinib (taux de
con
tr
6
1e
de
71,4
%}.
D'autres
etu
d
es
so
nt
en
cours
a
fi
n
de
valider
ces
don
n
ees
de
phase
1/11
et
ega
lement de determi
ner
Ia
pla
ce
du
ce
ritinib
dans
!
'arsena
l
therapeut
i
que
des
patients t
ransloq
ues
ALK.
T
ro
is e
tu
-
des
de
pha
se
II
eva
lu
ent
le
c
er
itinib
chez
les
patients crizotinib
re
sistan
ts
(NC
T
01685060
;
NCT02040870)
et
crizoti
ni
b
na"ifs
(NCT01964157).
Deux
etudes
de
phase
Ill
comparent
le
ceri
ti
nib
a u
ne
chimiotherap
ie
sta
n
dard
ch
ez
des patients
por
te
ur
s
d'un
adenocarcinome
bronchique
stade
IV
avec
une
translo
ca
tion
ALK
soit
precede
mm
en
t chimio-traites
(ASCEND-s
NCT0
1828
1
12),
soit en
1'e
lig
ne
versus
une
chimiotherapie
standard
a
base
de
platine
na"ifs
de
tout
tr
a
it
ement
(ASCEND
-4
NCT0
1
828099)
(24].
Auc
un
e
et
u
de,
cependant,
ne
compare
de
maniere
fran
-
tale le ceritinib
au
crizotinib.
Alectinib
L
'alec
tinib
es
t
ega
l
eme
nt
un
i
nh
ibiteur
fort
ement selectif de ALK
(inhibition
10
foi
s p
lu
s
pu
i
ssa
nte
que
le
crizotin
ib
) (25,26].
De
plus,
il
a
un
e
ac
ti
vi
te
contre
Ia
mutation
de
re
sistance
L1196M
;
en
effet, il
peu
t maintenir
une
interac
t
ion
efficace
au
nivea
u
de
Ia
position
1196
meme
apres
Ia su
bstitu
t
ion
d
'une
methi
onine
par
un
e l
eu
cin
e (27] ;
ainsi
que s
ur
d'autres
mu
tations
de
resis
tan
ce
secondaire
tels
que
F1174L
et
R127SQ,
m
ais
ega
l
e-
men
t s
ur
les
forme
s non
mut
ees.
Cependant
,
certaines
mut
a-
tio
ns
tell
es
que Ia G
1202R
con
fe
re
nt
un
fort
niveau
de
r
esistance
a
l'a
l
ecti
nib [28].
U
ne
phase
1
avec
escalade
de
dose
(20
a
300
mg
de
ux
fois
par
jour) a ete
deve
l
op
pee au j
apan
in
eluant
24
patie
nts
precedem-
ment pretrait
es
pa
r chimiotherapie
mais
na"if
s
de
traitement
par
crizot
inib po
ur
un
ade
no
car
cinome
bron
chiq
ue st
ade
IV
po
r
teurs
de
Ia
translocation
ALK
(29].
Aucu
ne
DLT
(Dose
Li
miti
ng
Tox
ic
it
y)
n'a ete ob
ser
vee
tout au
lon
g
de
!
'esca
l
ade
de
dos
e.
La
dose
maximale
to
l
eree
(MTD)
a e
te
de
300
mg
de
ux
lois par
jour,
dose
retenue
pour
Ia ph
ase
II
r
egroupan
t
46
pa
ti
ents.
La
repons
e
object
i
ve
etait
de
93,5
%.
Une
re
pons
e
par
tielle
6
semaines
apres
le
debu
t
du
trait
ement
etait
observee
ch
ez
97%
de
s pa
ti
e
nts
(40
/
46).La
su
rvi
e
sans
prog
r
ession
n'es
t
pas
atteinte a
l'
heure
ac
t
uelle,
mais
elle est
d'au
mains
14
mois
(83
% a 1
an).
De meme
que
le
ceri
t
inib,
l'al
ectinib
semble
avoir
u
ne
activ
ite au
niveau
du
SNC
(sys
te
me
ner
veux
centra
l
).
En
effet,
sur
21
patients
avec
des
m
etas
t
ases
cerebrales
au
baseline
Bu
ll
et
indu
--
-
CANCER
t
ome
1
02
>
;f
4 > avnl
1015

lnhi
biteu
rs
de
AL
K
de
2 •
gene
r
ation
dans
le
cancer
bronchique
non
a
petites
cellules : r
ev
ue
de
Ia litt
era
tur
e
(traitees
ou
non),
19
ont
pr
ese
nte s
ous
traitement
un
e r
epo
n
se
pa
rtie
ll
e (13/21)
ou
stabilite
cerebra
le (6/21).
De
plus,
Ia
tolerance
a
l'
al
ectinib
es
t tout a fait
acceptab
le
avec
comme
effets ind
es
ir
ab
l
es
pr
incipa
ux Ia
dysgueusie
{30
%),
une
a
ugmenta
ti
on
de
s
enzymes
h
epa
ti
qu
es
{28
Ofo)
de
gra
de
::;
2.
De
fa~on
para
ll
e
le,
une
et
ude
americain
e [30)
de
phase
I a
ete
menee
ayant
po
ur
ob
j
ec
tif de
de
terminer
Ia
dose
maxima
le
tol
e
ree
de
l'alectinib
dans
une
population
caucas
i
enne.
Elle
a
i
nclus
47
pati
en
ts
p
or
te
ur
s d'
un
e
tr
an
slocation
AL
K
pou
r
un
adenocarci
n
ome
bronchique
metastatique
crizotinib
resistant.
Aucune
reduc
ti
on
de
dose
n'a
ete
observee
jusqu
'a
600
mg
deux
fois
par
jour, et 2 O
LT
on
t ete
rapportees
a
900
mg
deux
dais
p
ar
jo
u
r.
La
MTD
re
tenue
pour
Ia
ph
ase
II
a
done
ete
de
600
mg
x
2/j.
La
r
epo
n
se
objective etait
de
54,5
%,
so
ul
ig
n
ant
l'activite
de
l
'a
l
ec
ti
nib
meme
chez
le
s patients
resis
tants
au
crizo
ti
nib.
II
est
important
de
no
ter
Ia
difference
de
d
ose
et
don
e d'exposi-
ti
on
en
tre
l
es
pop
ul
at
i
ons
japona
is
es
(30
0
mg
x
2/j)
et
ca
uc
a-
s
ienne
s
(600
mg
x 2/j).
En
effet,
il
es
t
possible
,
com
me p
our
l
es
inhibiteurs
de
I'
EGFR
[3
1 ,32],
que
les
J
apona
is aient
une
sens
ibil
ite
ac
cru
e
tJ
au
medicament
expliq
u
ant
u
ne
eff
icacite
a
une
dose
moindre
par
rapport a Ia
popul
ati
on
c
au
casienne.
T
rois
et
udes
de
phase
I
I/
III
avec
l'alectinib
so
nt en
cours
ch
ez
les
patien
ts
na"ifs
de
traitement p
ar
crizo
tin
ib
(
essa
i
ALEX
NCT020758
4
0)
et
chez
les
patients
res
i
sta
nts au
crizo
t
inib
(NCT
01
8
71
805 ; N
CT0
1
80
1111
). L
es
resultats
de
I'
e
tud
e
ALEX
seront
tres
att
en
dus
car
elle
compare
l'alectinib
au
crizotinib
en
1 re ligne metastat
iq
ue.
Elle
permett
ra
ainsi
de
determiner dir
ec-
tement
si
l
es
inhibit
eu
rs
d'AL
K
de
2e
generation (alectini
b)
sont
plus
eff
icaces
que le
cr
i
zot
ini
b,
et de participer a Ia definition
de
Ia
mei
lleu
re
st
ra
t
egie
th
er
ape
uti
que.
AP26113
L
'AP261
13
es
t
un
nouvel
inh
ibiteur
de
tyr
osine
kinase
inhib
ant
p
ui
ssammen
t l
es
formes mutees
EGFR
et
ALK,
mais
ega
l
ement
les
f
ormes
res
istant
es
aux
TKI
de
1
'e
gen
erat
ion
du
fait d'
une
act
ivite sur
les
mutations
de
res
ist
ances
te
ll
es
que
Ia L
119
6M
du
gene
ALK
et
T790M
de
I'EGFR
(33].
Cam
i
dge
et
al.
[34)
ont
rapporte l
es
resultats
de
Ia
pha
se
1/1
1
ayant
pour
object
if
de
determiner
Ia
dose
de
I'AP
26
1
13
chez
des
patients
po
rteurs
d'un
adenoca
r
ci
nom
e
bronchique
avance
refractaire
a
ux
traiteme
nt
s
standa
rd
, pr
ecedemmen
t
tra
i
tes
par
des
inhibiteurs de A
LK
ou
de
I
'EGFR
.
Quarante-qua
t
re
pat
i
ents
ont
ete
incl
us.
Deux
DLT
ont
ete
rap
p
ortees
a Ia
do
se
de
240
mg
/ j, 2 au
tres
a
300
mg/j.
La
dose
de
300
mg/j
a
done
ete
determinee
pour
Ia
phase
II
d'exte
nsion.
Surles 18 patients
transloque
s ALK
eval
u
ab
l
e,
10
on
t re
pondu
: 2
pat
i
ents
s
ur
3 etaient
na"ifs
de
crizotinib, et 8 s
ur
12
crizot
i
nib
-
resis
t
ant.
Le
taux
de
reponse
objec
tive etait
done
de
67
Ofo
tout
pat
ients
con
fo
ndus
.
Et
Ia survie
Ia
plus
l
ongue
ace
jour etait
de
40
semai-
nes
(en
cours).
lome 102 > o 4 >
avnl
2015
Com
me
le
ce
ritinib
ou
l'alect
inib,
I
'AP26113
a
une
activite
sur
l
es
m
etas
tases
ce
r
eb
ral
es
.
Chez
4 pati
en
ts
sur
5 t
ransloq
u
es
ALK
avec
d
es
me
ta
stases
cere
b
ra
les
au
baseline
(soil
non
traite
es
ou
progre
ss
ives
a
baseline),
il
a
ete
note
une
amelioration
r
ad
iol
ogique.
Le traitement
eta
it
assez
b
ien
tolere
avec
comme
toxicit
es
le
s
plus
frequemment r
apportees
:
les
naus
ees
(4
5 %),
Ia
fa
tigue
(39 %), l
es
diarrhe
es
(27
O
Jo
dont
5 %
de
G 3
ou
4).
Ces
ef
fets
in
desi
r
ab
l
es
etaient le plus
souvent
de
gra
de
::;
2.
Cependant,
il
a
egale
ment
ete
mis
en
evidence
des
react
ion
s
resp
iratoires
p
recoces
(9
%)
a
j1
ou
j2
du
tra
itement
se
tradu
i
san
t
par
une
dyspnee,
d
esaturat
i
on,
oppression
thoraciqu
e.
Ces
sympt6mes
sont
r
eve
rsi
bles.
Le
mecanisme
implique
reste
ace jour
inconnu.
Une
ph
ase
II
d'expansion
est
en
cours
(NC
T
02094573)
com
pr
e-
nant
4
coho
rtes :
ca
n
cers
bronc
hiqu
es
non
a
pe
tit
es
cellu
l
es
transloq
u
es
ALK
c
ri
zotinib-na"ifs
;
crizotinib-res
i
stants
;
EG
FR
mutes
r
es
i
stants
a
une
the
r
apie
ciblant
I'EGFR
,
autres
tumeurs.
Autres
therapies
D'autres
m
ed
ic
amen
ts
de
no
uve
ll
e generati
on
avec
une
activi
te
anti
-ALK
sont en
cours
de
developpemen
t,
tels
que
I'ASP3026
,
T
SR-00
1,
PF-06463922,
X-396
[35). L
es
donnees
co
n
cernant
ces
nouvelles
mo
l
ecu
l
es
sont
r
egro
u
pees
da
ns
le
tableau
Ill.
Discussion
Les
inhib
ite
urs
de
ALK
de 2e
generation
sont-ils
plu
s ef
fic
a
ce
s
que
le
crizotinib
?
Ces
mol
ecu
l
es
ont
montre l
eur
efficacite
sur
l
es
pat
i
en
ts
na"i
fs de
tr
ait
eme
nt
pa
r inhibiteurs
de
ALK,
avec
notamment
pour
l'alec-
ti
nib
des
taux
de
reponse
de
plus
de
93
%,
meme
s'
il
s'agissai
t
d'une
popu
la
ti
on j
aponaise,
et
un
e
SSP
mediane
non en
co
re
atte
in
te
(>
14
mois)
[2
9].
De
meme
pour
le
ceritinib
[21
],
un
e
activi
te
antHumorale
est
clairement
notee
meme
si
cette
de
r-
ni
ere
es
t
mo
i
ndre.
Mais
su
rt
out,
ces
therapeutiqu
es
res
tent
effi
caces
chez
des
pat
i
ents
p
ret
rait
es
par
un
inh
ibiteur
de
ALK
[21,30,34)
avec
des
t
aux
de
reponse
moyens
de
55
%.
En
effet,
ces
nouvea
ux
TK
I ont
une
ac
tivite a
Ia
lois
sur
Ia
fo
r
me
ALK
sauvage,
mais
su
rtou
t
sur
des
mutations
de
resistance
do
nt
Ia
plu
s
frequ
en
te
L 11
96M.
De
pl
us,
Ia
p
ene
tration
de
ces
med
i
came
nts
au
niveau
cerebral
semble
e
tr
e meilleure
que
le
crizotinib,
et
ains
i
ils
ont
un
effet
an
ti
-t
umo
ral
tr
es
inter
essa
nt
sur
les
metastases
cerebrales
;
cec
i
sous-co
uv
ert d'
un
profil
de
t
oxicite
r
ela
t
iveme
nt
acceptable.
Devant
ces
r
esu
ltats
se
pose
Ia
question
de !
'eq
u
iva
l
ence
de
ces
traitements et
imp
licitement
de
Ia
st
r
ateg
ie t
herapeutique.
En
effet,
aucun
resultat
d'etudes
avec
compara
i
so
n «
face
-
a-face
»
n'est
di
spon
ib
le.
Le
t
ableau
IV
r
egroupe
l
es
r
esu
l
tats
des
et
ud
es
de
chac
un
e
de
ces
mol
ec
ul
es
.
Un
debut
de
reponse
sera
apporte
grace
a
une
et
ude
de
ph
ase
Ill
en
cours
(NCT02075840)
comparan
t l'alectinib
au
crizotinib
en
1'
e
ligne
c
hez
les
patients t
rans
l
oques
ALK
pour
un
cancer
Bulletindu
--
-
CANC
ER
•
V\
00
M
 6
6
 7
7
 8
8
 9
9
1
/
9
100%