Résumé sur l`ester -

Résumé sur l'ester
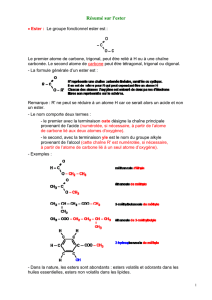
• Ester : Le groupe fonctionnel ester est :
Le premier atome de carbone, trigonal, peut être relié à H ou à une
chaîne carbonée. Le second atome de carbone peut être tétragonal,
trigonal ou digonal.
- La formule générale d’un ester est :
Remarque : R' ne peut se réduire à un atome H car ce serait alors un
acide et non un ester.
- Le nom comporte deux termes :
- le premier avec la terminaison oate désigne la chaîne
principale provenant de l’acide (numérotée, si nécessaire,
à partir de l’atome de carbone lié aux deux atomes
d'oxygène).
- le second, avec la terminaison yle est le nom du groupe
alkyle provenant de l’alcool (cette chaîne R' est
numérotée, si nécessaire, à partir de l’atome de carbone
lié à un seul atome d’oxygène).
- Exemples :

- Dans la nature, les esters sont abondants : esters volatils et odorants
dans les huiles essentielles, esters non volatils dans les lipides.
Synthèse d'arômes : réaction d'estérification r
I ) INTRODUCTION
Les esters apparaissent fréquemment comme composés essentiels dans des substances "odorantes"
( arômes naturels ou artificiels,..).
Chimiquement un ester est le résultat d'une réaction de condensation entre un alcool et un acide
avec départ d'une molécule d'eau suivant l'équation
Estérification :
Réaction chimique conduisant à la formation d'un ester: molécule contenant la
fonction ester - CO - O - R (radical carboné).
¾ acide + alcool ' ester + eau
¾ acide éthanoïque + pentanol ' acétate d'amyle + H2O.
¾ CH3 - CO - OH + C5H11 - OH ' CH3 - CO - O - C5H11 + H2O
Les réactions d'estérification sont généralement lentes et de rendement faible ( L'emploi d'un
catalyseur tel que H2SO4 peut s'avérer utile ).
Alcool Acide Ester
alcool isoamylique acide acétique acétate d'isoamyle

CH3CH(CH3)CH2CH2OH
20 gouttes
CH3COOH
10 gouttes
éthanol
C2H5OH
20 gouttes
acide acétique..
CH3COOH
10 gouttes
acétate d'éthyle
méthanol
CH3OH
15 gouttes
acide salicylique
1 pointe de spatule ( 0,1g )
salicylate de méthyle
éthanol
C2H5OH
8 gouttes
acide butyrique
CH3CH2CH2COOH
10 gouttes
butyrate d'éthyle
alcool benzylique
C6H5CH2OH
12 gouttes
acide butyrique
CH3CH2CH2COOH
10 gouttes
butyrate de benzyle
éthanol
C2H5OH
15 gouttes
acide propanoïque
CH3CH2COOH
20 gouttes
propionate d'éthyle
éthanol
C2H5OH
20 gouttes
acide benzoïque
C6H5COOH
1 pointe de spatule ( 0,4g )
benzoate d'éthyle
Polymérisation : Lorsque plusieurs molécules d'un même composé appelé monomère,
s'additionnent entre elles pour former une molécule unique de grande dimension, appelée
macromolécule, le corps obtenu est un polymère. C'est une polymérisation. Elle nécessite la
présence d'un catalyseur. Les polymères ont de nombreuses utilisations pratiques :
emballages, matériaux de construction, tissu, peinture, matières plastiques, ...
Polyaddition : réaction de formation de polymère sans élimination de molécule.
Polycondensation : réaction de formation de macromolécules mettant en jeu des espèces
chimiques renfermant plusieurs monomères différents au cours de laquelle il y a élimination
de petites molécules telle que :

• L'eau H2O
• L'ammoniac NH3
• Le dihydrogène . H2
• Le méthanol CH3-OH
Le degré de polymérisation est noté n ; c'est le nombre de motifs identiques présents dans la
macromolécule. Il se calcule en divisant la masse molaire moyenne de la macromolécule avec
la masse molaire du motif.
Application aux textiles :
Questions :
L'estérification : définition - équation bilan - application aux textiles. Quelle est la condition
pour que la polymérisation des esters ait lieu ? Est ce une polycondensation ou une
polyaddition, justifiez votre réponse ?
Le TERGAL est un polyester dénommé polytéréphtalate d'éthylène glycol dont le motif est :
-[ OOC - benzène - COO - CH2 - CH2 ]-
Dessiner la forme développée de ce motif.
Dessiner les formules des 2 monomères permettant la polymérisation.
Donner l'équation de cette polymérisation.
Réponses :
Les polyesters sont des thermoplastiques obtenus à partir d'une réaction de polycondensation
entre les fonctions acide et alcool de composés bifonctionnels tels que :
HOOC - benzène - COOH + HO - CH2 - CH2 - OH → -[ OOC - benzène - COO -
CH2 - CH2 ]n- + H2O
Acide phtalique + éthylène glycol → polytéréphtalate
d'éthylène glycol + eau
Ou acide téréphtalique
En réalité la polycondensation l'acide téréphtalique et du glycol ne permet pas
d'obtenir de très longues chaînes. On prépare donc d'abord le téréphtalate de diméthyle. Il
s'agit d'une estérification indirecte qui aboutit à la même macromolécule.

Le polytéréphtalate d'éthylène glycol est commercialisé sous les noms de :
TERGAL en France
DACRON aux USA
TERLANKA en Hollande (Pays Bas)
DIOLEN en Allemagne
TERITAL & WISTEL en Italie.
Pour identifier le polyester par combustion :
A l'approche de la flamme il fond et se rétracte
Dans la flamme il brûle lentement avec fusion
Production d'une fumée noire et une odeur aromatique ou d'amande douce.
Retiré de la flamme il s'éteint
L'aspect des cendres est une boule noire
Action des produits chimiques :
Acides : pas d'action
Bases : leur action n'est pas très bien supportée
Oxydants et solvants : pas d'action.
D'après l'ouvrage "LE VETEMENT" page 20, disponible au CDI sous le n° 59
Repères pratiques Nathan décembre 1998 :
Les polyesters représentent 70 % des fibres chimiques employées dans la confection
des vêtements. Ils sont classés parmi les fibres d'origine synthétique et sont composés de
macromolécules. Le terme polyester peut être utilisé au singulier comme au pluriel.
La fabrication du polyester
A partir de deux carbones d'hydrogène dérivés du pétrole ou de la houille, par des
traitements complexes, on obtient un produit blanc qui est fondu puis filé. La solidification a
lieu par refroidissement.
Le filament obtenu est plat. Pour lui donner douceur, volume et pour améliorer son
élasticité, il va subir une nouvelle opération appelée texturation. S'il existe quatre procédés
appliqués aux polyesters, le principe reste la torsion du fil et sa fixation par la chaleur.
Caractéristiques et usages du Polyester
 6
6
1
/
6
100%