Thérapie génique de la myopathie de Duchenne

Caroline Le Guiner Colloque AFSTAL - Lyon - 25/11/10
Nouvelle thérapie génique
pour la myopathie de Duchenne
Evaluation pré-clinique chez le chien GRMD
et réseau de compétences

• La plus fréquente des dystrophies musculaires (1/3500 naissances de petits garçons)
• Maladie génétique héréditaire liée à l’X : mutation dans le gène codant pour la protéine Dystrophine
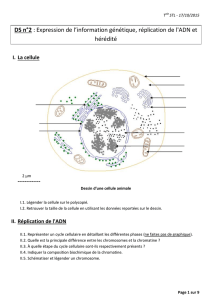
• La Dystrophine est indispensable à l’intégrité des membranes des fibres musculaires
Muscle sain
Dystrophine = ciment du muscle
Muscle myopathe
Absence de Dystrophine
La myopathie de Duchenne

Absence de Dystrophine
Détérioration des fibres musculaires
Affaiblissement progressif des muscles
Mort prématurée (20 à 30 ans)
A ce jour: Pas de thérapie…
La myopathie de Duchenne

La thérapie génique
Comment amener le gène «!sain!» dans la cellule?
Utiliser d’un «!vecteur », viral ou non viral
Gène « sain »
gène muté pas de protéine maladie
protéine fonctionnelle pas de maladie
rAAV = Vecteur dérivé de l’Adéno-Associated Virus

ITR ITR
REP CAP
AAV WT
TRANSGENE THERAPEUTIQUE
rAAV
ITR ITR
AAV WT
L’Adeno-Associated Virus et les vecteurs rAAV
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
1
/
21
100%