Poids et troubles du cycle

36 | La Lettre du Gynécologue • n° 348-349 - janvier-février 2010
Le poids et la gynécologie
DOSSIER
Poids et troubles du cycle
Relation of weight to menstrual disturbances
Brigitte Raccah-Tebeka*, Carole Maître**
U
n cycle menstruel régulier et ovulatoire
découle d’une cascade d’événements
hormonaux d’une précision incroyable
régulée par de très nombreux facteurs, au premier
rang desquels le poids, et particulièrement la masse
grasse, qui joue un rôle essentiel.
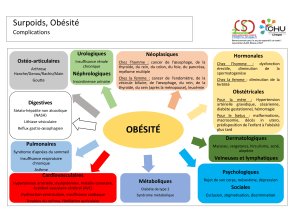
Obésité et troubles du cycle
Depuis de très nombreuses années, une relation
claire a été établie entre obésité et troubles du cycle
à type d’oligoménorrhée ou d’aménorrhée, consé-
quences d’une anovulation chronique responsable
d’une infertilité (1). Plus récemment, une distinction
fondamentale a été mise en évidence entre obésité
gynoïde et obésité androïde. En effet, bien plus que
l’indice de masse corporelle (IMC), la répartition du
tissu adipeux se révèle être le facteur décisif dans la
survenue des anomalies hormonales. Seule l’obésité
androïde est fortement associée au syndrome des
ovaires polykystiques (SOPK) puisqu’elle est présente
dans 30 à 75 % de ces cas selon les études (2). Les
mécanismes selon lesquels l’obésité influence l’ex-
pression du SOPK sont complexes et non totalement
élucidés.
Physiopathologie de la relation
obésité-SOPK
L’obésité en soi représente, chez la femme, une
condition de déséquilibre des hormones sexuelles.
La sex hormone-binding globulin (SHBG), protéine
de transport des hormones sexuelles, diminue linéai-
rement avec l’augmentation de la masse grasse,
entraînant une élévation des fractions libres des
androgènes directement délivrés aux organes cibles
(3). Le taux circulant de SHBG est régulé par de
nombreux facteurs stimulants (estrogènes, iodo-
thyronines, hormone de croissance) et inhibiteurs
(androgènes, insuline). La résultante de ces différents
facteurs en cas d’obésité accorde un rôle prédo-
minant à l’insuline, qui inhibe la synthèse hépa-
tique des protéines de transport. Cet état de fait
se retrouve particulièrement chez les femmes avec
obésité abdominale, qui ont des taux de SHBG plus
bas que les femmes appariées pour l’âge et le poids
(4). L’hyperandrogénie biologique retrouvée dans
les obésités centrales serait également liée à des
taux de production plus élevés avec modification
de la clairance métabolique de certains androgènes,
notamment la DHA et le delta 4-androstènedione.
Du fait de l’activité spécifique des androgènes sur la
morphologie et sur le métabolisme des adipocytes
viscéraux, l’hyperandrogénie pourrait, en retour,
jouer un rôle crucial dans le déterminisme et l’ag-
gravation de l’obésité abdominale. L’importance
du tissu adipeux dans le contrôle et dans l’équilibre
des hormones stéroïdes est, par ailleurs, tout à fait
fondamentale, puisqu’il est à la fois organe de stoc-
kage et lieu d’un intense métabolisme. En effet, de
nombreux enzymes impliqués dans la stéroïdogenèse
(3-bêta déshydrogénase, 17-bêta hydroxydéshydro-
génase et aromatase) y sont présents en quantité
importante.
L’existence d’une obésité maternelle semble pouvoir
être responsable d’une plus grande propension au
développement d’une hyperandrogénie ovarienne
chez la fille à la puberté. Par ailleurs, l’exposition aux
androgènes durant la vie fœtale pourrait favoriser
chez la fille le développement ultérieur d’une obésité,
principalement de type androïde, facilitant l’expres-
sion d’un SOPK (5). Des facteurs métaboliques, au
premier rang desquels l’insuline, interviennent de
façon majeure dans ces interrelations.
L’obésité abdominale est à l’origine d’une insulino-
résistance avec hyperinsulinisme compensateur.
Contrairement à la plupart des tissus cibles (muscle,
foie, tissu adipeux…), qui deviennent insensibles
à l’action de cette hormone, les ovaires y restent
totalement réceptifs par action directe de l’insu-
* Hopital Robert-Debré, 48,
Boulevard Sérurier, 75019 Paris.
** Département médical de l’INSEP,
11, avenue du Tremblay, 75012 Paris.

La Lettre du Gynécologue • n° 348-349 - janvier-février 2010 | 37
Résumé
Le fonctionnement hypothalamo-hypophyso-ovarien et toute la mécanique ovulatoire qui en découle reposent
sur une “bonne santé” physique dont le poids, et plus particulièrement la masse grasse et sa répartition,
constitue un élément déterminant. Toute altération en plus ou en moins est susceptible d’entraîner une
anovulation avec les troubles du cycle et de la fertilité qui s’y rapportent.
Mots-clés
Poids
Troubles du cycle
Keywords
Weight
Menstrual disturbances
line sur ses propres récepteurs ovariens. L’insuline
stimule ainsi la stéroïdogenèse et son excès est à
l’origine d’une hyperandrogénie d’origine thécale.
Cet excédent local d’androgènes est, quant à lui,
responsable d’une atrésie folliculaire prématurée
favorisant l’anovulation (6).
De nombreux facteurs liés à l’excès de tissu adipeux
semblent impliqués dans le développement d’une
anomalie du fonctionnement ovarien. À côté de l’in-
suline, dont le rôle essentiel a déjà été évoqué, il
s’agit des insulin-like growth factor (IGF), du système
endocannabinoïde et de diverses cytokines, au
premier rang desquelles la leptine (7). Produite en
excès par les adipocytes dans l’obésité, la leptine
exerce une action importante dans la régulation de
l’axe hypothalamo-hypophyso-ovarien, en particulier
par l’intermédiaire de récepteurs hypothalamiques
mais aussi ovariens. Au niveau hypothalamique,
elle joue un rôle déterminant dans la pulsatilité du
GnRH. Au niveau périphérique, elle réduirait le taux
d’ovulation en interférant avec le développement
du follicule dominant et la maturation ovocytaire.
Cette action négative sur la fonction ovarienne
semble secondaire à un trouble de la stéroïdogenèse
au sein de la granulosa et des cellules thécales par
opposition probable à l’action de facteurs stimulants
comme l’IGF1, le TGF bêta, l’insuline et la LH (8). Par
ailleurs, il semble exister une relation inverse entre
le taux d’adiponectine et le niveau d’adiposité. Une
diminution de la masse grasse, rétablissant en partie
la sensibilité des adipocytes à l’action de l’insuline,
permettrait une augmentation des concentrations
d’adiponectine. Il existerait, de plus, une action
inhibitrice des androgènes sur la sécrétion d’adi-
ponectine pouvant expliquer les taux très faibles
d’adiponectine en cas de SOPK, indépendamment
de l’obésité. Cette cytokine interviendrait dans la
mécanique ovulatoire par l’intermédiaire de récep-
teurs spécifiques retrouvés dans les cellules de la
granulosa (9).
Le système endocannabinoïde est physiologique
et complexe : il régule les apports alimentaires et
est impliqué dans le stockage et le métabolisme de
la masse grasse. Une suractivation du système est
observée dans l’obésité favorisant au niveau adipocy-
taire une baisse de l’adiponectine du fait d’une plus
grande insulinorésistance. Les cannabinoïdes sont
connus pour diminuer les taux de LH par une action
inhibitrice sur sa pulsatilité. Ainsi, des troubles du
cycle, de l’ovulation et de la fertilité sont courants
chez les utilisatrices de ces substances. Le rôle du
système endocannabinoïde paraît moins clair. Il a
cependant été démontré qu’un de ces médiateurs
voit son taux fluctuer durant le cycle à la fois au
niveau hypothalamique et hypophysaire et qu’un
taux très élevé est retrouvé dans l’ovaire lors de
l’ovulation.
Phénotype du SOPK selon l’obésité
Chez les femmes atteintes de SOPK, l’élévation de l’IMC
favorise la diminution de la SHBG et l’augmentation de
l’hyperandrogénie biologique. Cliniquement, l’hyper-
androgénie et les troubles du cycle sont plus fréquents
chez les femmes obèses que chez les femmes atteintes
du même syndrome mais conservant un poids normal.
De même, les SOPK avec obésité présentent plus volon-
tiers des anomalies métaboliques sévères avec une insu-
linorésistance et un hyperinsulinisme compensateur
plus marqués ainsi qu’une plus grande propension à
l’intolérance au glucose. Le syndrome métabolique y
est plus fréquent qu’en cas de poids normal ; il est défini
comme l’association de trois des items suivants : tour
de taille supérieur à 88 cm, triglycéridémie au-dessus
de 1,7 mmol/l, HDL-cholestérol inférieur à 1,3 mmol/l,
tension artérielle à plus de 135/85 mmHg et glycémie
à jeun supérieure à 6,1 mmol/l. Un IMC supérieur à 25
paraît fortement associé à des anomalies métaboliques
sévères (9).
De nombreuses études ont montré que l’obésité
augmentait la fréquence des anomalies du cycle et
l’infertilité en cas de SOPK. Les troubles de l’ovula-
tion, spontanés mais aussi après traitement, sont plus
courants si la patiente est obèse. Là encore, la réparti-
tion abdominale des graisses joue un rôle clé du fait de
l’altération majeure du métabolisme des androgènes et
de l’insulinorésistance considérable engendrée (10). Tous
les traitements visant à obtenir une réduction pondérale
conséquente permettent fréquemment une restauration
des cycles menstruels avec retour d’ovulations sponta-
nées ou stimulées (11). Mais on constate également que
les mesures conduisant à une diminution de l’insulino-
résistance permettent d’obtenir les mêmes résultats,

38 | La Lettre du Gynécologue • n° 348-349 - janvier-février 2010
Le poids et la gynécologie
DOSSIER
qu’il s’agisse de la mise en place d’un exercice physique
régulier ou de thérapeutiques telles que la metformine.
En fait, toutes les dispositions cherchant à réduire
l’insulinorésistance, et par là même l’hyperinsulinisme,
apportent incontestablement des résultats bénéfiques
sur la mécanique ovulatoire et tout ce qui en découle,
en particulier la régularité des cycles et la restauration
de la fertilité. Les chances de succès des diverses théra-
peutiques sont toutefois meilleurs chez les femmes dont
l’IMC est inférieur à 30 comparativement à celles dont
l’IMC est supérieur à 35 (12).
Sous-poids et troubles du cycle
Le sous-poids se définit par un IMC inférieur à
18,5 kg/m2, mais plus que l’IMC, c’est, là encore, la
composition corporelle et plus précisément le pourcen-
tage de masse grasse, normalement compris entre 25 et
30 % de la masse corporelle chez la femme, qui permet
une approche objective de l’équilibre nutritionnel, et ainsi
de la balance énergétique. Un pourcentage normal de
masse grasse correspond, en dehors d’une pathologie
avérée, à un équilibre de la balance énergétique, et
témoigne d’une dépense énergétique correctement
contrebalancée par les apports nutritionnels.
Poids, masse grasse et déclenchement
pubertaire
En 1974, Frisch et Mac Arthur faisaient l’hypothèse
qu’une valeur seuil de masse grasse était nécessaire
au déclenchement pubertaire et rapportaient dans
leurs travaux la valeur de 17 % de masse grasse (14).
Ce seuil, considéré actuellement comme variable
pour chaque femme, est un élément, parmi d’autres
facteurs génétiques et neuro-endocriniens, du déclen-
chement pubertaire.
Un retard significatif de la puberté de 1 à 2 ans chez
des sportives de haut niveau dans les sports à début
prépubertaire impliquant une minceur (gymnas-
tique artistique, rythmique, patinage) est rapporté
par rapport à une population témoin sédentaire de
même âge (15, 16).
Sous-poids, masse grasse, oligo-
ménorrhée et aménorrhée secondaire
Le lien entre sous-poids – plus précisément masse
grasse insuffisante – et troubles du cycle a été étudié
dans deux tableaux cliniques bien différents : celui
de l’anorexie mentale, et celui des élites sportives
dans les sports d’endurance ou dans les sports dits
esthétiques (patinage, gymnastique rythmique). Les
troubles des conduites alimentaires, l’aménorrhée et
l’ostéoporose ont constitué la triade de la sportive
décrite en 1994 par Nattiv et al. (17).
Une perte de poids corporel de 10 à 15 % par rapport
au poids idéal en fonction de la taille suffit pour
induire des perturbations du cycle. L’aménorrhée
liée à un poids insuffisant concerne 1 à 5 % des
femmes (18).
Les perturbations du cycle correspondent schéma-
tiquement à trois étapes de chronologie successive
et de gravité croissante :
– insuffisance lutéale avec des cycles courts
(< 24 jours) ;
– oligoménorrhée-spanioménorrhée avec des cycles
longs (> 35 jours) ;
– aménorrhée qui peut être présente d’emblée si le
déficit énergétique est chronique, important, avec
une masse grasse très faible (cas des anorexies
sévères, sportives de haut niveau où le morpho-
type filiforme est recherché) ; – à chaque étape, une
anovulation peut être présente ou non.
Miller et al. (19) ont étudié 116 femmes souffrant
d’anorexie mentale, définie par le DSM IV ; 74 étaient
en aménorrhée et 42 en euménorrhée : les deux
groupes étaient semblables pour l’IMC, l’âge de
la puberté, l’ancienneté de l’anorexie et l’activité
physique, la seule différence significative étant le
pourcentage de masse grasse, qui était plus élevé
chez les euménorrhéiques en dépit d’un poids faible
semblable, avec une masse grasse viscérale plus
importante mesurée par le scanner Dexa.
Dans une étude contrôle concernant des élites
sportives norvégiennes (n = 669) versus une popu-
lation sédentaire de même âge (n = 607), Torsveit
et Sundgot-Borgen (16) retrouvent une fréquence
plus grande de troubles du cycle dans les sports où le
pourcentage de masse grasse est plus faible (endu-
rance et sports esthétiques, sports à catégories de
poids) par rapport aux autres sports (sports d’équipe,
sports techniques) et par rapport aux sédentaires.
Les troubles du cycle des sportives n’étaient pas
plus fréquents lorsque l’entraînement concernait le
quartile supérieur, ce qui suggère fortement que ce
n’est ni l’intensité, ni le volume d’entraînement, ni
le stress qui est responsable de la perturbation des
cycles mais une composition corporelle avec une
masse grasse et des apports énergétiques insuffisants
en regard de la dépense énergétique.
Références
bibliographiques
1. Rogers J, Mitchell GW. The
relation of obesity to menstrual
disturbances. N Eng J Med 1952;
247:53-5.
2. Ehrmann DA. Polycystic
ovary syndrome. N Eng J Med
2005;352:1223-36.
3. Pasquali R, Gamberini A. Poly-
cystic ovary syndrome: a multifa-
ceted disease from adolescence
to adult age. Ann NY Acad Sci
2006;1092:158-74.
4. Pasquali R, Vicennati V, Pagotto
U. Endocrine determinants of
fat distribution. Handbook of
obesity. New York: M Dekker, Inc,
2003:671-92.
5. Abbott DH, Dumesic DA,
Franks S. Developmental origin
of polycystic ovary syndrome:
a hypothesis. J Endocrinol
2002;174:1-5.
6. Porestky L, Cataldo NA,
Rosenwaks Z, Giudice LC. The
insulin-related ovarian regula-
tory system in health and disease.
Endocr Rev 1999;20:535-82.
7. Mitchell M, Armstrong DT,
Robker RL, Norman RJ. Adipo-
kines: implications for female
fertility and obesity. Reproduction
2005;130:583-97.
8. Agarwal SK, Vogel K, Weitsman
SR, Magoffin DA. Leptin anta-
gonizes the insulin-like growth
factor-1 augmentation of
steroidogenesis in granulosa
and theca cells off the human
ovary. J Clin Endocrinol Metab
1999;84:1072-6.
9. Ledoux S, Campos D, Lopes F,
Dobias-Goff M, Palin MF, Murphy
B. Adiponectin induces periovu-
latory changes in ovarian folli-
cular cells. Endocrinology 2006;
147:5178-86.
10. Cupisti S, Kajaia N, Dittrich
R, Duezenli H, Beckmann MW,
Mueller A. Body mass index and
ovarian function are associated
with endocrine and metabolic
abnormalities in women with
hyperandrogenic syndrome. Eur
J Endocrinol 2008;158:711-9.
11. Pasquali R, Gambineri A,
Pagotto U. The impact of obesity
on reproduction in women with
polycystic ovary syndrome. BJOG
2006;113:1148-59.
12. Norman RJ, Noakes M, Wu
R, Davies MJ, Moran L, Wang JX.
Improving reproductive perfor-
mance in overweight/obese
women with effective weight
management. Hum Reprod
Update 2004;10(3):267-80.

La Lettre du Gynécologue • n° 348-349 - janvier-février 2010 | 39
DOSSIER
Physiopathologie des troubles du cycle
Le dénominateur commun retrouvé dans ces diffé-
rents tableaux cliniques est une balance énergétique
négative et un faible pourcentage de masse grasse.
La réserve énergétique est mobilisée pour maintenir
la balance énergétique : une valeur seuil de réserve
énergétique disponible est nécessaire pour des cycles
réguliers ; en dessous de 25-30 kcal/kg de masse
maigre par jour, le cycle menstruel est suspendu (20).
L’hormone clé qui relie le déficit énergétique à l’axe
hypothalamo-hypophysaire ovarien est la leptine,
peptide sécrétée essentiellement par le tissu adipeux :
son taux plasmatique s’élève progressivement durant
la puberté et en est un des éléments initiateurs (21).
Hilton et Loucks (22) ont montré que le taux plas-
matique de leptine était plus bas chez les femmes
sédentaires carencées en apport alimentaire que chez
les femmes non carencées, et qu’il était plus bas chez
les athlètes en déficit énergétique par rapport aux
sédentaires, le taux étant corrélé au pourcentage de
masse grasse. Au maximum, en cas d’aménorrhée, il y
a une disparition du cycle de sécrétion nycthémérale
de la leptine. L’étude contrôle de Miller (19) confirme
ces données en retrouvant un taux de leptine signifi-
cativement plus bas dans la population anorexique en
aménorrhée, par rapport à la population anorexique
en euménorrhée.
La sécrétion de leptine est directement corrélée à la
masse grasse et diminue avec le volume des adipo-
cytes : une quantité moindre de triglycérides pourrait
induire une diminution de l’expression du gène Ob
dans la cellule adipeuse. Elle est également corrélée
au taux d’insuline, qui favorise son expression et sa
sécrétion (20).
Un bilan énergétique déséquilibré, quelle qu’en soit
la cause (anorexie mentale, dépense énergétique
accrue, malnutrition des pays en développement),
avec une chute de poids de 10 %, entraîne une baisse
de la leptine de 55 %. Or, des récepteurs à la leptine
sont présents sur l’hypothalamus, l’hypophyse et les
ovaires, et d’autres organes périphériques qui sont
impliqués dans la fertilité et la reproduction (endo-
mètre, placenta, glandes mammaires).
La baisse de leptinémie entraîne ainsi un ralentis-
sement de l’axe gonadotrope, un ralentissement
de la pulsatilité de la GnRH avec, en cascade, un
ralentissement et une diminution d’amplitude de
la sécrétion de LH et une sécrétion plus faible de
FSH, et enfin une diminution des stéroïdes sexuels.
L’administration exogène de leptine ne restaure les
cycles qu’en présence d’une disponibilité suffisante en
glucose. La leptine joue son rôle de médiateur, sous
la dépendance du couple insuline-glucose.
D’autres mécanismes sont en jeu comme la baisse
de l’IGF-1 qui stimule in vitro la GnRH et le relargage
de LH. Par ailleurs, une balance énergétique négative
ralentit l’action stimulatrice du neuropeptide Y sur
la sécrétion de GnRH (19, 23).
Effets sur la fertilité
Un retour des cycles lié à un équilibre des apports
nutritionnels (anorexie, boulimie, sport de haut
niveau) ou à une baisse des dépenses énergétiques
(sports de haut niveau) est indispensable à une ferti-
lité normale. Le retour des cycles ovulatoires peut
être décalé dans le temps par rapport à la reprise
du poids normal, mais à long terme, en l’absence
d’aménorrhée persistante, la fertilité ne semble pas
diminuée (23). Celle-ci paraît être très influencée par
l’homéostasie pondérale et le maintien d’une masse
grasse suffisante et sans excès.
Conclusion
Les troubles du cycle consécutifs à une obésité ou à
un sous-poids sont réversibles. Les moyens thérapeu-
tiques visant à la restauration d’un équilibre pondéral
satisfaisant permettent, le plus souvent, d’aboutir à
un retour de cycles ovulatoires avec amélioration de
la fertilité. ■
Références
bibliographiques
13. Raush ME, Legro RS, Barnhart
HX et al. Predictors of pregnancy
in women with polycystic ovary
syndrome. J Clin Endocrinol Metab
2009;94(9):3458-66.
14. Frisch RE, McArthur JW.
Menstrual cycles: fatness as a
determinant of minimum weight
for height necessary for their
maintenance or onset. Science
1974;185:949-51.
15. Klentrou P, Plyley M. Onset
of puberty, menstrual frequency,
and body fat in elite rhythmic
gymnasts compared with normal
controls. Br J Sports Med 2003;
37:490-4.
16. Torsveit MK, Sundgot-Borgen
J. Participation in leanness sports
but not training volume is asso-
ciated with menstrual dysfunction:
a national survey of 1 276 elite
athletes and controls. Br J Sports
Med 2005;39:141-7.
17. Nattiv A, Agostini R, Drin-
kwater B, Yeager KK. The female
athlete triad. The inter-rela-
tedness of disordered eating,
amenorrhea, and osteoporosis.
Clin Sports Med 1994;13(2):405-
18.
18. Laughlin GA, Yen SS. Hypo-
leptinemia in women athletes:
absence of diurnal rhythm with
amenorrhea. J Clin Endocrinol
Metab 1997;82:318-21.
19. Miller KK, Grinspoon S,
Gleysteen S et al. Preservation of
neuroendocrine control of repro-
ductive function despite severe
undernutrition. J Clin Endocrinol
Metab 2004;89(9):4434-8.
20. Thong FS, McLean C, Graham
TE. Plasma leptin in female
athletes: relationship with body
fat, reproductive function and
endocrine factors. J Appl Physiol
2000;88:2037-44.
21. Koutkla P,Canavan B, Johnson
ML, De Paoli A, Grinspoon S.
Characterization of leptin pulse
dynamics and relationship to fat
mass, growth hormone,cortisol
and insulin. Am J Physiol Endo-
crinol Metab 2003;285:372-9.
22. Hilton LK, Loucks AB. Low
energy availibility, not exercice
stress, suppresses the diurnal
rhythm of leptin in healthy young
women. Am J Physiol Endocrinol
Metab 2000;278:E43-9.
23. ESHRE Capri Workshop Group.
Nutrition and reproduction in
women. Hum Reprod Update
2006;12(3):193-207.
Abonnez-vous en ligne !
Bulletin d’abonnement
disponible page 29
www.edimark.fr
1
/
4
100%