de l`inhibiteur de protéase au médicament contre l`hépatite C

Journal Identification = VIR Article Identification = 0476 Date: February 19, 2013 Time: 1:0 pm
éditorial
Virologie 2013, 17 (1) :3-5
Le télaprévir : de l’inhibiteur de protéase
au médicament contre l’hépatite C
Line Bourel-Bonnet1
Esther Kellenberger2
1Université de Strasbourg,
faculté de pharmacie,
UMR7199,
74, route du Rhin,
67401 Illkirch,
France
2Université de Strasbourg,
faculté de pharmacie,
UMR7200/MEDALIS Drug Discovery
Center,
74, route du Rhin,
67401 Illkirch,
France
L’hépatite C constitue un enjeu majeur de santé publique. Cette mala-
die infectieuse provoquée par le virus de l’hépatite C (VHC) est une
cause majeure de cirrhose et de cancer primitif du foie chez les por-
teurs chroniques du virus, soit environ3%delapopulation mondiale [1], et près
de1%delapopulation de France métropolitaine. Depuis une dizaine d’années,
le traitement prévalent pour soigner les malades atteints d’hépatite C est une
bithérapie qui associe l’interféron alpha (IFN-␣) et la ribavirine. Ce traitement
est curatif, mais il ne guérit pas tous les malades, car il manque d’efficacité
chez la moitié des patients et est souvent arrêté prématurément pour intolé-
rance. La bithérapie est un traitement lourd et contraignant : elle dure de six
à 12 mois, implique des injections répétées et engendre des effets indésirables
incommodants comme des symptômes pseudogrippaux (fièvre, maux de tête,
courbatures). En 2011, une nouvelle substance active, le télaprévir, a suscité
l’espoir d’un meilleur traitement pour les malades atteints d’hépatite C. Le téla-
prévir potentialise l’effet de la bithérapie, en permettant notamment un traitement
plus court.
Dans un article paru dans la revue Nature Biotechnology en 2011 [2], Kwong
et Kauffman de Vertex Pharmaceuticals ont retracé l’histoire mouvementée de
la conception du télaprévir. À travers ce remarquable succès en matière de
recherche et développement est mis en lumière comment la persévérance et
le savoir-faire des biologistes, chimistes et galénistes ont couronné la prise de
risques sur le choix de la cible. En écho à la découverte du saquinavir, premier
antiprotéase utilisé comme anti-VIH, le pari a été fait dans les années 1990 que
la réplication du VHC pouvait être stoppée en inhibant une activité protéase du
virus, en particulier celle de la protéine NS3-4A. Comme les deux virus sont très
différents tant par leur constitution que leur cycle viral, et comme l’importance
de NS3-4A dans l’infection par VHC n’était pas évaluée dans des systèmes bio-
logiques modèles (tableau 1), il n’était pas certain que NS3-4A soit une bonne
cible de médicament [3]. Cependant, les chercheurs avaient l’expertise dans la
conception d’antiprotéases [4] et disposaient des moyens techniques pour tester
l’effet de « petites » molécules synthétiques sur l’activité de l’enzyme, et ce sont
finalement les premiers essais d’inhibiteurs de NS3-4A sur des malades qui ont
démontré la pertinence des agents antiprotéases pour lutter contre le VHC.
Le télaprévir n’est pas issu d’une campagne de criblage à haut débit, mais d’une
modification du substrat peptidique naturel de la NS3-4A, la poly-protéine virale
NS5A-NS5B, avec comme double objectif l’amélioration de propriétés pharma-
cocinétiques et l’optimisation de l’effet biologique (tableau 2) [5]. Dans ce but,
les premiers tests d’inhibition enzymatique in vitro ont rapidement été rem-
placés par une approche cellulaire recréant des conditions proches de la réalité
physiologique, dans lesquels les inhibiteurs potentiels doivent franchir des mem-
branes et sont soumis au pH et à la force ionique des différents compartiments
cellulaires avant de produire leur effet mesuré par la réplication de l’ARN viral.
Tirés à part : E. Kellenberger
doi:10.1684/vir.2013.0476
Virologie, Vol 17, n◦1, janvier-février 2013 3
Pour citer cet article : Bourel-Bonnet L, Kellenberger E. Le télaprévir : de l’inhibiteur de protéase au médicament contre l’hépatite C. Virologie 2013; 17(1) : 3-5 doi:10.1684/vir.2013.0476
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 25/05/2017.

Journal Identification = VIR Article Identification = 0476 Date: February 19, 2013 Time: 1:0 pm
éditorial
Tableau 1. Validation de NS3-4A en tant que cible
thérapeutique pour lutter contre le virus de l’hépatite C (VHC).
Les critères de validation
1. L’effet antiviral de l’inactivation de NS3-4A est démontré
Dans un modèle cellulaire de réplication de VHC (1999)
Dans un modèle animal de l’hépatite C (2004)
Chez les malades, lors d’essais cliniques «preuve de
concept »(2003)
2. La structure tridimensionnelle de NS3-4A (1996)
Est connue et peut servir de guide pour l’optimisation de
candidats-médicaments
Ne révèle pas un domaine susceptible de lier avec une forte
affinité des «petites »molécules synthétiques
3. Un essai fiable et automatisé permet de mesurer l’effet
d’inhibiteurs
Seul le point 3 était satisfait dans les années 1990, les dates de publi-
cation associées aux autres points sont données entre parenthèses. Les
évaluations favorable ou défavorable des critères 1 et 2 sont indiquées res-
pectivement par les symboles et .
Tableau 2. Caractéristiques d’un candidat-médicament idéal.
Propriétés de la
substance active
Paramètres considérés lors la
conception du télaprévir
Pharmacocinétique
Solubilité et passage
des membranes
Taille, surface polaire
Biotransformation/
métabolisme
Liaisons peptidiques hydrolysables
Élimination
Réponse biologique
optimale
Efficacité Affinité nM pour NS3-4A
Effets secondaires
limités
Affinité réduite d’un facteur
≥500 pour les protéases
humaines
Un décapeptide centré sur la liaison peptidique clivée par
NS3-4A a constitué le point de départ de la conception
du télaprévir, et les changements réalisés ont globalement
tendu à la réduction de la taille et du caractère pepti-
dique de l’inhibiteur. Cette démarche a été facilitée par la
synthèse sur support solide, qui, en donnant accès rapi-
dement à une grande quantité d’analogues de peptides ou
de mimes de peptides, a permis de délimiter les prérequis
structuraux pour les inhibiteurs de NS3-4A. Des informa-
tions complémentaires ont été apportées par les structures
cristallographiques de la protéase (figure 1). Là encore,
les chercheurs ont été confrontés à une situation difficile,
puisque le site actif de NS3-4A ciblé par les inhibiteurs
est un sillon peu profond, flexible et globalement éloigné
des canons attendus pour des protéines dites « druggable »,
c’est-à-dire des protéines pouvant lier avec une haute affi-
nité une « petite » molécule (<500 Da) [3].
Le meilleur des inhibiteurs testés, le télaprévir, a été syn-
thétisé en 2000. Ce n’est qu’une dizaine d’années plus
tard qu’il a été approuvé par les autorités sanitaires. Ce
laps de temps recouvre plusieurs événements, dont le pre-
mier a été l’évaluation du potentiel thérapeutique de cette
molécule sur les modèles cellulaires et animaux. En 2003,
l’entrée en phase clinique du premier inhibiteur de NS3-
4A, le BILN2061 de chez Boehriger Ingelheim, a constitué
un élément décisif pour la continuation du programme de
recherche et développement du télaprévir. À ce stade, il
a fallu adapter les procédés de synthèse à la production
à l’échelle industrielle et les 20 étapes de la synthèse des
premiers lots employés dans les tests précliniques ont été
réduites à 14 pour la forme définitive employée dans les
essais cliniques (à titre de comparaison, la moyenne pour
un médicament est de 7 étapes). Pour passer à l’utilisation
chez l’homme, la formulation du télaprévir a été particuliè-
rement délicate en raison des propriétés physicochimiques
peu favorables à une bonne absorption par voie orale (masse
moléculaire et surface polaire élevées, très faible solubilité
dans l’eau) et d’une tendance à adopter des formes cris-
tallines polymorphes, dont les cinétiques de dissolution et
les limites de solubilité dans les fluides biologiques sont
différentes, compromettant la reproductibilité des lots et
leur efficacité. De nombreux essais infructueux ont été ten-
tés avant d’obtenir la formulation satisfaisante, à savoir
une dispersion de la forme amorphe stabilisée à l’aide
d’un polymère et d’un tensioactif dans un comprimé pel-
liculé qu’il faut s’abstenir de croquer ou d’écraser afin
de garder le bénéfice de la formulation. L’efficacité et la
sécurité du télaprévir ont ensuite été étudiées chez des
volontaires sains puis des patients atteints d’hépatite C. Si
l’antiprotéase diminue bien la charge virale, il sélectionne
aussi très rapidement des virus résistants, en particulier
chez les patients infectés par le virus de génotype 1a et
chez ceux en échec thérapeutique à l’issu du traitement
par la bithérapie IFN-␣/ribavirine. Les essais cliniques ont
par conséquent abouti à la mise en place d’une trithérapie
qui associe le télaprévir à la bithérapie IFN-␣/ribavirine,
dans un protocole qui vise à maîtriser les effets indési-
rables propres au télaprévir. Le télaprévir permet d’obtenir
un gain de 30 % pour l’élimination virale (40 à 45 % en
bithérapie versus 70 à 75 % en trithérapie chez les patients
naïfs), et par conséquent une durée de traitement réduite.
Malgré les efforts déployés, la trithérapie n’est pas LE trai-
tement idéal de l’hépatite C, car les effets secondaires du
télaprévir sont lourds et fréquents (troubles cutanées avec
rash et prurit, anémie pouvant nécessiter des transfusions,
notamment chez le patient cirrhotique) et s’additionnent à
ceux de l’IFN-␣et de la ribavirine. De plus, la trithérapie
4Virologie, Vol 17, n◦1, janvier-février 2013
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 25/05/2017.

Journal Identification = VIR Article Identification = 0476 Date: February 19, 2013 Time: 1:0 pm
éditorial
O
O
O
OO
O
NH
NH
Télaprévir
(680 Da)
N
NN
H
N
N
H
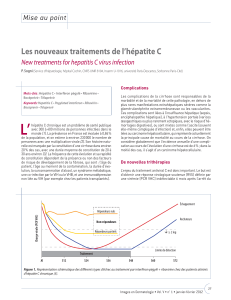
Figure 1. Le complexe télaprévir/NS3-4A. La structure tridimensionnelle du complexe, déterminée par cristallographie aux rayons X (code
PDB : 3SV6), révèle que le télaprévir (en vert) vient se poser sur la protéase (en jaune). L’image du milieu montre les «surfaces »des
molécules empilées, celle de droite détaille les atomes des résidus impliqués dans les liaisons covalente et hydrogène établies entre le
télaprévir et la protéase, dont la chaîne principale est schématisée par un ruban.
télaprévir/IFN-␣/ribavirine ne permet toujours pas de soi-
gner les malades qui ne supportent ou ne répondent pas
à l’IFN-␣, est indiquée uniquement chez les patients pré-
sentant le génotype 1 du VHC et est d’un coût élevé
(2295,83 euros TTC les 42 comprimés en officine de ville).
En conclusion, le télaprévir est le premier inhibiteur de
protéase de VHC à avoir obtenu l’autorisation de mise
sur le marché en septembre 2011 en Europe sous le nom
d’Incivo®et la commission de transparence de la Haute
Autorité de santé a qualifié son service médical rendu
d’« important ». Ce nouveau médicament, dont le déve-
loppement a réellement constitué un tour de force, ouvre
la voie à une série de nouvelles molécules ciblant le
VHC : l’antiprotéase de Schering-Plough, le bocéprévir,
vient d’être approuvé sous le nom de Victrelis®,etdes
dizaines de nouvelles molécules sont actuellement en phase
clinique, parmi elles d’autres antiprotéases, mais aussi des
inhibiteurs nucléosidiques et non nucléosidiques de l’ARN
polymérase virale NS5B et des inhibiteurs de NS5A [6].
Certaines de ces nouvelles molécules agissent sur plusieurs
génotypes et leur combinaison permet d’envisager des trai-
tements sans IFN dans un futur proche.
Conflits d’intérêts : aucun.
Références
1. World Health Organisation. Retrieved 28/08/2012, from: http://www.
who.int/csr/disease/hepatitis/en/index.html.
2. Kwong AD, Kauffman RS. Discovery and development of telaprevir:
an NS3-4A protease inhibitor for treating genotype 1 chronic hepatitis C
virus. Nat Biotechnol 2011 ; 29 : 993-1003.
3. Gashaw I, Ellinghaus P, Sommer A, Asadullah K. What makes a good
drug target? Drug Discov Today 2011 ; 16 : 1037-43.
4. Turk B. Targeting proteases: successes, failures and future prospects.
Nat Rev Drug Discov 2006;5:785-99.
5. Ursu O, Rayan A, Goldblum A, Oprea T. Understanding drug-likeness.
Wiley Interdiscip Rev Comput Mol Sci 2011;1:760-81.
6. Fusco DN, Chung RT. Novel therapies for hepatitis C: insights from
the structure of the virus. Annu Rev Med 2012 ; 63 : 373-87.
Virologie, Vol 17, n◦1, janvier-février 2013 5
Copyright © 2017 John Libbey Eurotext. Téléchargé par un robot venant de 88.99.165.207 le 25/05/2017.
1
/
3
100%