Chapitre_18_-_Alcool..

!"#$%&'()*+),)-.&%/#&%01)2()301.&%01),)4(5)#4.0045) ) 6!78)
*)
!9-68:;<)*+),)-!:8=-:8>?)@<)A>?!:8>?),)B<7)-B!>>B7)
6-;:8<)*),)6;<7<?:-:8>?)
8C ;<B-:8>?)7:;D!:D;<E;<-!:8=8:<)6>D;)B<7)-B!>>B7)<:)B<7)69<?>B7)
)
*C
7&'F.&F'()2(5)#4.0045)(&)2(5)$"G1045C)
)
•
B(5)#4.0045))
B(5) #4.0045) $055H2(1&) F1) I'0F$()301.&%011(4)
"J2'0KJ4() L>9
M) '(4%G) N) F1)
#&0O() 2() .#'P01() &G&'#/#4(1&
)Q-RSTC) 845) $(F/(1&) U&'()
'(I'0F$G5)(1)V).4#55(5),)
<K(O$4())
)
)
WFXYX04)
YXOG&"J4PFXYX04)
A0'OF4()
&0$040I%ZF()$4#1()
)
)
)
)
!4#55()2()4[#4.004)
)
)
)
)
)
!"#$%&'"()(*$%+,-.(/"(#012$3,/(45675(".1(&'$/-+-0(89$/:,,/(3'//$-%";((
)
•
B(5)$"G1045)
B(5)$"G1045)$055H2(1&)F1)
I'0F$()"J2'0KJ4(
)L>9)(5&)4%G)N)F1)
#&0O()2().#'P01()-RV
)#$$#'&(1#1&)N)F1)
.J.4()
#'0O#&%ZF(
C))
B#) $4F$#'&) 2(5) $"G1045) 01&) 2(5) 10O5) .0F'#1&5) .015#.'G5) $#') 4[F5#I(C) =0F5) '(&%(12'(\) #F) O%1%OFO) 4()
$"G104)Q.%X.01&'(TC))
) )
YC
7%I1#&F'()%13'#'0FI()2(5)#4.0045)
)
<1)5$(.&'05.0$%()%13'#'0FI(M)4(5)#4.0045)$'G5(1&(1&)F1()
P#12()2[#P50'$&%01)
(1&'()V]]])(&)V^]]).OX*)2F()N)4#)/%P'#&%01)2[G401I#&%01)2()4#)4%#%501)>X9
C
)
@#15)4().0'$5)$F'M)0F)2#15)F1()504F&%01).01.(1&'G(M)4(5)301.&%015)"J2'0KJ4(5)
501&)#550.%G(5)$#')4%#%501)"J2'0IH1(C)!(.%)(K$4%ZF()ZF()4#)P#12()50%&)4#'I(C)
(
!"#$%&'"()("3(.,/'1-,3(1%<.(8-/'0"(8$3.('3(.,/=$31($*%,1-&'"(:,##"(44/>?(/".(
@%,'*".(2A8%,BA/".(3"(.,31(*/'.($..,:-0.(*$%(/-$-.,3(5("1(,3(,C."%="('3"(C$38"(
+-3"(D(6EFF:#GH;(
)
VC
;G#.&%/%&G)#&&(12F()$0F')4(5)#4.0045)(&)$"G1045)
)
#C
;G#.&%/%&G)2(5)#4.0045))
)
)
)
)
PC
;G#.&%/%&G)2(5)$"G1045))
)
)
)
OH
CO
H
O
H
!
!
Phénol
W#12()2()/%P'#&%01)
2[G401I#&%01)2()4#)4%#%501)>X9)
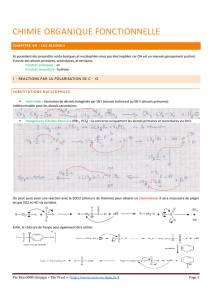
Exemple,:,Spectre,infrarouge,de,l’hexan-1-ol,

!"#$%&'()*+),)-.&%/#&%01)2()301.&%01),)4(5)#4.0045) ) 6!78)
Y)
88C 6;>6;8<:<7)-!8@>XW-78_D<7)@<7)-B!>>B7)<:)@<7)69<?>B7)
@F)$0%1&)2()/F()#.%20XP#5%.%&G)2()W'015&(2M)4(5)#4.0045)501&)201.)2(5)
#O$"04J&(5
C)
)
*C D1)#4.004)(5&)F1)#.%2()Q$(F&).G2(')F1)9`T)
)
4,'*/"()(
)
*I$(8'(:,'*/"
()(HEGHJ(
4,##"31(,C1"3-%('3($/:,,/$1"
(K((
)
)
)
)
)
)
)
)
)
)
)
-F&'()OG&"02()2[0P&(1&%01),))
$#')'G#.&%01)2[0KJ20'G2F.&%01)#/(.)F1)OG)#4.#4%1M)$#')(K(O$4()4()502%FO)OG,%ZF()?#Q5T
))
(
LB"#*/"($=":(/9012$3,/()(
4,'*/"(L1M75NL1M7G?(5OP@Q(,))<&a>9)`)(a)b)<&X>a)`)c)9YQIT))
4,'*/"(R$SNR$(,))))))))))))))))))))))))))))))))?#Q5T)b)?#`)`)(a))))))))))))))))))))))))))))))))))))
))))))))))))))
))))))))))))))W%4#1),
));a>9)`)?#Q5T)b)?#`)`);>a)`)c)9YQIT)
)
)
YC D1)#4.004)(5&)F1()P#5()Q$(F&).#$&(')F1)9`T)
)
4,'*/"()(
)
)
*I$(8'(:,'*/"()(GO(
4,##"31(,C1"3-%('3(-,3($/TA/,B,3-'#(K((
(
(
(
(
(
(
(
(
!0.'#0()(8-$@%$##"(8"(*%08,#-3$3:"(8"(/9$/:,,/()(
(
(
) ) ) )
W%4#1
))
)
_
milieu acide
OH
_
_
R
H
O
_
RH
H
alkyloxonium
milieu
basique
O
_
_
R
alcoolate alcool
pKa 16-18 pKa -2
Diisopropylamidure de lithium (LDA)
14
HO H2O
pKa
50
, Li+
butyllithium (BuLi) butane
38
NH2-, Li+NH3
ion amidure ammoniac
36
N
Li+
N
H
35
H-, Na+H2
Hydrure de sodium Dihydrogène
R-OH
R-O-16-18
Alcool
Alcoolate
Ph OH
Ph O10
E° (V)
R-OH R-O- + 1/2 H2(g)
Na+Na
-1
-2,71

!"#$%&'()*+),)-.&%/#&%01)2()301.&%01),)4(5)#4.0045) ) 6!78)
V)
VC 6'0$'%G&G5)#.%20XP#5%ZF(5)2F)$"G104)
• B()$"G104)(5&)F1)
#.%2(),)$(F&).G2(')F1)$'0&01)(&)30'O(')4[%01)$"G104#&()
,))
) )
$d#Q6">9E6">XT)b)*]
)
)))))))))))))))6"G104)))))))))6"G104#&()
4,##"31$-%"()((
)
)
)
LB*/-:$1-,3()((
)
)
)
)
)
)
)
)
)
)
)
4,##"31(,C1"3-%(/9-,3(*203,/$1"(K((
)
)
)
)
)
)
)
)
)
• B().#'#.&H'()P#5%ZF()5(401)W'e15&(2)1()5('#)$#5)G&F2%G)2#15)4().#5)2(5)$"G1045M).#')&'H5)O#F/#%5()P#5(C)
)
)
888C 6;>WB<f-:8_D<)B8<<)-)B-);<-!:8=8:<)@<7)-B!>>B7)<?)!98f8<)>;g-?8_D<),)
-!:8=-:8>?)?<!<77-8;<
)
)
#C
<K$40%&#&%01)2()4#)1F.4G0$"%4%()2()4[#4.004)
B[#&0O()2[0KJIH1()2()4#)301.&%01)"J2'0KJ4()(5&)F1)5%&()1F.4G0$"%4(),)01)$(F&)(1/%5#I(')2[F&%4%5(')F1)#4.004)(1)&)ZF()1F.4G0$"%4()
2#15)4#)7?)5F%/#1&(),))
)
<1)$'#&%ZF(M).(&&()'G#.&%01)1[(5&)$#5)0P5('/G().#')
&'0$)4(1&())
Ph OH Ph O+ H
6'0P4HO()
704F&%01)
)
)
)
)
)
)
)
)
)
)
)
)
δ+
δ−

!"#$%&'()*+),)-.&%/#&%01)2()301.&%01),)4(5)#4.0045) ) 6!78)
S)
PC
<K$40%&#&%01)2()4[G4(.&'0$"%4%()2()4[#4.004)
)
>1)#)/F)ZF()4[#&0O()2().#'P01()$0'&)4#)301.&%01)"J2'0KJ4()G&#%&)F1)5%&()G4(.&'0$"%4(),)01)$(F&)(1/%5#I(')F1()7?)0F)F1()G4%O%1#&%01)
5F')F1)#4.004),)))
7?),))
)
) )
!(&&()'G#.&%01)1[(5&)$#5)0P5('/G()Q&'0$)4(1&(T))
)
<4%O%1#&%01),))
)
)!(&&()'G#.&%01)1[(5&)$#5)0P5('/G()Q&'0$)4(1&(T)
)
)
)
)
)
)
)
)
)
)
)
)
)
)
)
)
)
)
)
)
)
)
OH
Cl
Cl HO
6'0P4HO()
704F&%015)
)
)
)
)
)
)
)
)
)
)
)
)
)
)
)
)
)
)
)
)
)
)
)
)
)
)
)
)
7?Y)
`)9>X)`)#.%2().01hFIFG)
δ+
δ−

!"#$%&'()*+),)-.&%/#&%01)2()301.&%01),)4(5)#4.0045) ) 6!78)
^)
6-;:8<)Y),)D:8B87-:8>?)@<7)-B!>>B7)<?):-?:)_D<)?D!B<>698B<)Q-6;<7)-!:8=-:8>?T)
)
☹ ☺
) )
*C
7J1&"H5()2[G&"('0KJ2(5)$#')4#)OG&"02()2()i%44%#O501)
)
#C
!012%&%015)0$G'#&0%'(5)(&)P%4#1C)
)
•
;G#.&%35),)
-4.004#&();X>X)
) ) )@G'%/G)"#40IG1G);[XR)$'%O#%'()Q0F)5(.012#%'()$(F)(1.0OP'GT))
•
:(O$G'#&F'(),)
#OP%#1&(C
))
•
704/#1&),)
$04#%'(M)#$'0&%ZF()&J$%ZF(O(1&)4()@f7>)QF&%4%5#&%01)2();>XM)201.)504/#1&)101)#ZF(FKT
))
)
)
W%4#1),)
)
)
)
)
LB"#*/"()((
(
(
)
)
PC
fG.#1%5O()
)
B()2G'%/G)"#40IG1G)(5&)$'%O#%'()Q0F)5(.012#%'()O#%5)$(F)(1.0OP'GT),)4#)5FP5&%&F&%01)1F.4G0$"%4()5F%&)F1)OG.#1%5O()2()&J$()))
)
fG.#1%5O(
),)
)
)
)
)
)
)
)
)
.C
!#'#.&G'%5&%ZF(5)2()4#)'G#.&%01)
:+(:2$*-1%"(J()(UR
))
;#$$(4(')4(5).#'#.&G'%5&%ZF(5)2()4#)'G#.&%01)5F')4[(K(O$4()2()4#)'G#.&%01)2()4[G&"#104#&()2()502%FO)#/(.)4()Q7TXYX."40'0PF(C)
)
)
)
)
)
)
)
)
)
)
)
)
)
)
)
)
)
R-OH
mauvais
nucléophile
base
ou métal alcalin R-O
bon
nucléophile
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
1
/
14
100%