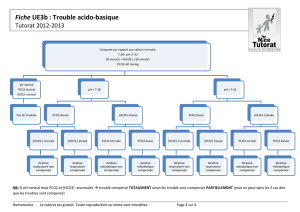
Le rein dans l`équilibre acido

Le rein dans l’équilibre acido-basique de
l’organisme
•L’eau pure contient 10-7moles/l de H+.
•pH = - log [H+] = 7
•Un acide est une substance qui libère des H+. Si on ajoute
un acide dans l’eau, [H+] augmente et le pH diminue (pH<7).
Un acide fort se dissocie complètement alors qu’un acide
faible se dissocie partiellement.
•AH A- + H+ acide fort
•AH A- + H+ acide faible
•Une base accepte des H+. Une base dans l’eau donne un pH
>7.
•Dans une solution où le pH passe de 7 à 3, [H+] est x par
10 000

Importance de la stabilité du pH du milieu intérieur
-le pH affecte la structure des protéines : dénaturation des protéines
(enzymes) empêche leur fonctionnement.
Dénaturation

Importance de la stabilité du pH du milieu intérieur
-le pH affecte le fonctionnement des neurones. Explication :
Déficit de H+dans le VEC (alcalose)efflux de H+cellulaire, compensé sur le plan électrique par un
influx de K+.L’ de [K+]i dépolarise les neurones hyperexcitabilité .Au niveau musculaire : spasmes,
tétanies, convulsions, mort par paralysie respiratoire.
Al’inverse, l’excès de H+ dans le VEC (acidose)influx de H+ compensé par un efflux de K+.L’ de [K+]i
entraîne une hyperpolarisation des neurones hypoexcitabilité et dépression de l’activité cérébrale
(confusion, désorientation puis coma).

Causes possibles de perturbation du pH du plasma
Certains aliments contiennent des acides faibles, par exemple le vinaigre
ou les fruits (acide citrique, acide malique…).

Causes possibles de perturbation du pH du plasma
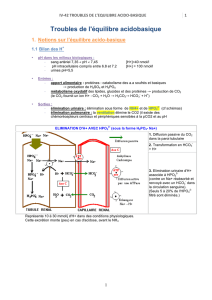
Le métabolisme produit des acides :
-acides volatiles.La respiration cellulaire libère du CO2dans le sang. CO2
se combine à l’eau pour former de l’acide carbonique :
-CO2 + H2O H2CO3HCO3
-+ H+
La paroi de l’estomac produit de l’acide chlorhydrique HCl. Lors de
vomissements,la perte de HCl tend à rendre le plasma plus alcalin.
-acides non volatiles. Les muscles en activité libèrent de l’acide lactique
dans le sang. La dégradation des acides aminés soufrés (méthionine)
produit de l’acide sulfurique H2SO4.
 6
6
 7
7
 8
8
 9
9
 10
10
 11
11
 12
12
 13
13
 14
14
 15
15
 16
16
 17
17
 18
18
 19
19
 20
20
 21
21
 22
22
 23
23
 24
24
 25
25
 26
26
 27
27
 28
28
1
/
28
100%