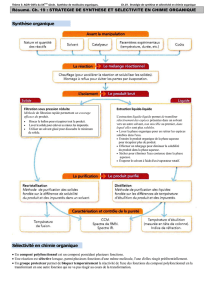
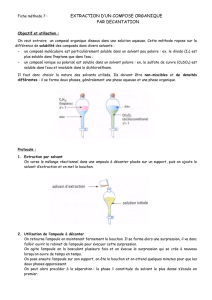
Exercices : stratégie et sélectivité en chimie organique

Terminale S www.sciencesphysiques.info
Corrections d’exercices : stratégie et sélectivité en chimie organique Page 1 / 5
Stratégie et sélectivité en chimie organique
Correction d’exercices
Exercice n°3 page 492
a. Formule brute du 2-nitrobenzaldéhyde : C
7
H
5
O
3
N
Masse molaire (notée M
1
) : M
1
= 151 g.mol
-1
Quantité de matière introduite :
1
1
1
M
m
n== 3,3.10-3 mol
b. Quantité de matière (notée n2) d’acétone (C3H6O). On note sa masse molaire M2.
M2 = 58 g.mol-1
2
2
2
MV
n×ρ
= avec 1
L.g 790
−
=ρ
n
2
= 1,4.10
-2
mol
c.
Quantité d’ions hydroxyde (n
3
) : n
3
= c × V = 5,0.10
-3
mol
d.
L’eau distillée sert de solvant.
Exercice n°4 page 493
a.
b. D’après les nombres stœchiométriques, le réactif limitant est le 2-nitrobenzaldéhyde.
Exercice n°5 page 493
Schéma d’un montage à reflux
avec ballon bicol.
Exercice n°6 page 493
a.
Lors de la manipulation, il faut porter une blouse fermée et des lunettes de protection si nécessaire.
b.
Le 2-nitrobenzaldéhyde est à manipuler avec des gants pour éviter les irritations cutanées, et de
préférence sous la hotte pour éviter une irritation des voies respiratoires.

Terminale S www.sciencesphysiques.info
Corrections d’exercices : stratégie et sélectivité en chimie organique Page 2 / 5
Exercice n°7 page 493
a. Il faut essorer le solide pour le séparer du mélange réactionnel, puis le laver.
b. Ces opérations sont effectuées grâce à un filtre Büchner placé sur une fiole à vide.
Exercice n°8 page 493
a. Après séchage, on peut mesurer la température de fusion du produit, réaliser une CCM ou des
analyses spectrales.
b. Pour purifier le solide, on effectue une recristallisation.
Exercice n°17 page 496
a. La solution possède un aspect laiteux car c’est une émulsion : suspension de fines gouttelettes
d’eugénol (phase organique) dans l’eau. Cette émulsion diffuse la lumière et donne son aspect
laiteux à la solution.
b. Pour récupérer l’eugénol, on va réaliser une extraction liquide – liquide.
c. On va choisir un solvant non miscible au solvant initial (ici l’eau) et dans lequel l’espèce dissoute
(ici l’eugénol) est plus soluble que dans le solvant initial. Dans le cas présent, on peut donc choisir
l’éthoxyméthane (appelé éther), le dichlorométhane, ou le cyclohexane.
Pour faciliter l’évaporation du solvant à l’évaporateur rotatif, on choisira un solvant ayant une faible
température d’ébullition (comme l’éther ou le dichlorométhane).
On préfèrera finalement l’éther, moins toxique que de dichlorométhane.
d. Protocole expérimental :
- Verser dans une ampoule à décanter la solution contenant l’eugénol.
- Ajouter 20 mL d’éther.
- Agiter l’ampoule à décanter en dégazant de temps en temps.
- Laisser décanter puis séparer les phases.
- Extraire l’eugénol restant de la phase aqueuse avec deux fois 20 mL d’éther.
- Rassembler les phases organiques.
- Sécher la phase organique à l’aide de sulfate de magnésium anhydre.
- Filtrer.
- Evaporer le solvant à l’évaporateur rotatif.
Exercice n°20 page 497
a. Etapes de la synthèse :
- Transformation : « Dans un ballon… 30 minutes ».
- Traitement : « Laisser refroidir… eau froide ».
- Identification : « Mesurer sa température de fusion ».
- Traitement : « Si nécessaire, effectuer une recristallisation… ».
- Identification : « Mesurer la température de fusion du produit recristallisé ».
Les réactifs sont l’acide de Meldrum, le diméthylaminobenzaldéhyde et le solvant est l’eau.
b. La température de fusion du produit brut réactionnel est différente de celle du produit purifié. La
purification était donc justifiée. De plus la température attendue (tables) est de 173°C, et celle
obtenue pour le brut n’était que de 166°C.

Terminale S www.sciencesphysiques.info
Corrections d’exercices : stratégie et sélectivité en chimie organique Page 3 / 5
c. Formule brute du produit
D’après l’équation de la réaction, on constate que la réaction de Knoevenagel, est une élimination
(ici élimination de H
2
O).
Remarque : lors d’une élimination d’eau, on ne fait pas toujours apparaître dans l’équation de la réaction
l’eau formée dans les produits. On peut écrire « - H
2
O » sous la flèche de l’équation.
Les atomes présents dans la molécule formée sont donc ceux présents dans les deux réactifs, moins
ceux présents dans une molécule d’eau. La formule brute du produit formé est donc C
15
H
17
O
4
N.
Calcul du rendement (notons r le rendement de cette synthèse)
attendue
obtenue
n
n
r= avec nattendue = nmax = 5 mmol (le mélange est stœchiométrique)
et nobtenue = =
M
m 3,6.10-3 mol d’où r = 0,72 (ou r = 72%)
d. L’espèce formée est solvatochrome car son spectre d’absorption (et donc sa couleur) est différent
selon le solvant dans laquelle elle se trouve.
Exercice n°3 page 508
Espèces polyfonctionnelles :
a. classe des alcènes et des alcools
b. classe des amines et des acides carboxyliques
c. classe des alcools et des aldéhydes
e. classe des cétones et acides carboxyliques
d et f ne sont pas des molécules polyfonctionnelles
Exercice n°5 page 508
1. La transformation présentée n’est pas sélective car deux groupes caractéristiques du réactif sont
modifiés.
2. a. La transformation n°2 est une protection et est sélective. Seul le groupe carbonyle a été protégé.
b. La transformation n°4 est une déprotection.
c. Les transformations n°2,3 et 4 sont sélectives. Dans chacun des cas, une seule classe fonctionnelle est
modifiée.
Exercice n°16 page 513
a. L’aspartame est bien une molécule appartement entre autre à la classe fonctionnelle des amides :

Terminale S www.sciencesphysiques.info
Corrections d’exercices : stratégie et sélectivité en chimie organique Page 4 / 5
b. La molécule d’aspartame peut être présente sous la forme d’une espèce chargée. En effet un ion H
+
peut migrer du groupe carboxyle vers le groupe amino :
c. Il faut protéger la fonction acide (2) pour qu’elle ne forme pas de liaison peptidique.
Si on ne la protège pas, la réaction suivante peut avoir lieu :
d. De même si on ne protège pas la fonction amine de l’acide aspartique, une liaison peptidique peut
s’établir avec celle-ci :
e. Acide aspartique protégé :
Dipeptide protégé après le couplage peptidique :
f. Si l’on protège le groupe amino avec le groupe R
1
-CO- , alors on fait apparaître un groupe amide.
Lors de la déprotection de ce groupe, on risque de transformer la liaison peptidique qui nous
intéresse.
g. Si l’on protège le groupe carboxyle avec CH
3
- , un groupe ester va se former.
Or, lors de sa déprotection, on risque de transformer le groupe ester de la phénylalanine.

Terminale S www.sciencesphysiques.info
Corrections d’exercices : stratégie et sélectivité en chimie organique Page 5 / 5
h. Synthèse sur les critères de choix des groupes protecteurs lors d’une synthèse organique
Lors d’une synthèse organique, il est courant que les réactifs utilisés soient des espèces
polyfonctionnelles. Il faut donc envisager une, voire plusieurs étapes de protection puis de déprotection de
certains groupes caractéristiques de ces molécules.
Pour choisir les groupes protecteurs les plus adaptés, il faut s’interroger sur l’efficacité de la protection et
aussi sur celle de la déprotection.
Ainsi l’on recherchera des groupes protecteurs sélectifs, c'est-à-dire qui transforment les groupes à
protéger sans modifier les autres. Les réactions associées aux étapes de protection doivent aussi avoir le
meilleur rendement possible.
D’autre part, les étapes de déprotection doivent régénérer le groupe protégé sans modifier le reste de la
molécule, et se faire elles aussi avec le meilleur rendement possible.
Une stratégie de protection – déprotection pertinente serait de déprotéger plusieurs groupes en une seule
étape : on améliore ainsi le rendement global de la synthèse.
1
/
5
100%